- 医療関係者向けホーム
- フィルグラスチムBS注「モチダ」
- Clinical Study:乳癌患者対象試験(国内第Ⅲ相試験) 試験の概要
 Clinical Study乳癌患者対象試験(国内第Ⅲ相試験)
Clinical Study乳癌患者対象試験(国内第Ⅲ相試験)
「禁忌を含む使用上の注意」等は添付文書をご参照ください。
試験の概要 乳癌患者対象試験(国内第Ⅲ相試験)1)
1) 持田製薬販売社内資料(臨床薬理試験―乳癌患者におけるがん化学療法による好中球減少症に対する好中球数回復作用の検討―)
<承認時評価資料>
目的
FEC療法(フルオロウラシル、エピルビシン、シクロホスファミド併用療法)を術前あるいは術後補助療法として施行予定の乳癌患者を対象に、本剤投与による好中球の回復効果を好中球減少(好中球絶対数< 1,000/mm3)期間に基づき評価する(サイクル2のみ)。
また、本剤投与時の安全性を評価する。
試験デザイン
非ランダム化多施設共同オープン試験
対象
組織学的に浸潤性乳癌と診断された臨床病期Ⅰ~Ⅲの女性患者(20歳以上70歳未満)
投与方法
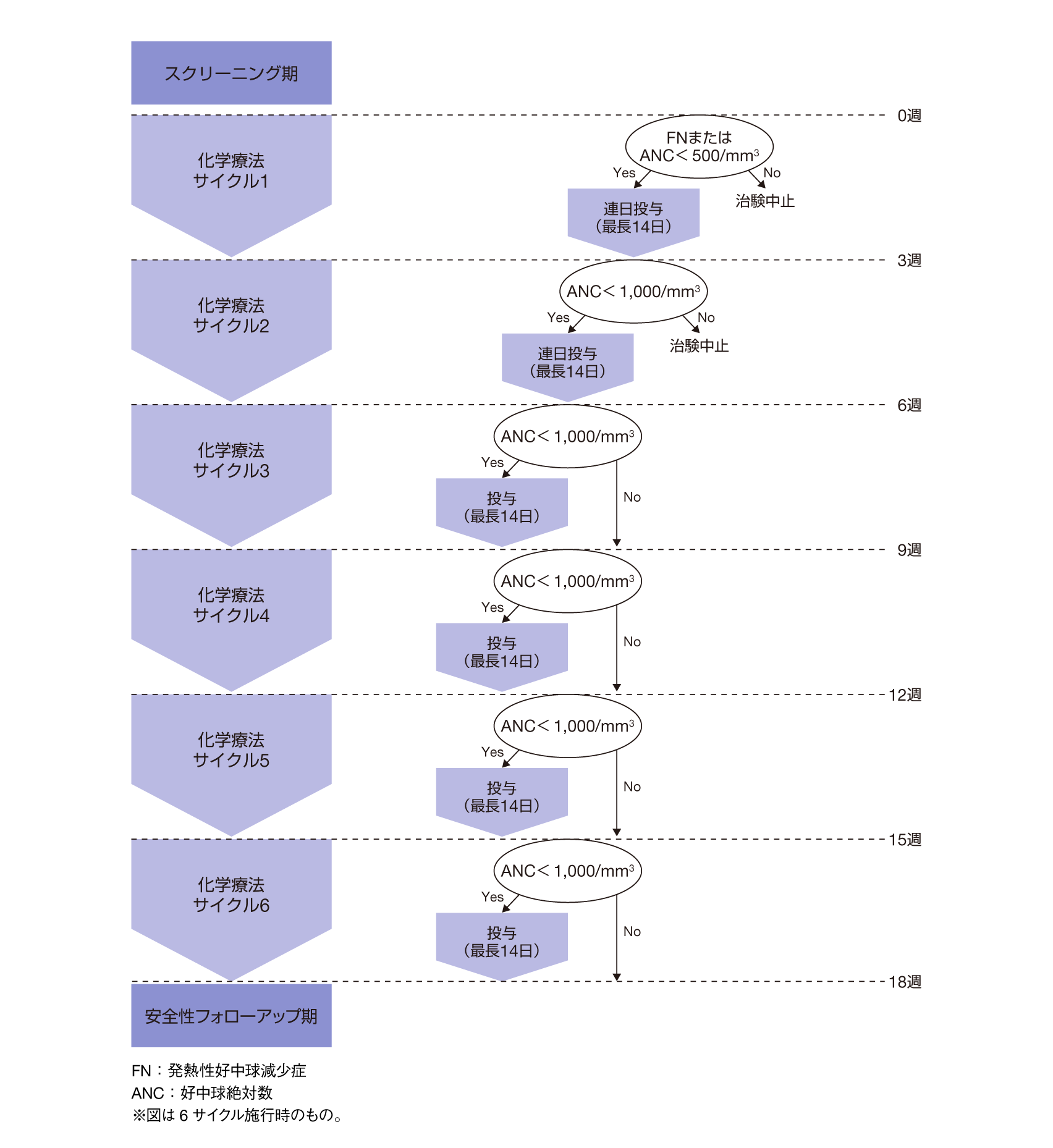
化学療法としてFEC療法を、3週間を1サイクルとして、4あるいは6サイクルまで実施した。
化学療法サイクル1では、Day 1に化学療法を開始し、発熱性好中球減少症〔好中球絶対数1,000/mm3未満で発熱(腋窩温で38℃以上)〕が発現した場合あるいは好中球絶対数が500/mm3未満を確認した場合に、本剤50μg/m2を1日1回最長14日間連日皮下投与した。
化学療法サイクル2では、好中球絶対数が1,000/mm3未満に減少した時点から本剤の投与を開始し、50μg/m2を1日1回最長14日間連日皮下投与した。
化学療法サイクル3以降は、好中球絶対数が1,000/mm3未満を確認した後に、本剤50μg/m2を1日1回最長14日間皮下投与した(非連日投与も許容)。
評価項目
<有効性>
主要評価項目
サイクル2における好中球減少期間(好中球絶対数< 1,000/mm3)
副次的評価項目
発熱性好中球減少症の発現率、本剤投与後の抗G-CSF抗体産生の発現状況
<安全性>
安全性評価項目
有害事象および副作用の発現状況、臨床検査値の推移、血圧、脈拍数の推移