- 医療関係者向けホーム
- フィルグラスチムBS注「モチダ」
- Information:薬効薬理
 Information
Information
薬効薬理
臨床薬理試験
1.単回皮下投与試験1)
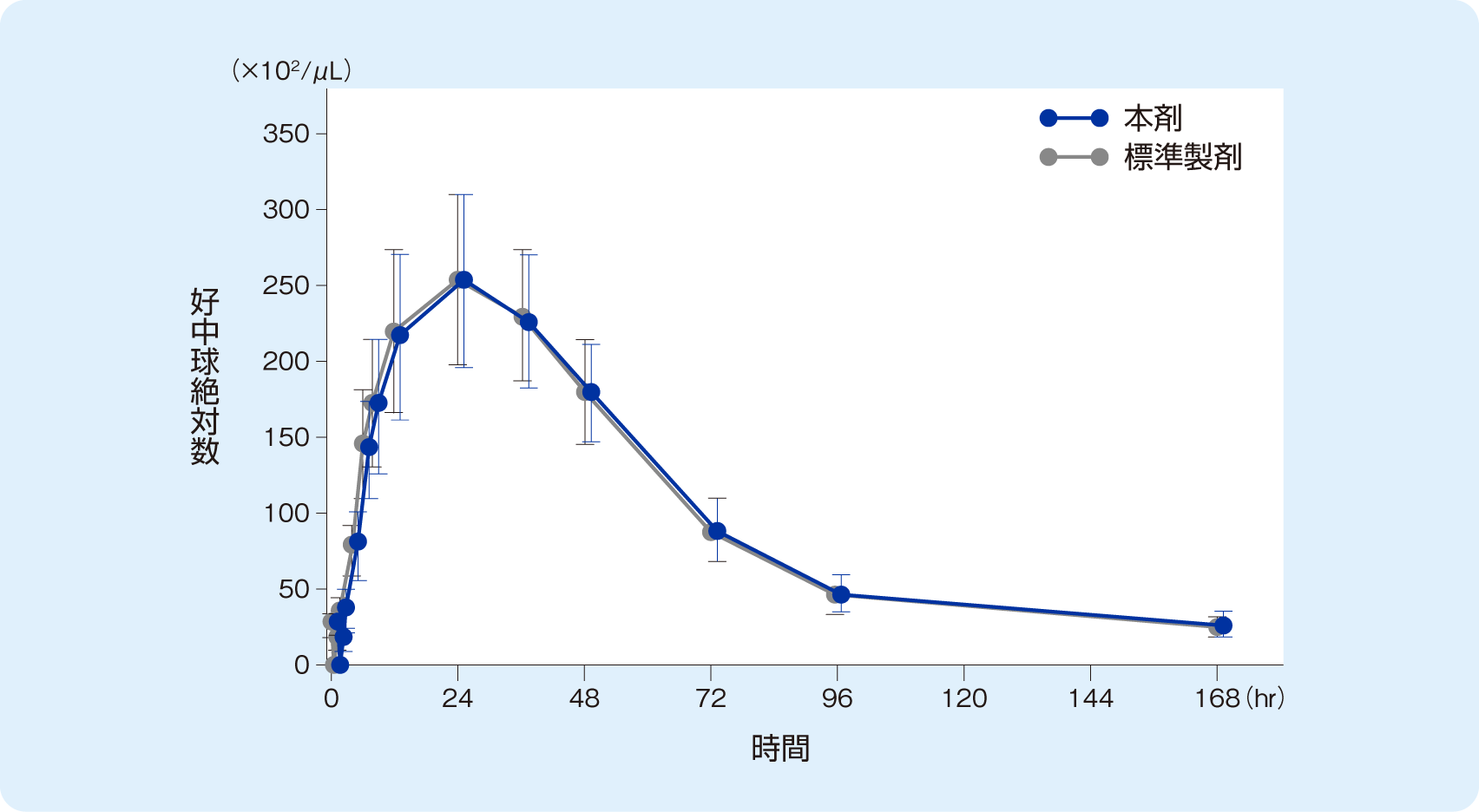
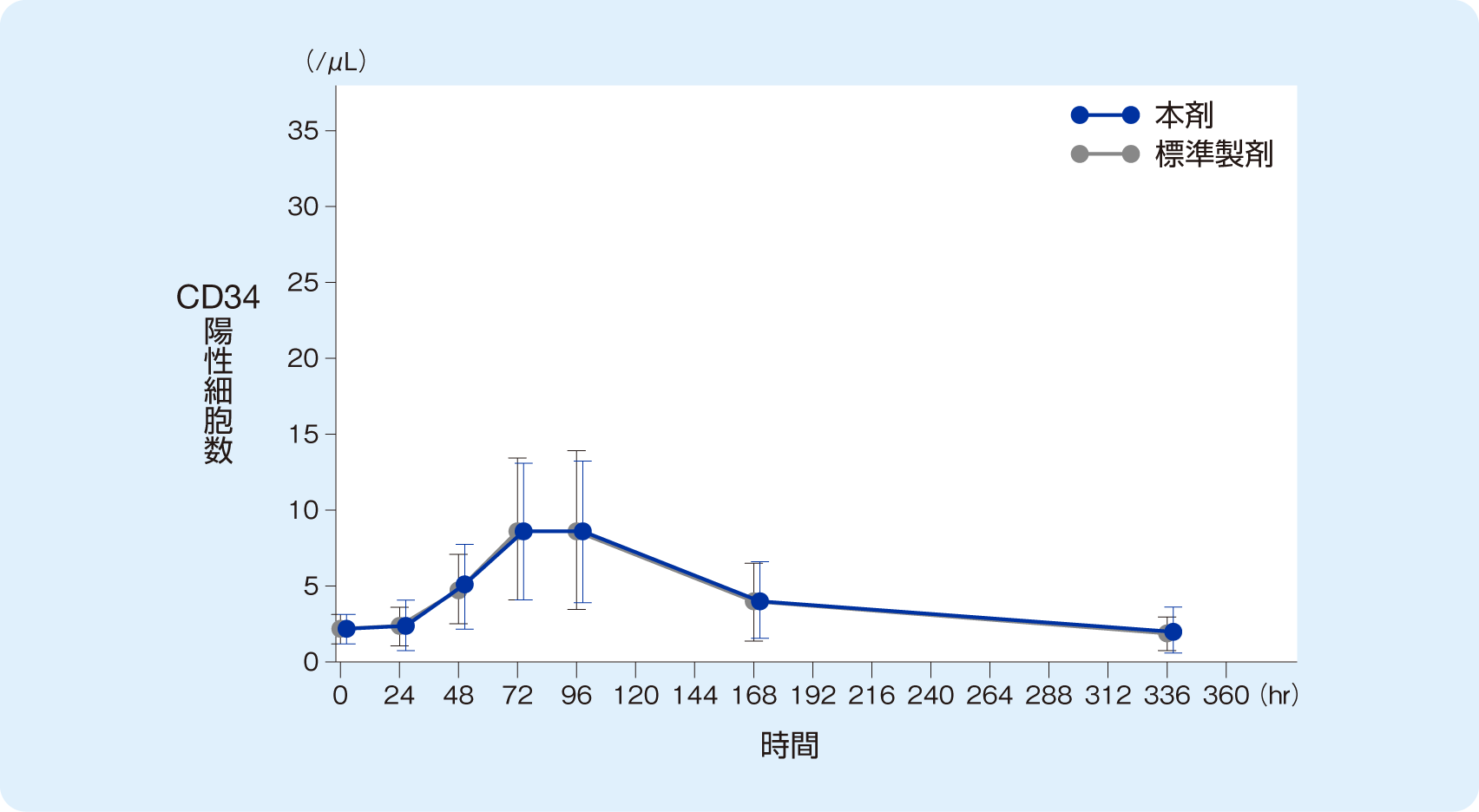
健康成人男性40例に、本剤またはグラン®(標準製剤)400μg/m2を絶食下で単回皮下投与し、非盲検2期クロスオーバー法により両製剤の薬力学的効果を比較した。
(1)薬力学的同等性
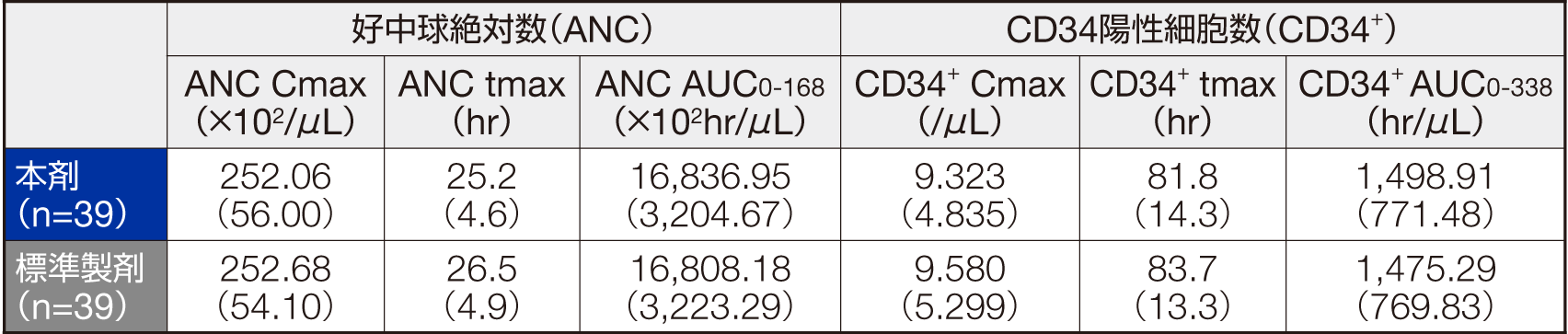
クロスオーバー2期全てを完了した39例で本剤と標準製剤の好中球絶対数(ANC)およびCD34陽性細胞数は下図のように推移した。ANC CmaxおよびCD34+ Cmaxにおける、製剤間の平均値(対数変換値)の差の95%信頼区間は共にlog(0.80)~ log(1.25)の範囲内であった。また、ANC tmaxおよびCD34+ tmaxにおいて、製剤間の中央値の差の95%信頼区間における対照薬(標準製剤)の中央値に対する比は共に-0.2 ~+0.2の範囲内であり、両製剤は薬力学的に同等/同質であると考えられた。
2.反復皮下投与試験2)
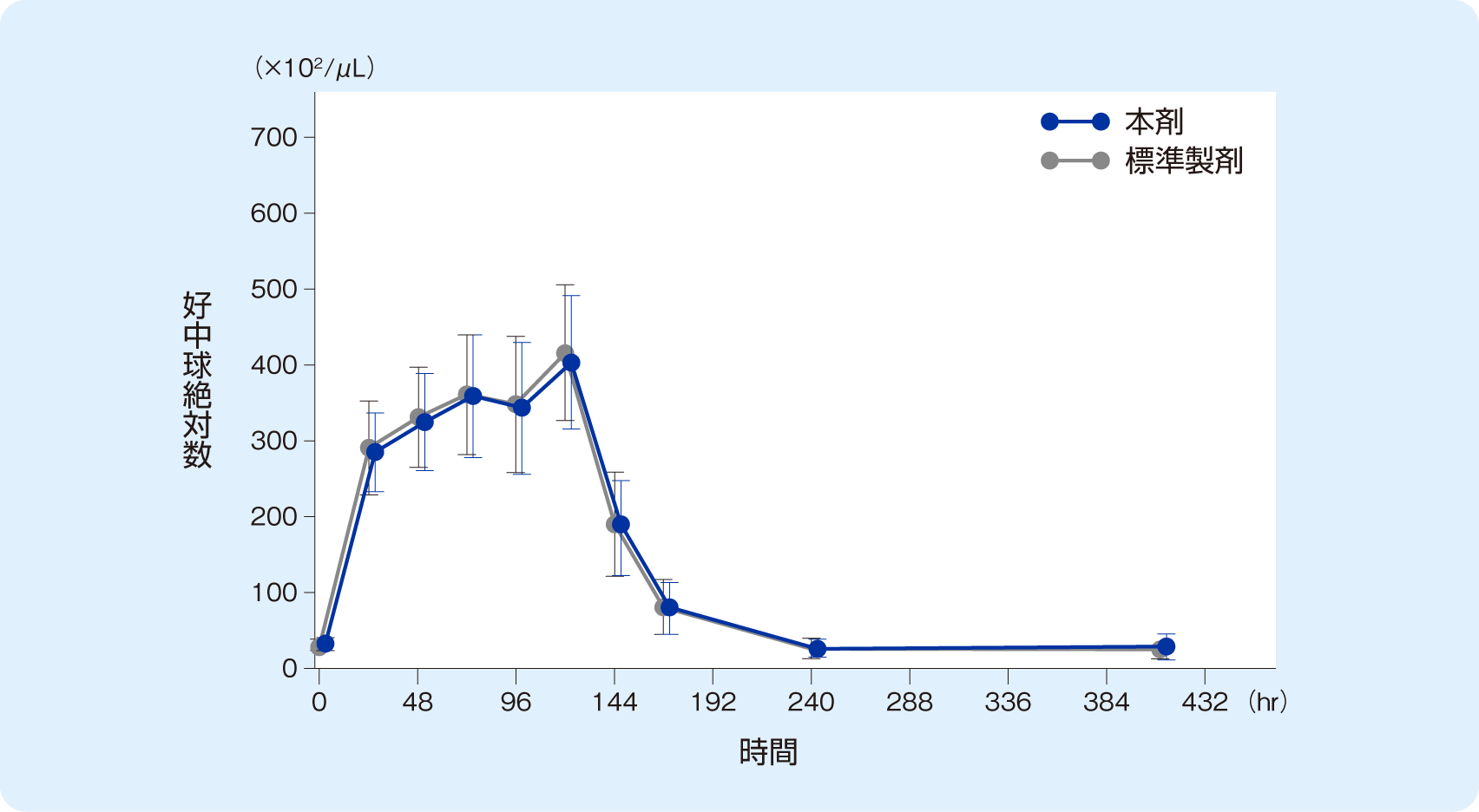
健康成人男性42例に、本剤または標準製剤400μg/m2を1日1回5日間反復皮下投与し、二重盲検2期クロスオーバー法により両製剤の薬力学的効果を比較した。
(1)薬力学的同等性
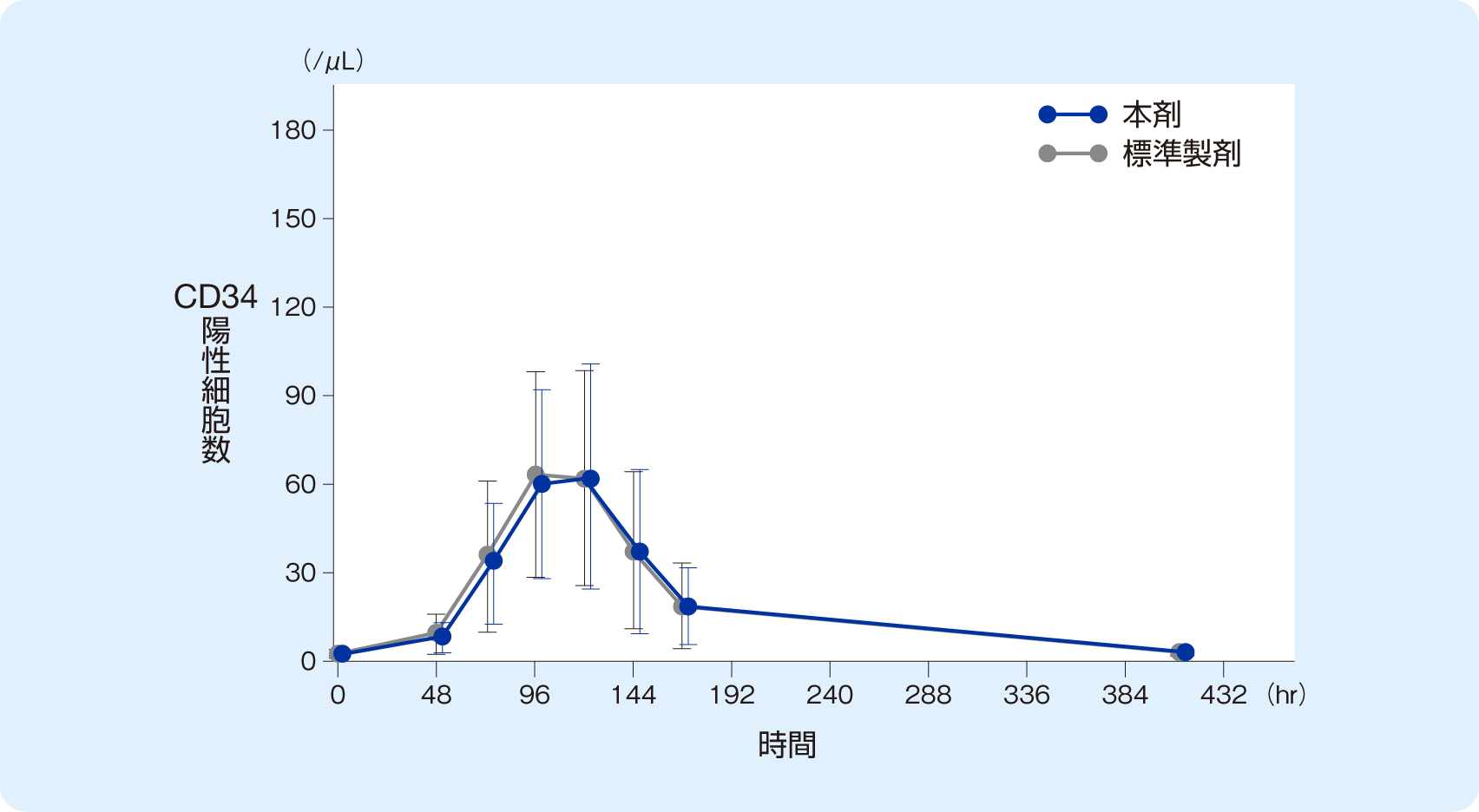
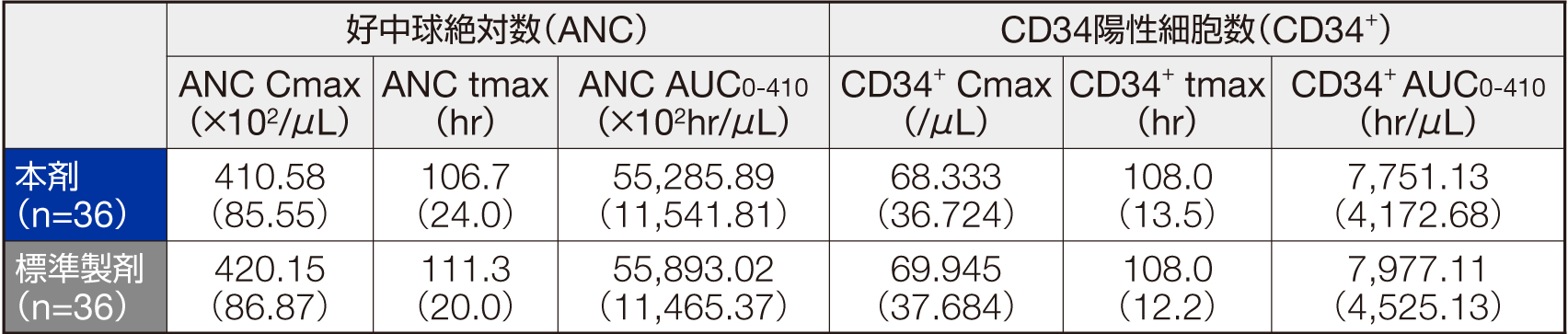
クロスオーバー2期全てを完了した36例で本剤と標準製剤の好中球絶対数(ANC)およびCD34陽性細胞数は下図のように推移した。ANC CmaxおよびCD34+ Cmaxにおける、製剤間の平均値(対数変換値)の差の95%信頼区間は共にlog(0.80)~ log(1.25)の範囲内であった。また、ANC tmaxおよびCD34+ tmax において、製剤間の中央値の差の95%信頼区間における対照薬(標準製剤)の中央値に対する比は共に-0.2 ~+0.2の範囲内で、両製剤は薬力学的に同等/同質であると考えられた。
3.単回点滴静注試験3)
健康成人男性24例に、本剤または標準製剤200μg/m2を30分かけて絶食下で単回点滴静注し、二重盲検2期クロスオーバー法により両製剤の薬力学的効果を比較した。
(1)薬力学的同等性
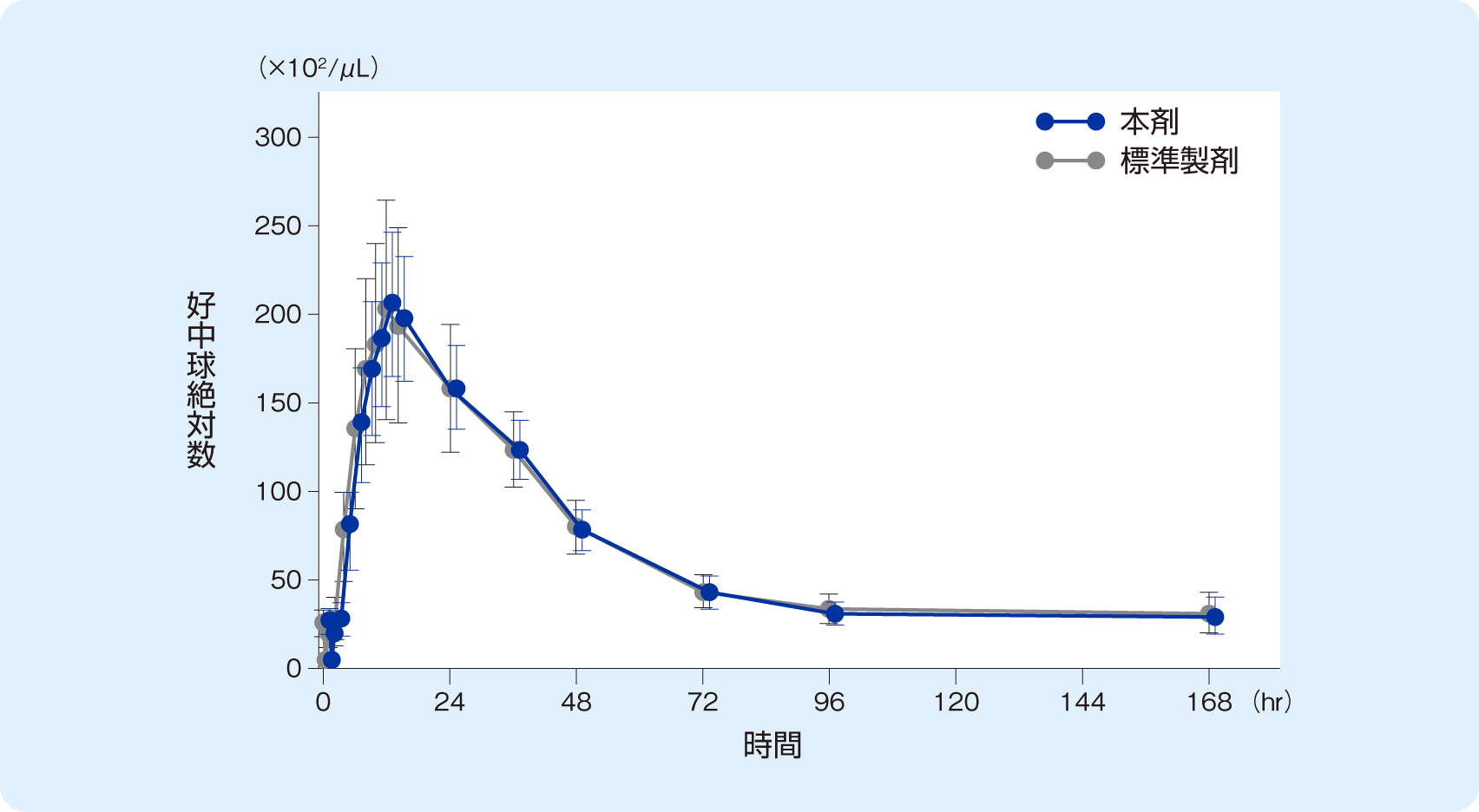
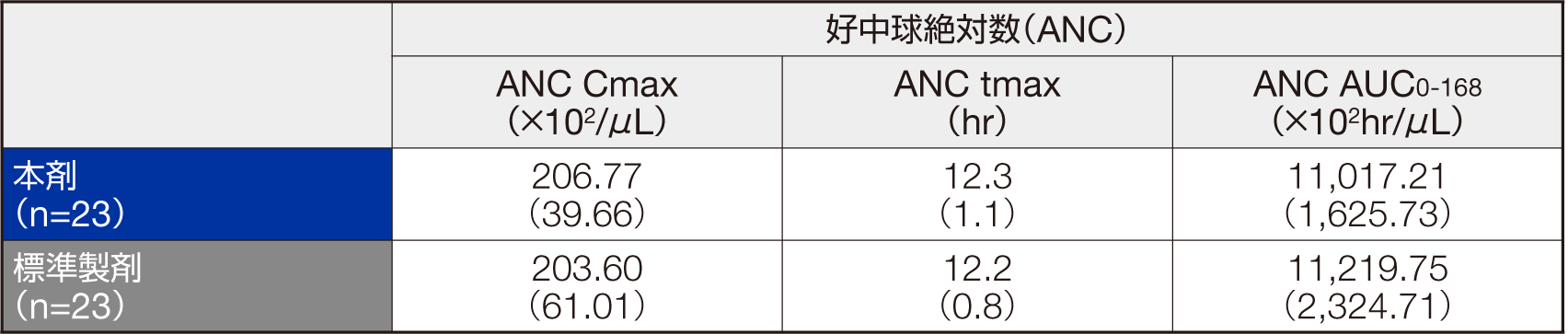
クロスオーバー2期全てを完了した23例で、本剤と標準製剤の好中球絶対数(ANC)は下図のように推移した。ANC Cmaxにおける製剤間の平均値(対数変換値)の差の95%信頼区間またはANC tmax における製剤間の中央値の差の95%信頼区間における対照薬(標準製剤)の中央値に対する比は、それぞれlog(0.80)~ log(1.25)または-0.2 ~+0.2の範囲内であったことから、両製剤は薬力学的に同等/同質であると考えられた。
「効能・効果」、「用法・用量」につきましては添付文書をご参照ください。
非臨床試験
好中球増加作用
(1)G-CSF 依存性細胞における増殖促進作用(in vitro)4)
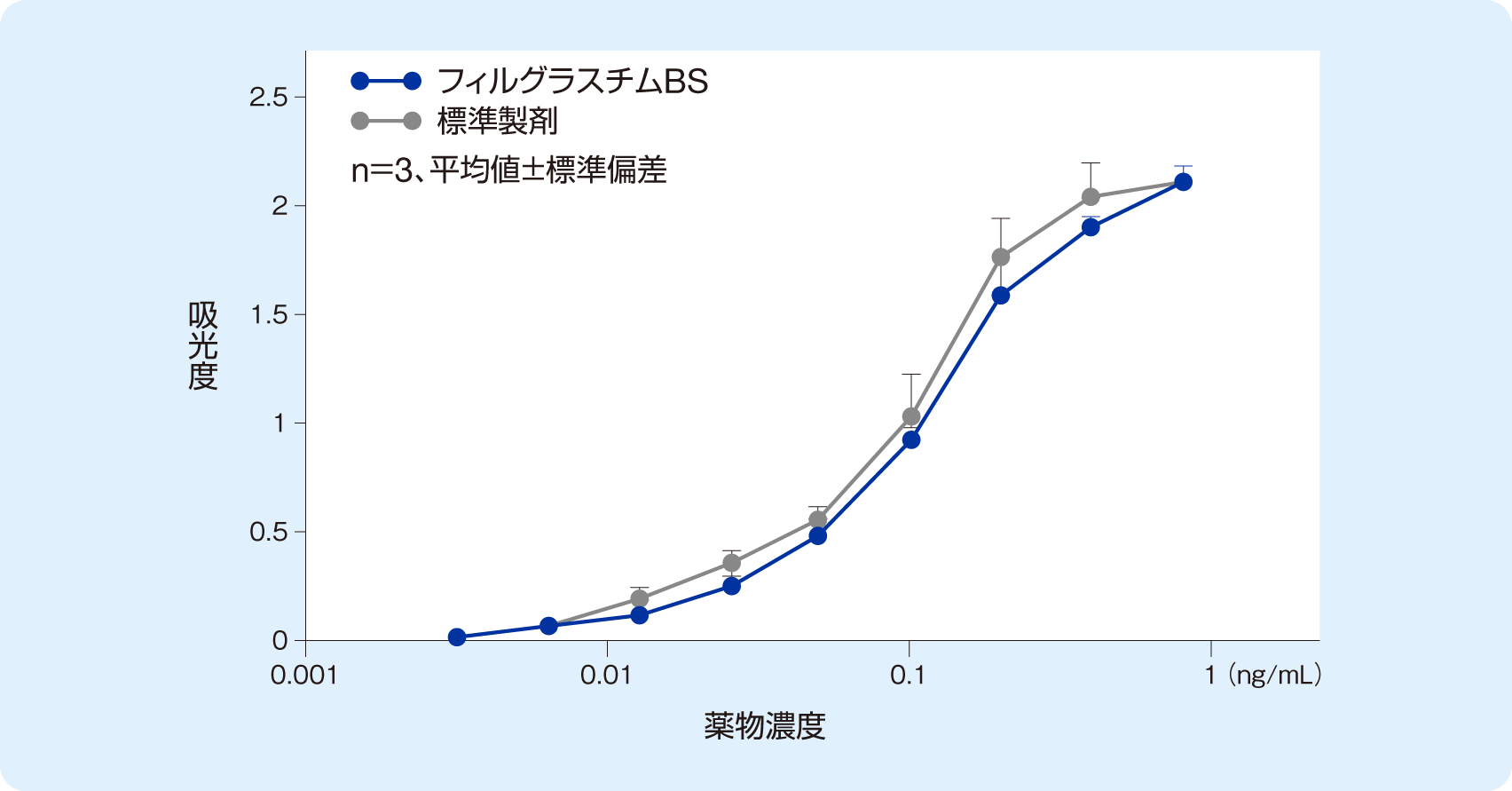
フィルグラスチムバイオ後続品の原薬(以下フィルグラスチムBSとする)は、G-CSF依存性増殖を示す細胞に対して細胞増殖促進活性を示し、その50%有効濃度は0.107ng/mLであり、グラン®(標準製剤)の50%有効濃度は0.087ng/mLであった。
フィルグラスチムBSおよび標準製剤のG-CSF依存性細胞における増殖促進作用
(2)正常ラットにおける末梢血好中球数に及ぼす影響(ラット)5)
フィルグラスチムBSは正常ラットへの単回静脈内投与あるいは単回皮下投与のいずれにおいても、末梢血好中球数を増加させた。その程度は溶媒投与群と比較してそれぞれ最大で約2.2倍および約3.1倍であり、標準製剤ではそれぞれ最大で約2.7倍および約3.9倍であった。なお、リンパ球数、単球数、好酸球数、好塩基球数、赤血球数および血小板数には明らかな変化は観察されなかった。
フィルグラスチムBSおよび標準製剤の末梢血好中球数に及ぼす影響(正常ラット)
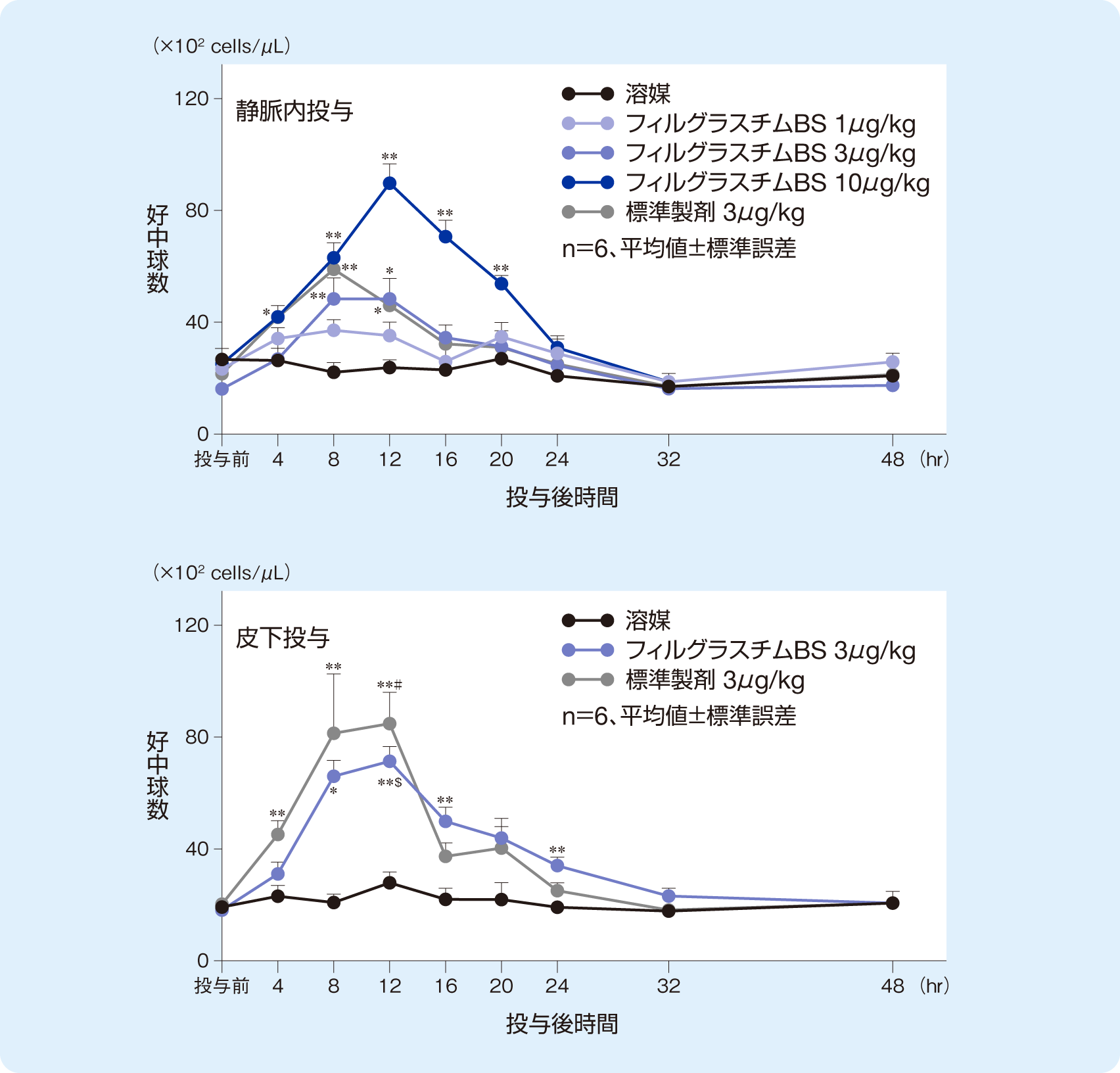
- *および**:溶媒投与群に対する統計学的有意差を示す(*:p<0.05、**:p<0.01、Dunnettの多重比較検定)。
- $:フィルグラスチムBS 3μg/kg静脈内投与群に対するフィルグラスチムBS 3μg/kg皮下投与群の統計学的有意差を示す($:p <0.05、Studentのt検定)。
- #:標準製剤 3μg/kg静脈内投与群に対する標準製剤 3μg/kg皮下投与群の統計学的有意差を示す(#:p <0.05、Aspin-Welchのt検定)。
- <試験方法> Crl:CD(SD)雄性ラット(1群6例)に溶媒、フィルグラスチムBSあるいは標準製剤を単回静脈内または単回皮下投与し、末梢血球数(白血球、好中球、リンパ球、単球、好酸球、好塩基球、赤血球および血小板)を測定した。
- 1)持田製薬販売社内資料(臨床薬理試験―単回皮下投与比較試験―)
- 2)持田製薬販売社内資料(臨床薬理試験―反復皮下投与比較試験―)
- 3)持田製薬販売社内資料(臨床薬理試験―単回点滴静注比較試験―)
- 4)持田製薬販売社内資料(薬理試験―顆粒球コロニー形成刺激因子(G-CSF)依存性細胞における増殖促進作用の検討―)
- 5)持田製薬販売社内資料(薬理試験―正常ラットにおける末梢血好中球数に対する作用の検討―)