- 医療関係者向けホーム
- 医療関連情報
- よりぬき産婦人科トピックス
- 子宮内膜症・子宮腺筋症への薬物療法による不正出血の診断~EP剤とP剤による不正出血の病理学的機序について~(Vol.9 No.3 臨床最前線)
2021年11月4日公開(2022年10月25日変更)
子宮内膜症・子宮腺筋症への
薬物療法による不正出血の診断
~EP剤とP剤による不正出血の病理学的機序について~
太田 郁子先生
太田郁子ウィメンズクリニック 院長
本コンテンツは、OG SCOPE Vol.9 No.3 臨床最前線(2019年2月発行)の記事を一部再編集しております。
はじめに
今回は診断後のホルモン療法施行時の不正出血について、子宮内膜という観点から述べたい。子宮内膜症・子宮腺筋症には、子宮内膜腺細胞・子宮内膜間質細胞のみならず、基底層・子宮平滑筋内層の成分が関与している。したがって、正所のホルモン療法時の作用点とその作用の病理学的理解が病変への作用の理解の一助となると考えられる。
子宮内膜へのEP(estrogen/ progestin)剤および P(progestin)剤の作用機序
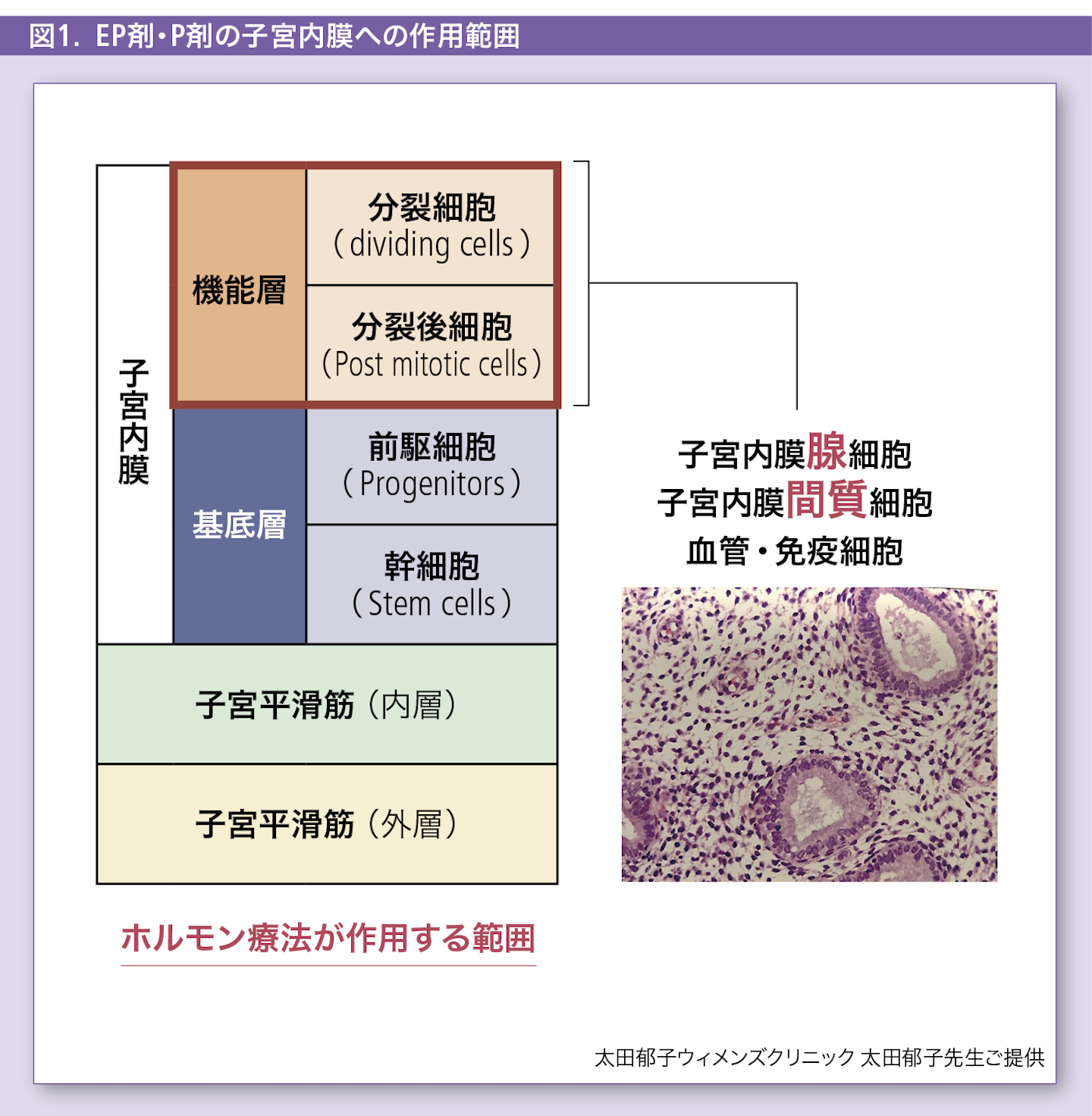
COCs(combined oral contraceptives)/ LEP剤(low dose estrogen progestins)はEP剤、ジエノゲストやMPA(メドロキシプロゲステロン酢酸エステル)はP剤として本症やその症状に使用されるが※、両剤はともにプロゲステロンの効果を供与する目的で投与される。したがって、子宮内膜への作用は主にプロゲスチンによる作用といってよい。EP剤のエストロゲンの役割は、当初P剤で、避妊を目的として開発された際に不正出血を抑制する目的のため、エストロゲンが付加された。また、エストロゲン付加によりネガティブフィードバックによるFSHの低下を励起し、卵胞発育を抑制し、より避妊効果が確実となった。子宮内膜へのこれらのホルモン剤の作用範囲は図1に示す。
※COCsの適応症は避妊、LEP剤の適応症は月経困難症(一部のLEP剤は子宮内膜症に伴う疼痛の改善の適応症を持つ)、ジエノゲスト1 mgの適応症は子宮内膜症及び子宮腺筋症に伴う疼痛の改善、ジエノゲスト0.5mgの適応症は月経困難症、MPAの適応症は無月経、月経周期異常(稀発月経、多発月経)、月経量異常(過少月経、過多月経)、機能性子宮出血、黄体機能不全による不妊症、切迫流早産、習慣性流早産。2021年7月の承認状況に応じて加筆修正しています。
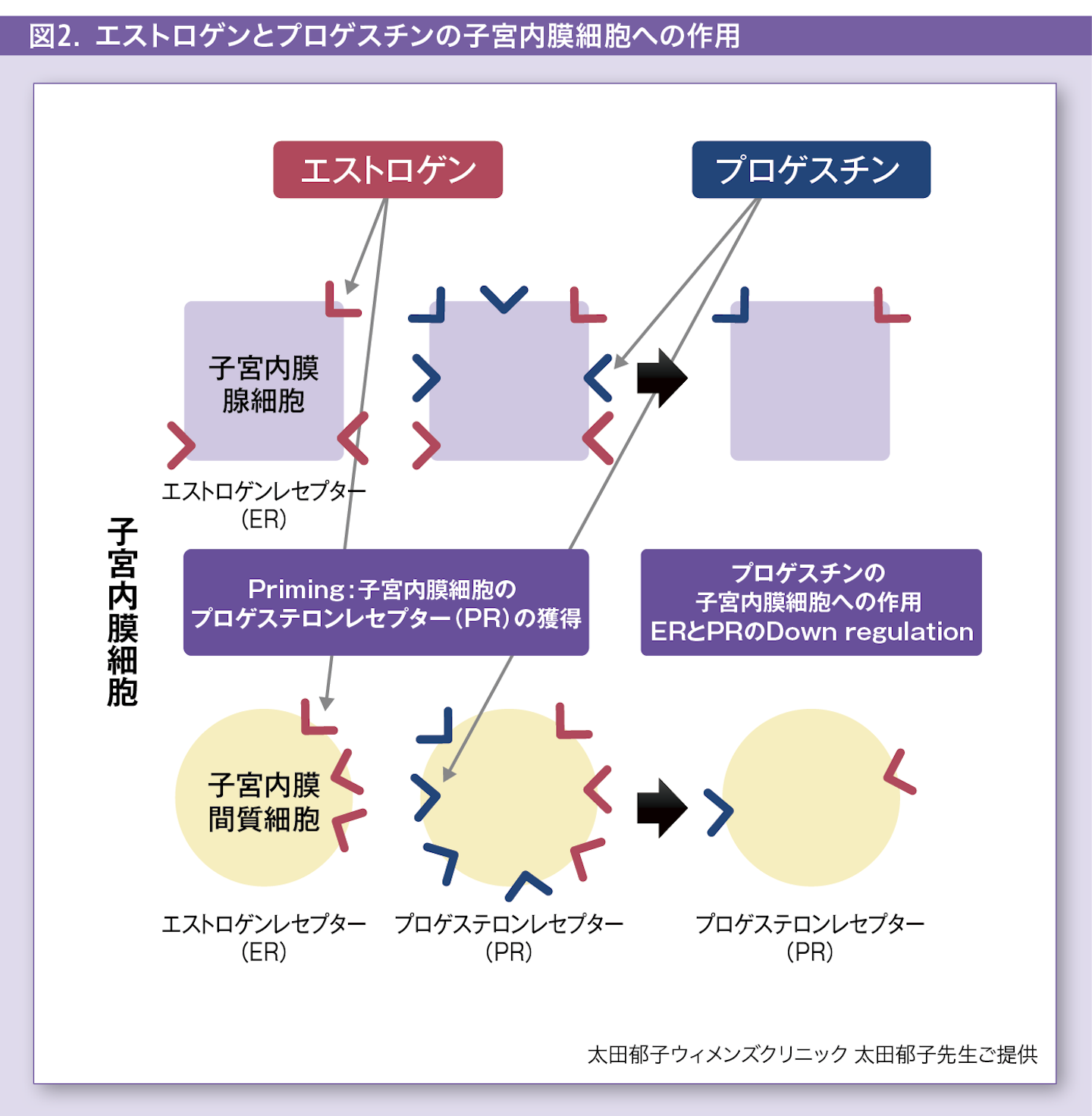
子宮内膜機能層へのエストロゲン・プロゲステロンの作用
子宮内膜機能層は子宮内膜腺細胞と子宮内膜間質細胞、血管細胞などから成る。腺細胞は分泌期に複雑な腺構造を構築し、妊娠に備えた弾力性のあるスポンジのような着床層を構成する。一方、間質細胞はその複雑化した腺管を支える緩衝支持組織となる。腺細胞および間質細胞は増殖期初期にエストロゲンによるpriming(プロゲステロンレセプターを増やす働き)を受け、プロゲステロンレセプター(PR)を獲得する。プロゲステロンの作用は腺・間質細胞のエストロゲンレセプター(ER)、PRのDown regulationであり、プロゲステロンの暴露が長期に持続すると、両細胞はERとPRの発現が大幅に低下する(図2)。これをsecretory exhaustionと呼び、長期のプロゲスチン暴露により最終的に形成されるエストロゲン・プロゲステロンにほとんど感度を持たない萎縮性子宮内膜を‘pill’ endometriumと称す。EP剤およびP剤の目的はこの‘pill’ endometriumを速やかに形成し、ホルモンの変動に伴う出血および病変の増殖を抑制することに他ならない。また機能層のみへの作用のため、基底層には正常な内膜を構成する幹細胞が保持され、可逆的変化と考えてよい。
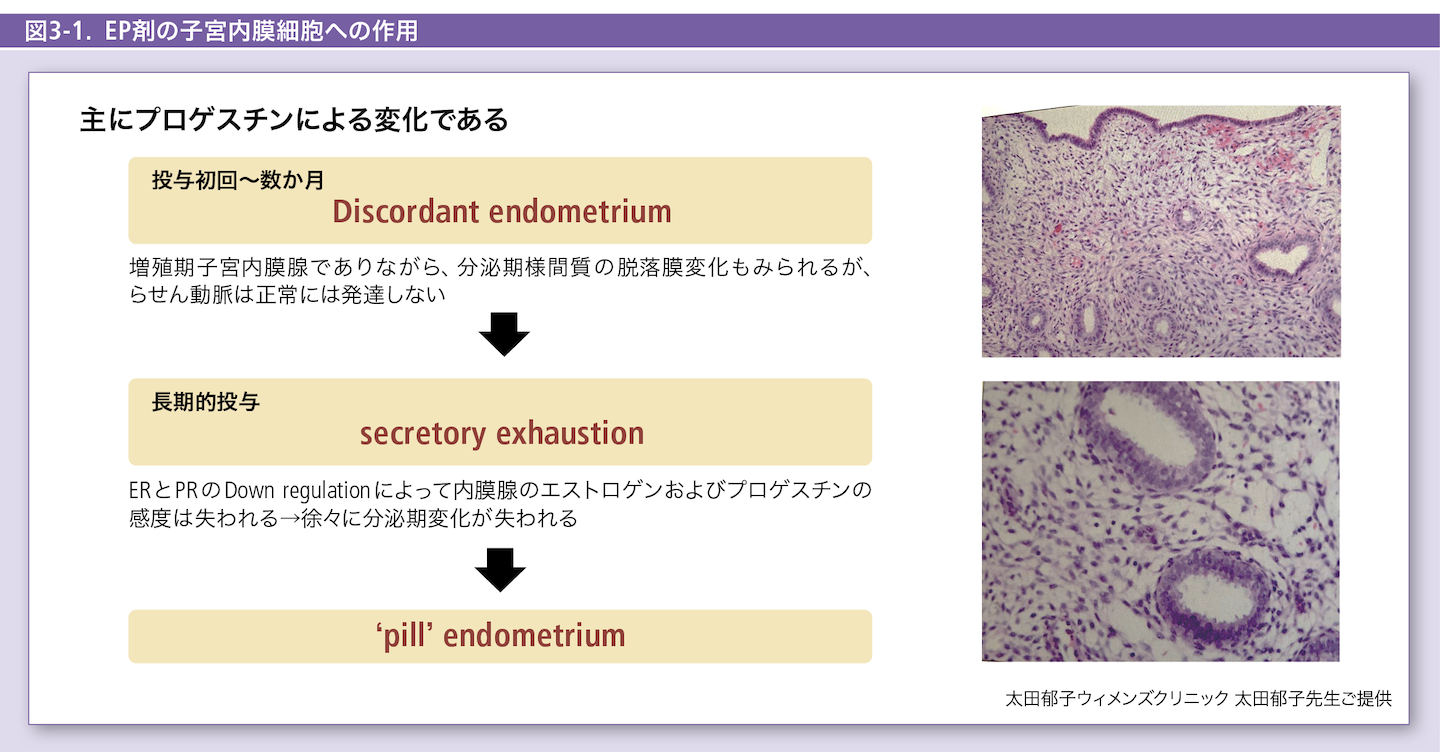
EP剤およびP剤使用時の子宮内膜の変化
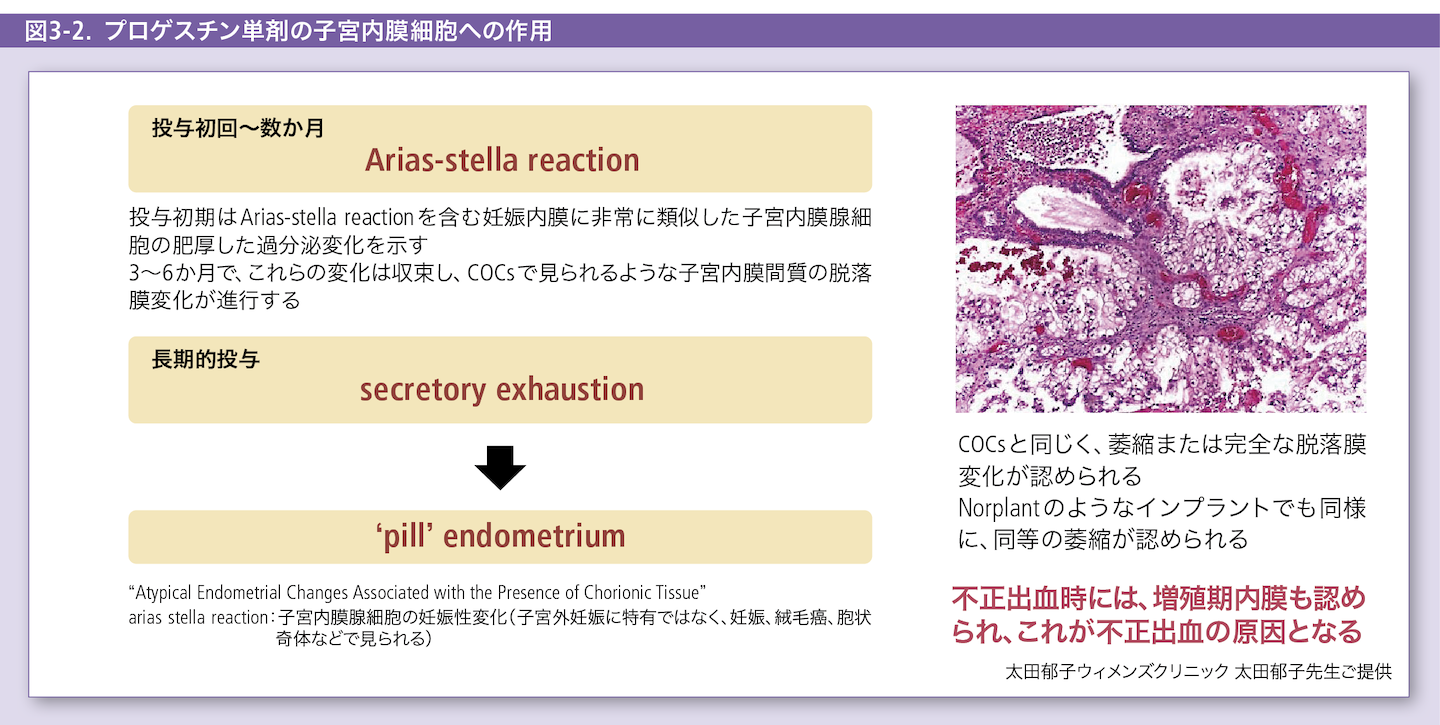
EP剤およびP剤は最終的には同じ‘pill’ endometriumに到達するが、その期間と過程が異なる。EP剤の場合、高濃度の外因性エストロゲンに常に晒され、さらに内膜の刷新は28日周期で起きるため、secretory exhaustionは緩徐に進行する。投与数か月から1年以内はDiscordant endometrium(増殖期変化と分泌期変化が混合している状態)が認められるが、休薬による内膜の刷新によって不正出血の頻度は少なく、徐々に‘pill’ endometriumに到達する。一方、P剤においては、初回投与から数か月はArias-stella reactionが認められる。Arias-stella reactionは異所性妊娠に特異的な反応ではなく、妊娠など高濃度の黄体ホルモンに長期間暴露されたときに起こる子宮内膜腺細胞の変化である。さらにFSHを抑制する外因性エストロゲンの付加がないため、卵胞の発育が起こり、エストロゲンは内因性で変動し、さらに内膜の刷新が起きないため、secretory exhaustionは急速に進行する。したがって、EP剤における病態の安定(‘pill’ endometriumへの到達)は約1~2年を要し、P剤においては3~4か月を要すると報告されている。
ʻpillʼ endometriumとは?
‘pill’ endometriumは病理学的には閉経後萎縮子宮内膜像と同様である(図3-1~図3-3)。しかし、最も大きく異なるのは前者ではERとPRがほとんど発現していないが、後者では逆にERとPRのUp regulationが認められる点である。‘pill’ endometriumの特徴は、らせん動静脈が未発達で血管壁が衝撃に脆弱なだけではなく、間質細胞が大幅に減少しており、また分泌期変化(脱落膜変化)が失われているため、緩衝支持機構が弱い構造であることである。したがって、何らかの原因で出血が生じた場合、その出血は速やかな止血を得られない。また完全にホルモンへの応答感度が失われているわけではなく、基底層から成熟した細胞が補充される際に一部増殖性変化が認められることがあり、これが不正出血の原因となると報告されている。
EP剤とP剤の特徴
最後に前述を踏まえて、各剤の特徴を示す(表1)。EP 剤においては十分なエストロゲンが外因性に補充されるために、P剤のアンドロゲン作用は問題にならないが、P 剤単独で投与する場合はP剤のアンドロゲン作用により、卵胞の形成が抑制されると内因性エストロゲンの産生量が低下し、骨量減少・更年期症状の発現といった症状を呈する可能性がある。したがって、P 剤単独で使用する際は、卵胞形成の有無を経過観察することはもちろん、アンドロゲン作用の低い製剤を使用することが望ましい。
おわりに
本稿では子宮内膜のEP剤、P剤の変化を述べたが、これは子宮内膜症・子宮腺筋症病変部においても起こる変化である。子宮内膜をよく観察し、病変の変化を推察することも経過観察上重要なことであると思われる。またホルモン剤は子宮内膜機能層のみに作用することから、子宮内膜基底層類似細胞も有する子宮内膜症・子宮腺筋症病変に対しては、ホルモン療法は可逆的・一時的変化であり、中断とともに再燃することも念頭に置く必要があると思われる。
参考文献
- Mutter GL,.Pathology of the Female Reproductive Tract 3rd Edition,2014:p310-325