- 医療関係者向けホーム
- 循環器領域
- ユリス®錠
- Pick Up
- 痛風関節炎の診断・治療とユリス®錠の血清尿酸値低下作用
 Pick Up
Pick Up
2020年07月30日公開(2026年04月21日一部改訂)
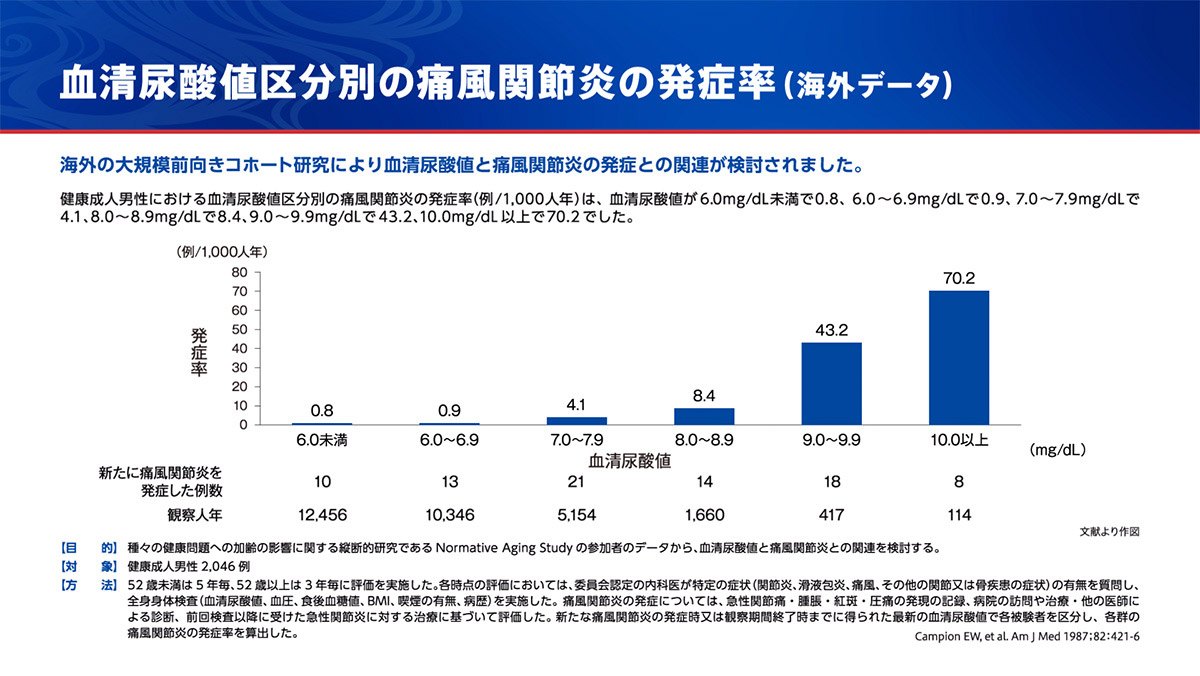
高尿酸血症が長年持続すると痛風関節炎や痛風結節、腎障害、尿路結石など尿酸一ナトリウム結晶が関与する臨床症状が顕性化してきます。このなかで痛風関節炎や痛風結節をきたしたものが痛風です1)。
2020年5月に発売されたユリス®錠は、痛風、高尿酸血症の治療選択肢の1つとなる選択的尿酸再吸収阻害薬
(Selective Urate Reabsorption Inhibitor:SURI)です。
今回は、血清尿酸値と痛風関節炎の関連、ガイドラインに基づいた痛風の診断と高尿酸血症の治療、及び後期第Ⅱ相試験データが示すユリス®錠の血清尿酸値低下作用についてご紹介いたします。
- 1)日本痛風・尿酸核酸学会ガイドライン改訂委員会 高尿酸血症・痛風の治療ガイドライン 第3版 診断と治療社 2018 : 115
血清尿酸値と痛風関節炎の関連-海外の大規模前向きコホート研究より-
痛風の診断-高尿酸血症・痛風の治療ガイドライン 第3版より-
第 3 章 高尿酸血症・痛風の診療マニュアル
B 診断 3 痛風
要 点
- 痛風関節炎は関節内や関節周囲組織に沈着した尿酸一ナトリウム結晶により誘発される関節炎ないし滑液包炎である。
- 尿酸一ナトリウム結晶は補正偏光顕微鏡下に強い負の複屈折性を示す針状結晶で、関節液中の白血球に貪食された尿酸一ナトリウム結晶の検出が確定診断となる。
- 化膿性関節炎との鑑別や感染合併を否定するためには関節液採取と顕微鏡検査が必要である。
- 痛風発作中の血清尿酸値は低いことがあり血清尿酸値の診断的価値は高くない。
- 非侵襲的画像診断では関節エコー、dual energy CTでの結晶沈着の可視化が有用である。
- 日本痛風・尿酸核酸学会ガイドライン改訂委員会 高尿酸血症・痛風の治療ガイドライン 第3版 診断と治療社 2018:99-101
参 考尿酸一ナトリウム結晶の画像所見
顕微鏡像(補正偏光顕微鏡下)
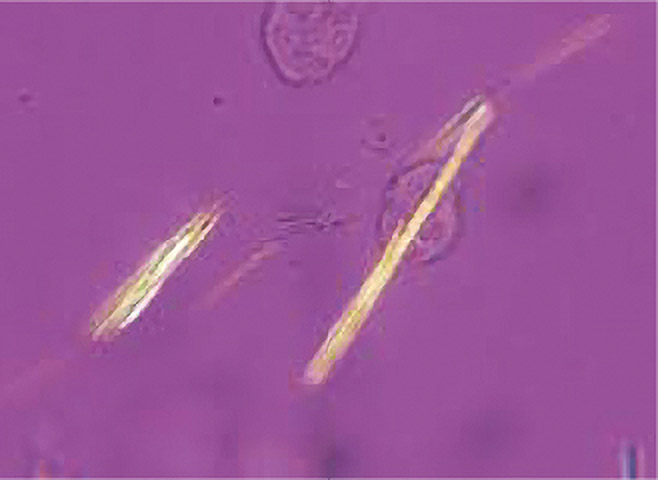
尿酸一ナトリウム結晶が、針状の負の複屈折性結晶として観察される。
関節エコー画像
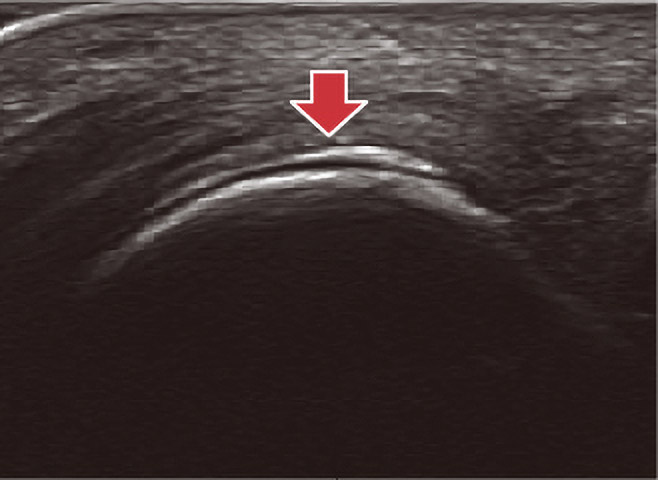
関節滑膜に層状に沈着した尿酸塩結晶は、関節軟骨の低エコー域を挟んで高ないし等エコーレベルの不整な線状エコー画像(double contour sign:DCS)として描出される。
- 画像:大山 博司 先生(両国東口クリニック 理事長)ご提供
高尿酸血症の治療-高尿酸血症・痛風の治療ガイドライン 第3版より-
第 3 章 高尿酸血症・痛風の診療マニュアル
C 治療 3 高尿酸血症
要 点
- 高尿酸血症の治療では、心血管病など生命予後に関係する肥満、高血圧、糖・脂質代謝異常などとともに、高尿酸血症の発症に関連する生活習慣を改善することが最も大切である。
- 痛風関節炎を繰り返す患者や痛風結節を認める患者は薬物治療の適応となり、血清尿酸値を6.0mg/dL以下に維持するのが望ましい。
- 痛風関節炎を誘発させないために、尿酸降下薬は最小量から開始すべきで、必要に応じてコルヒチンカバーを併用する。
- 無症候性高尿酸血症への薬物治療の導入は血清尿酸値8.0mg/dL以上を一応の目安にするが、適応は慎重にすべきで、現時点で得られているエビデンスや薬物の副作用について情報を患者に示し納得のうえで開始することが望ましい 。
- 日本痛風・尿酸核酸学会ガイドライン改訂委員会 高尿酸血症・痛風の治療ガイドライン 第3版 診断と治療社 2018:114-7
監修コメント
両国東口クリニック 理事長大山 博司先生
痛風関節炎は関節内に析出した尿酸塩結晶が引き起こす急性関節炎であり、その確定診断のためには、顕微鏡下で関節液中の白血球に貪食された尿酸一ナトリウム結晶を検出することがgolden standardとされています。
近年では、関節超音波検査(Bモード画像)が痛風関節炎の診断において低侵襲・低コストで簡便性に優れるなどの利点を有するとされています。特に関節軟骨の表面の関節滑膜に層状に沈着した尿酸塩結晶は、「double contour sign:DCS」と呼ばれる特徴的な所見を呈するため、他の疾患との鑑別に有用です。
また、痛風関節炎を繰り返す患者などの治療においては、血清尿酸値を長期にわたって6.0mg/dL以下に維持することが望ましいため、患者一人ひとりにとって適した薬剤を選び、適切に血清尿酸値をコントロールする必要があります。関節超音波検査による関節内尿酸塩結晶沈着の可視化は、治療介入が必要な患者への説明や、治療継続の指導の際のツールとしても有用とされ、今後の臨床現場における普及が期待されています。
今回ご紹介した内容が、先生方の痛風診療の一助になりましたら幸いです。
「禁忌を含む注意事項等情報」等は電子添文をご参照ください。
ユリス®錠の血清尿酸値低下作用
後期第Ⅱ相試験(用量反応検証試験)
後期第Ⅱ相試験は一部承認外の用法及び用量による成績が含まれますが、用量反応検証試験として実施されたため掲載します。
- 社内資料:用量反応検証試験・後期第Ⅱ相臨床試験[2020年1月23日承認、CTD 2.7.6.14、CSR FYU-981-006(資料5.3.5.1-2)]〔承認時評価資料〕
- Hosoya T, et al. Clin Exp Nephrol 2020 ; 24 : S53-61
- [利益相反] 本研究は株式会社富士薬品の資金により行われた。本論文の著者のうち4名は株式会社富士薬品の社員である。
- 著者には、本研究に関する株式会社富士薬品のアドバイザーでありコンサルタント料等を受領している者が含まれる。
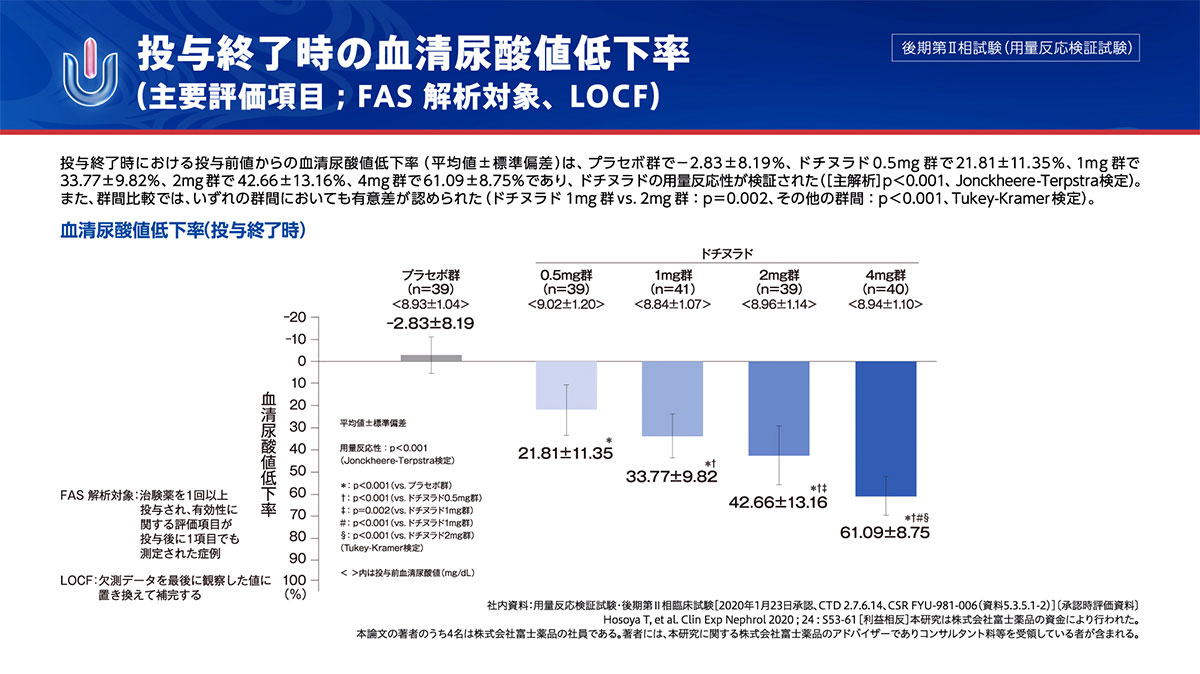
投与終了時の血清尿酸値低下率(主要評価項目;FAS解析対象、LOCF)
ドチヌラド0.5mg群~4mg群において、用量反応性が検証されました。
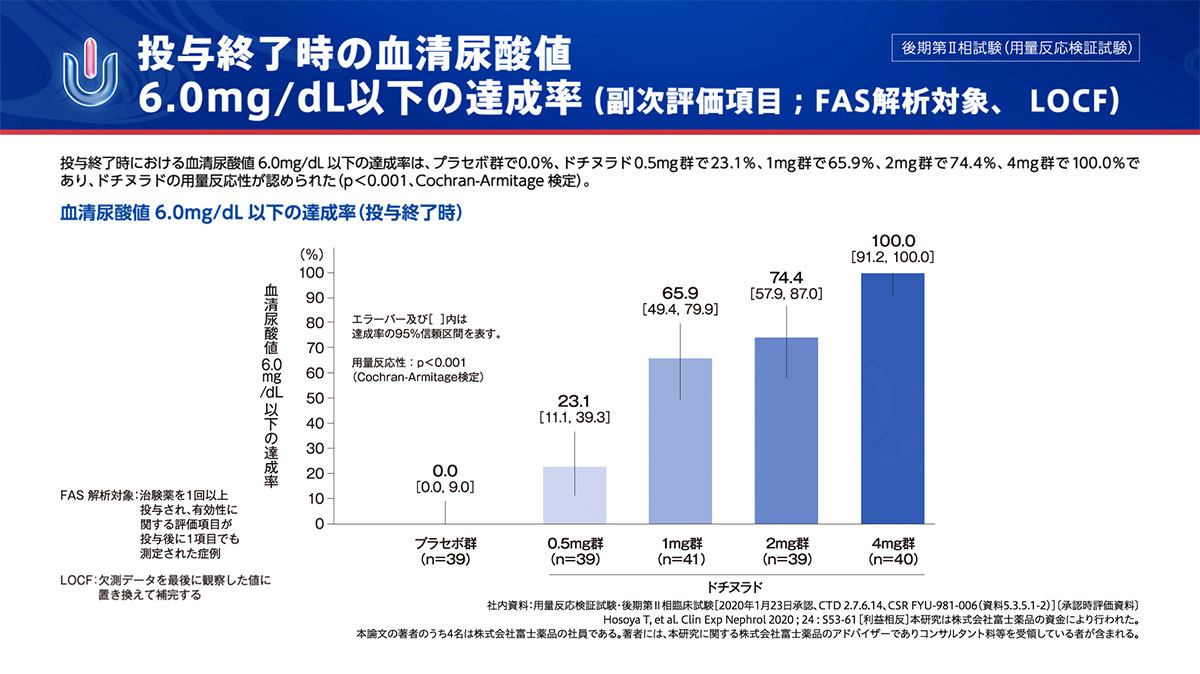
投与終了時の血清尿酸値6.0mg/dL以下の達成率
(副次評価項目;FAS解析対象、LOCF)
ドチヌラド0.5mg群~4mg群において、用量反応性が認められました。
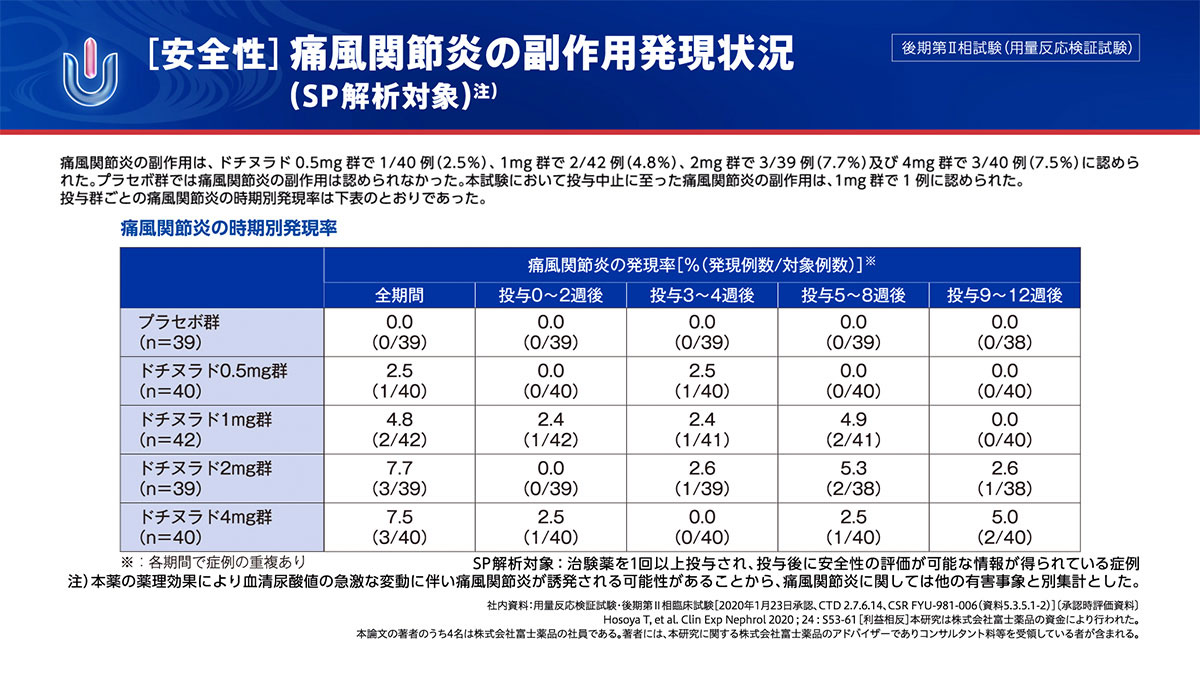
安全性(SP解析対象)
副作用は、プラセボ群で15.4%、ドチヌラド0.5mg群で15.0%、1mg群で19.0%、2mg群で17.9%、4mg群で17.5%に認められました。
副作用は、プラセボ群で6/39例(15.4%)、ドチヌラド0.5mg群で6/40例(15.0%)、1mg群で8/42例(19.0%)、2mg群で7/39例(17.9%)、4mg群で7/40例(17.5%)に認められました。
2例以上に発現した副作用は、プラセボ群で尿中β2ミクログロブリン増加が2/39例(5.1%)、ドチヌラド1mg群でβ‒NアセチルDグルコサミニダーゼ増加が3/42例(7.1%)、痛風関節炎が2/42例(4.8%)、2mg群で痛風関節炎が3/39例(7.7%)、尿中β2ミクログロブリン増加、β‒NアセチルDグルコサミニダーゼ増加、白血球数増加がそれぞれ2/39例(5.1%)、4mg群で痛風関節炎が3/40例(7.5%)、尿中β2ミクログロブリン増加、β‒NアセチルDグルコサミニダーゼ増加、α1ミクログロブリン増加がそれぞれ2/40例(5.0%)に認められました。ドチヌラド0.5mg群でみられた副作用は、痛風関節炎、四肢不快感、γ‒グルタミルトランスフェラーゼ増加等でいずれも1/40例(2.5%)に認められました。
本試験において、死亡例を含む重篤な副作用は認められませんでした。また本試験において投与中止に至った副作用は、プラセボ群で尿中β2ミクログロブリン増加が、1mg群で痛風関節炎がそれぞれ1例に認められました。
6. 用法及び用量
通常、成人にはドチヌラドとして1日0.5mgより開始し、1日1回経口投与する。その後は血中尿酸値を確認しながら必要に応じて徐々に増量する。維持量は通常1日1回2mgで、患者の状態に応じて適宜増減するが、最大投与量は1日1回4mgとする。
2026年3月作成
15790-2/N6 52 GT
コンテンツ評価にご協力をお願いいたします。
このコンテンツは参考になりましたでしょうか?
ご回答ありがとうございます。
マイページ設定により、先生のご興味のある領域/製品の最新情報を
効率的にチェックすることができます!
今後のコンテンツ改善のために、
「参考にならなかった」理由を
教えてください。
(複数回答可)

引き続き、持田製薬 医療関係者向けサイトを
よろしくお願いいたします。

![痛風関節炎の診断・治療とユリス®錠の血清尿酸値低下作用 [監修]両国東口クリニック 理事長 大山 博司 先生](/newtemp/domain/img/newmajor/urece/pick/cs/04/pic_kv_hd01.jpg)
![痛風関節炎の診断・治療とユリス®錠の血清尿酸値低下作用 [監修]両国東口クリニック 理事長 大山 博司 先生](/newtemp/domain/img/newmajor/urece/pick/cs/04/pic_kv_hd01_sp.jpg)