- 医療関係者向けホーム
- 循環器領域
- ユリス®錠
- Clinical Study:後期第Ⅱ相試験(用量反応検証試験) 試験の概要
 Clinical Study後期第Ⅱ相試験(用量反応検証試験)
Clinical Study後期第Ⅱ相試験(用量反応検証試験)
後期第Ⅱ相試験は一部承認外の用法及び用量による成績が含まれますが、用量反応検証試験として実施されたため掲載します。
試験の概要「後期第Ⅱ相試験(用量反応検証試験)」
- 社内資料:用量反応検証試験・後期第Ⅱ相臨床試験[2020年1月23日承認、CTD 2.7.6.14、CSR FYU-981-006(資料5.3.5.1-2)]
〔承認時評価資料〕 - Hosoya T, et al. Clin Exp Nephrol 2020 ; 24 : S53-61
[利益相反]本研究は株式会社富士薬品の資金により行われた。本論文の著者のうち4名は株式会社富士薬品の社員である。
著者には、本研究に関する株式会社富士薬品のアドバイザーでありコンサルタント料等を受領している者が含まれる。
- 「禁忌を含む注意事項等情報」等は電子添文をご参照ください。
試験デザイン
多施設共同、二重盲検、ランダム化、プラセボ対照、用量漸増並行群間比較試験
目的
痛風を含む高尿酸血症患者を対象として、ドチヌラドの用量反応性の検証及び安全性の検討を行う。
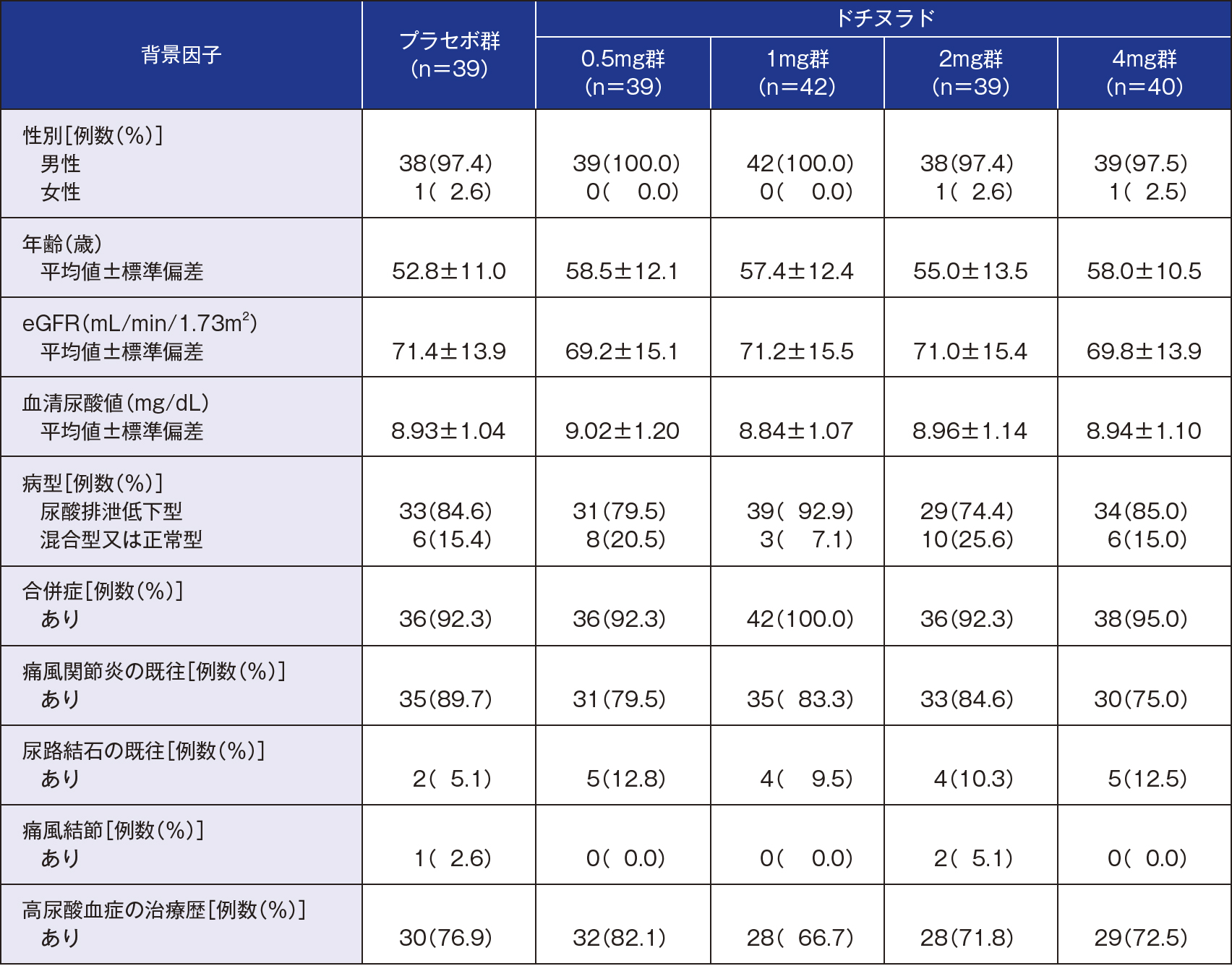
対象
20歳以上の痛風を含む高尿酸血症患者※1(割付症例数:201、投与症例数:200)
[血清尿酸値:痛風患者7.0mg/dL以上、高尿酸血症患者(合併症※2あり)8.0mg/dL以上、高尿酸血症患者(合併症※2なし)9.0mg/dL以上]
- ※1「尿酸産生過剰型」あるいは「判定不能」を除く
※2 高血圧、糖尿病、メタボリックシンドローム
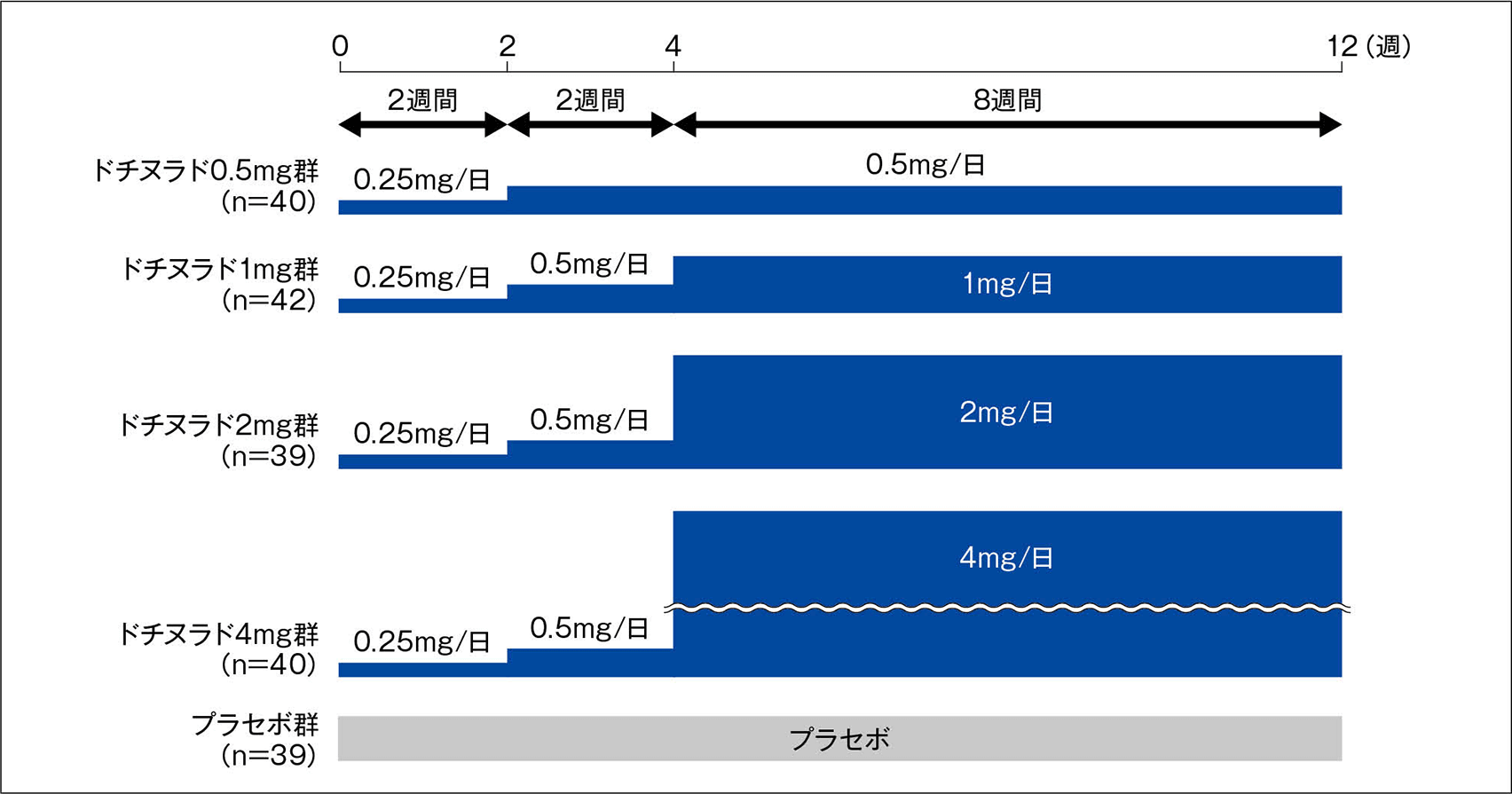
投与方法
対象患者をドチヌラド4用量群(0.5mg群、1mg群、2mg群、4mg群)又はプラセボ群の計5群にランダムに割り付け、治験薬を1日1回朝食後に経口投与した。ドチヌラド4用量群は0.25mg/日を投与開始から2週後まで2週間投与した後、0.5mg/日に増量して3週目から4週後まで2週間投与し、さらに0.5mg/日、1mg/日、2mg/日、4mg/日のいずれかに維持又は増量して5週目から12週後まで8週間投与した。
評価項目
有効性に関する評価項目
【主要評価項目】
投与終了時(投与12週後又は投与中止時)における投与前値からの血清尿酸値低下率
[(投与前値-投与終了時の値)/投与前値×100]
【副次評価項目】
- 各時点(投与2、4、8、12週後)における投与前値からの血清尿酸値低下率
- 各時点(投与前、投与2、4、8、12週後)及び投与終了時における血清尿酸値
- 投与終了時における血清尿酸値6.0mg/dL以下の達成率[血清尿酸値が6.0mg/dL以下の例数/有効性評価対象例数×100]
など
安全性に関する評価項目
- 有害事象
- 副作用
- 痛風関節炎
など
解析計画
主要評価項目について、投与終了時の血清尿酸値低下率は、Jonckheere-Terpstra検定を用いた用量反応性の検証(主解析)及びTukey-Kramer検定を用いた群間比較を行った。副次評価項目について、血清尿酸値低下率(各時点)は、投与8週後及び12週後におけるJonckheere-Terpstra検定を用いた用量反応性の検討及びTukey-Kramer検定を用いた群間比較を行った。血清尿酸値(各時点及び投与終了時)は、対応のあるt検定を用いて投与群ごとに投与前後の比較を行った。血清尿酸値6.0mg/dL以下の達成率は、投与終了時におけるCochran-Armitage検定を用いた用量反応性の検討を行った。
6. 用法及び用量
通常、成人にはドチヌラドとして1日0.5mgより開始し、1日1回経口投与する。その後は血中尿酸値を確認しながら必要に応じて徐々に増量する。維持量は通常1日1回2mgで、患者の状態に応じて適宜増減するが、最大投与量は1日1回4mgとする。