- 医療関係者向けホーム
- 循環器領域
- トラムセット®
- Clinical Study:非がん性慢性疼痛(変形性膝関節症及び腰痛症に対する臨床効果) 鎮痛効果不十分となるまでの期間
 Clinical Study非がん性慢性疼痛(変形性膝関節症及び腰痛症に対する臨床効果)
Clinical Study非がん性慢性疼痛(変形性膝関節症及び腰痛症に対する臨床効果)
鎮痛効果不十分となるまでの期間
主要評価項目(検証的解析結果)
鎮痛効果不十分となるまでの期間(二重盲検期)[サブグループ解析:対象疾患別]
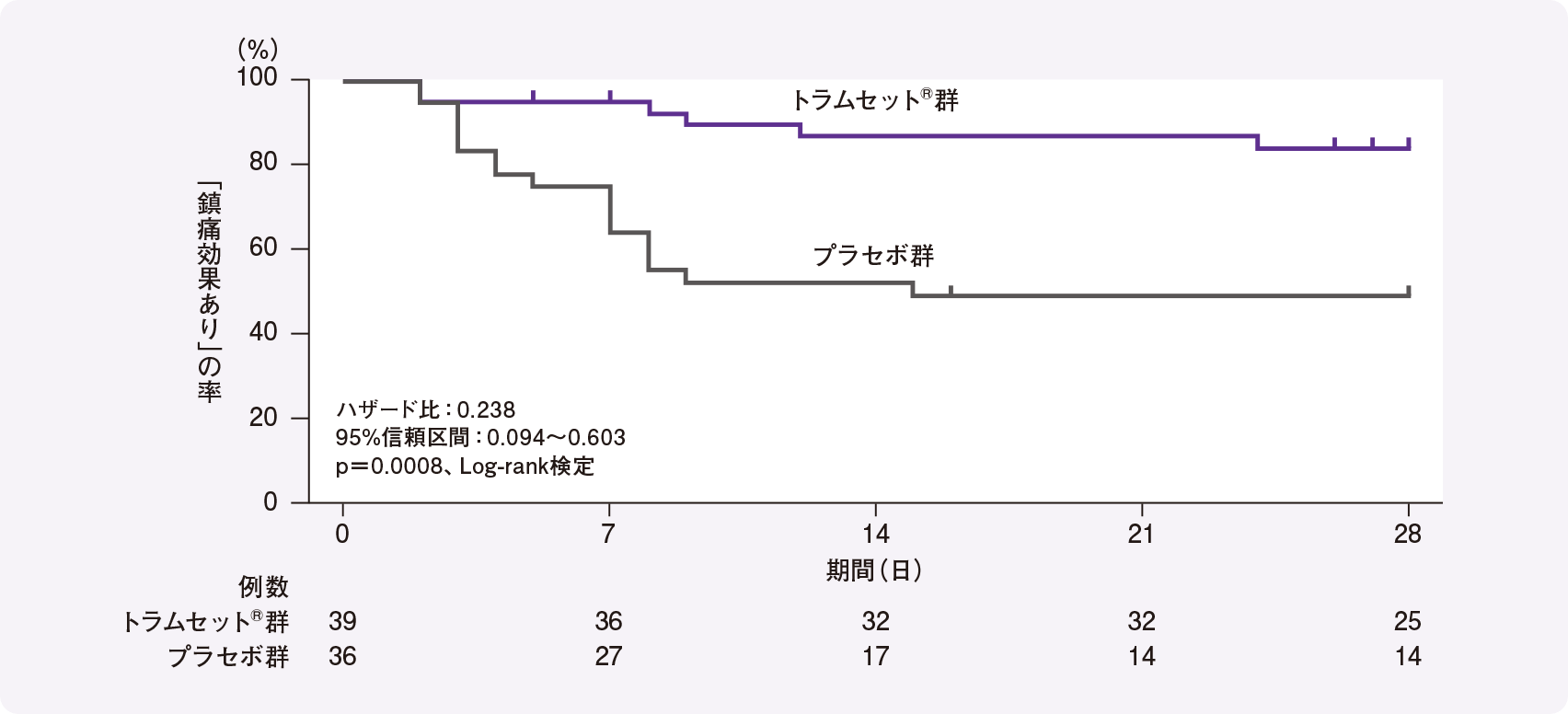
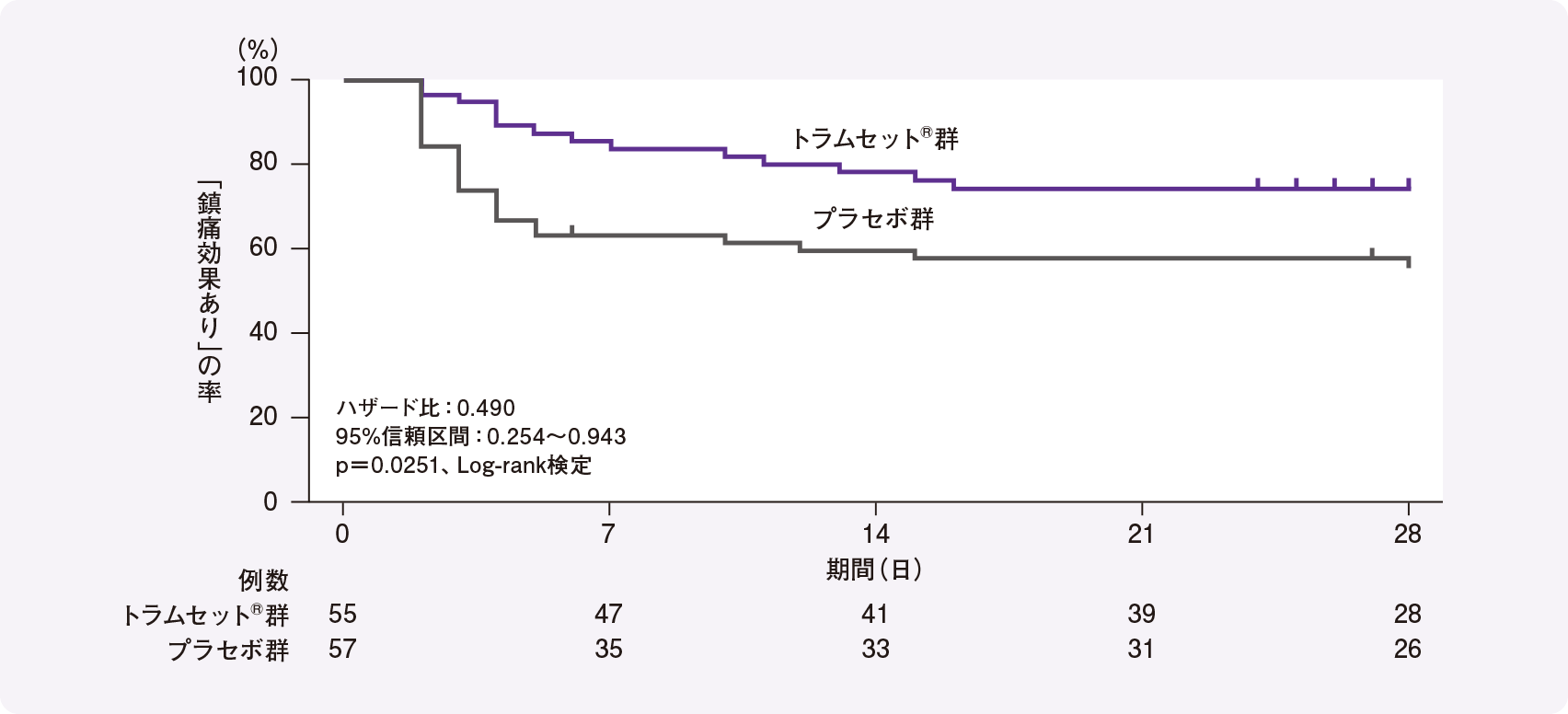
全体の二重盲検期開始時から鎮痛効果不十分※1となるまでの期間(検証的な解析項目)は、トラムセット®群がプラセボ群と比較して有意に長く、トラムセット®のプラセボに対する優越性が検証された[p=0.0001、層別Log-rank検定(層別因子:変形性膝関節症、腰痛症)]。また、二重盲検期に鎮痛効果が不十分となった患者の割合は、変形性膝関節症患者においてはトラムセット®群が15.4%(6/39例)、プラセボ群が50.0%(18/36例)、腰痛症患者においてはトラムセット®群が25.5%(14/55例)、プラセボ群が43.9%(25/57例)であった。
[サブグループ解析:対象疾患別]
層別因子である対象疾患別に解析した結果、いずれの疾患においてもトラムセット®群がプラセボ群と比較して有意に長かった(変形性膝関節症:名目上のp=0.0008、腰痛症:名目上のp=0.0251、Log-rank検定)。
-
※1:以下のいずれかの条件を満たした時点を「鎮痛効果不十分」とした。
- 1)二重盲検期において連続する2日間のVAS24値が、非盲検期終了前3日間のVAS24値の平均値と比較して15mmを超えて悪化
- 2)患者が効果不十分による投与中止を申し出た場合
トラムセット®配合錠の警告、重要な基本的注意
1. 警告(抜粋)
- 1.1 本剤により重篤な肝障害が発現するおそれがあることに注意し、アセトアミノフェンの1日総量が1500mg(本剤4錠)を超す高用量で長期投与する場合には、定期的に肝機能等を確認するなど、慎重に投与すること。[8.6参照]
8. 重要な基本的注意(抜粋)
- 8.7 鎮痛剤による治療は原因療法ではなく、対症療法であることに留意すること。