製品Q&Aご使用にあたり
本Q&Aは、医療従事者向けの内容で、医療従事者が患者に対して行う診断、指導、助言等に代替するものではありません。また、掲載している情報は、医療従事者が製品の適正な使用を行うための一般的情報または参考情報であり、全ての症例またはケースに適応するものではありません。従いまして、本Q&Aのご利用によって生じた結果については、責任を負いかねますのでご了承ください。
本Q&Aには、承認外の内容(用法・用量、適応、剤形等)が含まれている場合がありますので、ご注意ください。製品のご使用に当たっては、最新の電子添文をご確認くださいますようお願いいたします。
なお、本Q&Aを許可なく複写、複製、転掲、頒布、改変等を行うことはご遠慮ください。
用法・用量
-
リアルダを食後に経口投与する理由は?食事の影響はありますか?
リアルダの国内臨床試験が食後経口投与にて実施されたためです。
健康成人にリアルダ(メサラジンとして2,400mg、4,800mg)を単回経口投与したときの血漿中未変化体及び代謝物(アセチル体)の濃度推移、尿中排泄率及び吸収率に、食事による著しい影響は認められませんでした1)。電子添文抜粋
6. 用法及び用量
通常、成人にはメサラジンとして1日1回2,400mgを食後経口投与する。活動期は、通常、成人にはメサラジンとして1日1回4,800mgを食後経口投与するが、患者の状態により適宜減量する。
通常、体重23kg超の小児にはメサラジンとして1日1回40mg/kgを食後経口投与するが、2,400mgを上限とする。活動期は、通常、体重23kg超の小児にはメサラジンとして1日1回80mg/kgを食後経口投与するが、4,800mgを上限とし、患者の状態により適宜減量する。16. 薬物動態
16.2 吸収
16.2.3 食事の影響
健康成人に本剤を単回経口投与(メサラジンとして2,400mg、4,800mg)したときの血漿中未変化体及びアセチル体の濃度推移、尿中排泄率及び吸収率に、食事による著しい影響は認められなかった。【参考資料】
1) インタビューフォーム Ⅶ. 薬物動態に関する項目 1. 血中濃度の推移 (4)食事・併用薬の影響 1)食事の影響2026年2月作成
-
リアルダを1日2回に分けて投与してもよいですか?
1日2回に分けての投与は承認された用法ではなく、適正使用の観点からお勧めしません。
リアルダは1日1回投与で有効成分であるメサラジンを標的部位である大腸に送達し、大腸全域に持続的に放出することが可能な放出制御製剤です。電子添文抜粋
6. 用法及び用量
通常、成人にはメサラジンとして1日1回2,400mgを食後経口投与する。活動期は、通常、成人にはメサラジンとして1日1回4,800mgを食後経口投与するが、患者の状態により適宜減量する。
通常、体重23kg超の小児にはメサラジンとして1日1回40mg/kgを食後経口投与するが、2,400mgを上限とする。活動期は、通常、体重23kg超の小児にはメサラジンとして1日1回80mg/kgを食後経口投与するが、4,800mgを上限とし、患者の状態により適宜減量する。2026年2月作成
-
リアルダの投与開始8週目以降も、活動期の潰瘍性大腸炎の用量で投与を継続してよいですか?
活動期の用量でリアルダを投与開始してから8週間を目安に有効性を評価し、継続の必要性があると判断された場合には、活動期の用量のまま8週目以降も投与継続することは可能です。評価をせず漫然と継続することは避けてください。
活動期の潰瘍性大腸炎患者を対象とした国内臨床試験では、投与期間が8週間を超えた場合の有効性・安全性を検討していないため、漫然と投与を継続しないよう電子添文(7. 用法及び用量に関連する注意)にて注意喚起しています。
なお、8週を超える投与が保険診療上認められるかについては、審査支払機関の判断になります。電子添文抜粋
7. 用法及び用量に関連する注意
7.1 活動期の用量を投与する場合は、投与開始8週間を目安に有効性を評価し、漫然と継続しないこと。
2026年2月作成
-
リアルダはメサラジンの注腸剤や坐剤と併用できますか?
メサラジンの注腸剤や坐剤との併用は可能です。
ただし、メサラジン注腸剤又は坐剤と併用する場合には、メサラジンとしての総投与量が増加することを考慮し、特に肝又は腎機能の低下している患者や高齢者等へ投与する際は、適宜減量するなど十分に注意してください。併用時に異常が認められた場合には、減量又は中止するなどの適切な処置を行ってください。
なお、保険診療上、併用が認められるかについては、審査支払機関の判断になります。電子添文抜粋
7. 用法及び用量に関連する注意
7.2 本剤をメサラジン注腸剤又は坐剤と併用する場合には、メサラジンとしての総投与量が増加することを考慮し、特に肝又は腎機能の低下している患者並びに高齢者等への投与に際しては適宜減量するなど、十分に注意すること。併用時に異常が認められた場合には、減量又は中止するなどの適切な処置を行うこと。[9.2.2、9.3.2、9.8 参照]
2026年2月作成
-
リアルダは1200mgと600mgの錠剤がありますが、小児、成人ともにどちらの錠剤でも使用可能ですか?
リアルダの1200mg錠、600mg錠ともに、小児から成人まで、潰瘍性大腸炎の活動期・寛解期を問わず使用可能です。
ただし、1200mg錠から600mg錠への切替え、もしくは600mg錠から1200mg錠への切替えを行う場合は、患者の状態を慎重に観察するようにしてください。本剤は標的部位である大腸で有効成分を放出するよう設計された製剤であることから、薬物動態を指標とする生物学的同等性の評価が難しく、1200mg錠と600mg錠の生物学的同等性試験は実施されていません1)。
なお、1200mg錠及び600mg錠の切替え前後の有効性及び安全性を確認するため、成人の寛解期の潰瘍性大腸炎患者を対象に、1200mg錠から600mg錠への切替え試験(1200mg錠1日1回2錠を8週間投与した後、600mg錠1日1回4錠を8週間投与した非盲検非対照試験)2)を実施しています。その結果、1200mg錠及び600mgの有効性は同等であり、有害事象の発現状況に特筆すべき違いは認められませんでした。電子添文抜粋
7. 用法及び用量に関連する注意
7.4 使用製剤(本剤1200mg錠及び600mg錠)を切替える場合は、患者の状態を慎重に観察すること。[17.1.3 参照]
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.3 国内第Ⅲ相臨床試験(寛解期の潰瘍性大腸炎患者)
寛解期の潰瘍性大腸炎患者を対象として、本剤1200mg錠注1)1日1回2錠(メサラジンとして2,400mg)を8週間投与した後、本剤600mg錠注1)1日1回4錠(メサラジンとして2,400mg)を8週間投与した非盲検非対照試験を実施した。その結果、本剤1200mg錠投与時及び本剤600mg錠投与時いずれにおいても血便の非発現率注2)は100%(23/23例)であり、薬剤切替え前後で血便の非発現率に変化はなかった。
副作用発現頻度は、本剤1200mg錠投与時には0%(0/23例)、本剤600mg錠投与時には4.3%(1/23例、血尿のみ)であった。[7.4 参照]注1)600mg錠と1200mg錠の生物学的同等性を評価する試験は実施されていない。
注2)本剤1200mg錠又は本剤600mg錠が投与された期間に評価された全ての時点でのUC-DAIスコアの血便スコアが0の症例を血便の非発現と定義し、血便の非発現となった症例数の割合として算出した。
【参考資料】
1) 審査報告書(2025年06月24日) 7. 臨床的有効性及び臨床的安全性に関する資料並びに機構における審査の概略 7.R 機構における審査の概略 7.R.1 有効性について 7.R.1.3 本剤1,200mg錠から600mg錠への切替えについて
2) インタビューフォーム Ⅴ. 治療に関する項目 5. 臨床成績 <小児患者>(4)検証的試験 1)有効性検証試験 <参考:承認の根拠となった有効性の成績>③寛解期の潰瘍性大腸炎患者に対する国内第Ⅲ相臨床試験(承認時評価資料、MD090111U21試験)2026年2月作成
-
リアルダを小児に使用する場合、年齢による処方制限はありますか?
年齢による処方制限はありません。
リアルダ錠600mg、1200mgともに、本剤の内服が可能であり、体重23kg超の小児であれば処方可能です。
本剤は有効成分であるメサラジンを標的部位である大腸に送達し、大腸全域に持続的に放出する放出制御製剤であるため、錠剤を分割・粉砕するなどして投与することはできません。ご注意ください。
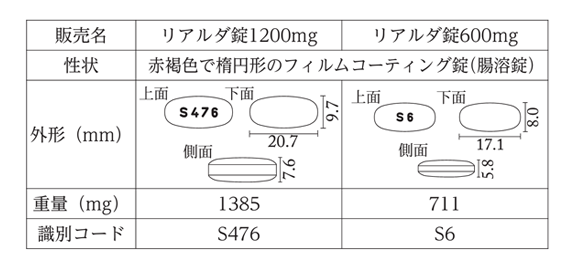
リアルダ錠600mgの大きさは、長径17.1mm×短径8.0mm×厚さ5.8mm、リアルダ錠1200mgの大きさは、長径20.7mm×短径9.7mm×厚さ7.6mmです。電子添文抜粋
3. 組成・性状
3.2 製剤の性状
6. 用法及び用量
通常、成人にはメサラジンとして1日1回2,400mgを食後経口投与する。活動期は、通常、成人にはメサラジンとして1日1回4,800mgを食後経口投与するが、患者の状態により適宜減量する。
通常、体重23kg超の小児にはメサラジンとして1日1回40mg/kgを食後経口投与するが、2,400mgを上限とする。活動期は、通常、体重23kg超の小児にはメサラジンとして1日1回80mg/kgを食後経口投与するが、4,800mgを上限とし、患者の状態により適宜減量する。7. 用法及び用量に関連する注意
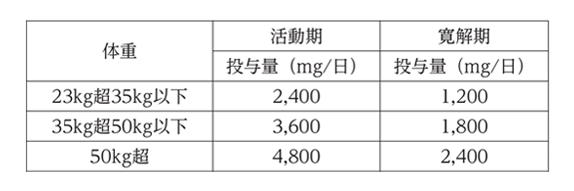
7.3 小児に対する1日投与量については、下表を目安とすること。[9.7、17.1.4、17.1.5 参照]
9. 特定の背景を有する患者に関する注意
9.7 小児等
体重18kg未満の小児等を対象とした臨床試験は実施していない。[7.3、17.1.4、17.1.5 参照]14. 適用上の注意
14.1 薬剤調製時の注意
14.1.2 乳鉢による粉砕は行わないこと。
14.3 薬剤投与時の注意
本剤は放出制御製剤であることより、かまずに服用すること。2026年2月作成
-
リアルダの小児への投与量は?
体重23kg超の小児には、通常、メサラジンとして1日1回40mg/kgを食後経口投与しますが、2,400mgを上限としてください。活動期は、通常、メサラジンとして1日1回80mg/kgを食後経口投与しますが、4,800mgを上限とし、患者の状態により適宜減量してください。
なお、リアルダ錠は600mgと1200mgの2規格のため、上記体重計算通りの量を投与できないケースがあります。そのため、下表を目安に投与量を決めてください。
電子添文抜粋
6. 用法及び用量
通常、成人にはメサラジンとして1日1回2,400mgを食後経口投与する。活動期は、通常、成人にはメサラジンとして1日1回4,800mgを食後経口投与するが、患者の状態により適宜減量する。
通常、体重23kg超の小児にはメサラジンとして1日1回40mg/kgを食後経口投与するが、2,400mgを上限とする。活動期は、通常、体重23kg超の小児にはメサラジンとして1日1回80mg/kgを食後経口投与するが、4,800mgを上限とし、患者の状態により適宜減量する。7. 用法及び用量に関連する注意
7.3 小児に対する1日投与量については、下表を目安とすること。[9.7、17.1.4、17.1.5 参照]

2026年2月作成
-
リアルダを飲み忘れた時はどうすればよいですか?
飲み忘れた場合は、忘れた分を気がついた時にできるだけ早く飲ませてください。ただし、次に通常服用する時間が近い場合は飲まずに、次の服用時間から1回分を飲ませてください。2回分を一度に飲まないようにさせてください。
2026年2月改訂
特殊患者
-
リアルダを腎機能が悪い方に投与できますか?
重篤な腎障害のある患者は、有効成分であるメサラジンの排泄が遅延し、腎障害がさらに悪化するおそれがあるため、禁忌です。
腎機能の低下している患者(重篤な腎障害のある患者を除く)への投与は可能ですが、メサラジンの排泄が遅延し、副作用があらわれるおそれがあるため注意が必要です。本剤投与により、間質性腎炎、ネフローゼ症候群、腎不全の報告があります。投与中は腎機能を検査するなど、患者の状態を十分に観察してください。また、メサラジンの注腸剤や坐剤と併用する場合には、メサラジンとしての総投与量が増加することを考慮し、適宜減量するなど十分に注意してください。
なお、国内の臨床試験では、中等度から重度の腎障害患者は除外されていました。電子添文抜粋
2. 禁忌(次の患者には投与しないこと)
2.3 重篤な腎障害のある患者[9.2.1 参照]
7. 用法及び用量に関連する注意
7.2 本剤をメサラジン注腸剤又は坐剤と併用する場合には、メサラジンとしての総投与量が増加することを考慮し、特に肝又は腎機能の低下している患者並びに高齢者等への投与に際しては適宜減量するなど、十分に注意すること。併用時に異常が認められた場合には、減量又は中止するなどの適切な処置を行うこと。[9.2.2、9.3.2、9.8 参照]
8. 重要な基本的注意
8.1 間質性腎炎、ネフローゼ症候群、腎不全が報告されているため、投与中は腎機能を検査するなど、患者の状態を十分に観察すること。[11.1.5 参照]
9. 特定の背景を有する患者に関する注意
9.2 腎機能障害患者
9.2.1 重篤な腎障害のある患者
投与しないこと。腎障害がさらに悪化するおそれがある。[2.3 参照]9.2.2 腎機能の低下している患者(重篤な腎障害のある患者を除く)
排泄が遅延し、副作用があらわれるおそれがある。中等度から重度の腎障害患者は臨床試験では除外されている。[7.2 参照]11. 副作用
11.1 重大な副作用
11.1.5 間質性腎炎、ネフローゼ症候群、腎不全(いずれも頻度不明)
[8.1 参照]2026年2月改訂
-
リアルダを肝機能が悪い方に投与できますか?
重篤な肝障害のある患者は、有効成分であるメサラジンの代謝が遅延し、肝障害がさらに悪化するおそれがあるため、禁忌です。
肝機能の低下している患者(重篤な肝障害のある患者を除く)への投与は可能ですが、メサラジンの代謝が遅延し、副作用があらわれるおそれがあるため注意が必要です。本剤投与により、肝機能障害、肝炎、黄疸の報告があります。投与中はAST、ALT等の肝機能をモニターするなど、患者の状態を十分に観察してください。また、メサラジンの注腸剤や坐剤と併用する場合には、メサラジンとしての総投与量が増加することを考慮し、適宜減量するなど十分に注意してください。
なお、国内の臨床試験では、中等度から重度の肝障害患者は除外されていました。電子添文抜粋
2. 禁忌(次の患者には投与しないこと)
2.4 重篤な肝障害のある患者[9.3.1 参照]
7. 用法及び用量に関連する注意
7.2 本剤をメサラジン注腸剤又は坐剤と併用する場合には、メサラジンとしての総投与量が増加することを考慮し、特に肝又は腎機能の低下している患者並びに高齢者等への投与に際しては適宜減量するなど、十分に注意すること。併用時に異常が認められた場合には、減量又は中止するなどの適切な処置を行うこと。[9.2.2、9.3.2、9.8 参照]
8. 重要な基本的注意
8.2 肝機能障害、肝炎、黄疸が報告されているため、投与中はAST、ALT等の肝機能をモニターするなど、患者の状態を十分に観察すること。[11.1.6 参照]
9. 特定の背景を有する患者に関する注意
9.3 肝機能障害患者
9.3.1 重篤な肝障害のある患者
投与しないこと。肝障害がさらに悪化するおそれがある。[2.4 参照]9.3.2 肝機能の低下している患者(重篤な肝障害のある患者を除く)
代謝が遅延し、副作用があらわれるおそれがある。中等度から重度の肝障害患者は臨床試験では除外されている。[7.2 参照]11. 副作用
11.1 重大な副作用
11.1.6 肝機能障害、肝炎、黄疸(いずれも頻度不明)
AST、ALT、γ-GTPの上昇等を伴う肝機能障害、肝炎、黄疸があらわれることがある。[8.2 参照]2026年2月改訂
-
リアルダを妊婦に投与できますか?
妊婦に対する臨床試験は実施しておらず、安全性が確立していないことから、妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ服用させてください。
国内臨床試験では妊娠例が1例報告されています。活動期の潰瘍性大腸炎患者を対象とした、前観察期、投与期(8週間)および後観察期(1週間)から成る試験において、リアルダの8週間(57日間)の投与を終え、後観察期間中に妊娠と確定診断されました。確定診断時の胎児週齢は7週であったことから、リアルダを投与している期間中に妊娠が成立していたことになります。なお、本症例はリアルダの投与終了後、他の経口メサラジン製剤へ切り替え、胎児週齢38週に帝王切開により出産していますが、母子ともに異常は認められませんでした1)、2)。電子添文抜粋
9. 特定の背景を有する患者に関する注意
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。なお、動物試験において、メサラジンによる催奇形性は認められていない。【参考資料】
1) 社内資料(国内第Ⅲ相試験(MD090111U33試験))
2) インタビューフォーム Ⅷ. 安全性(使用上の注意等)に関する項目 6. 特定の背景を有する患者に関する注意 (5)妊婦2026年2月改訂
-
リアルダを授乳婦に投与できますか?
授乳婦に対する臨床試験は実施しておらず、安全性が確立していないことから、治療上の有益性及び母乳栄養の有益性を考慮して、授乳の継続又は中止を検討してください。
メサラジン(化学名:5-アミノサリチル酸)製剤を服用している授乳中の母親の乳汁中において、低濃度のメサラジンおよび高濃度のメサラジン代謝物(N-アセチル-5-アミノサリチル酸)が検出されたとの報告があります1)~3)。また、海外において、メサラジン製剤服用中に授乳した患者の乳児に下痢が発現したとの報告があります4)、5)。電子添文抜粋
9. 特定の背景を有する患者に関する注意
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。メサラジンでヒト乳汁中へ移行することが報告されている。また、乳児に下痢が起きることが報告されている。【参考資料】
1) Jenss, H. et al.:Am. J. Gastroenterol. 1990;85(3):331
2) Christensen, L. A. et al.:Acta Obstet. Gynecol. Scand. 1994;73(5):399-402
3) Klotz, U. et al.:Lancet. 1993;342(8871):618-619
4) Nelis, G. F.:Lancet. 1989;1(8634):383
5) Ito, S. et al.:Am. J. Obstet. Gynecol. 1993;168(5):1393-13992026年2月改訂
安全性
-
便中にリアルダの錠剤が出てくることはありますか?
便中にリアルダの錠剤が排泄されることがあります。
成人の潰瘍性大腸炎患者を対象とした国内臨床試験では、2例でそれぞれ1回ずつ錠剤が便中に認められましたが、錠剤が便中へ排泄されたことに起因する原疾患の悪化等は認められませんでした1)。電子添文抜粋
14. 適用上の注意
14.4 薬剤投与後の注意
14.4.1 便中に錠剤が認められることがある。
【参考資料】
1) インタビューフォーム Ⅷ. 安全性(使用上の注意等)に関する項目 11. 適用上の注意2026年2月改訂
製剤
-
リアルダ錠は一包化できますか?
リアルダ錠をPTPシートから取り出し一包化調剤することは避けてください。吸湿により溶出性に影響を及ぼすことがあるため、服用直前にPTPシートから錠剤を取り出してください。
電子添文抜粋
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.1 吸湿により溶出性に影響を及ぼすことがあるため、本剤をPTPシートから取り出し一包化調剤することは避けること。
14.2 薬剤交付時の注意
14.2.2 服用直前にPTPシートから錠剤を取り出させること。
2026年2月改訂
-
リアルダ錠は粉砕・分割できますか?
リアルダ錠は、粉砕・分割して投与することはできません。
本剤は、有効成分であるメサラジンを親水性基剤と親油性基剤からなるマトリックス中に分散させた素錠部に、pH応答性の高分子フィルムをコーティングすることで、メサラジンを標的部位である大腸に送達し、大腸全域へ持続的に放出することを可能にした放出制御製剤です。粉砕・分割すると、その特性が失われてしまいます。電子添文抜粋
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.2 乳鉢による粉砕は行わないこと。
14.3 薬剤投与時の注意
本剤は放出制御製剤であることより、かまずに服用すること。2026年2月改訂
-
リアルダ錠は簡易懸濁できますか?
リアルダ錠は、簡易懸濁して投与することはできません。
本剤は、有効成分であるメサラジンを親水性基剤と親油性基剤からなるマトリックス中に分散させた素錠部に、pH応答性の高分子フィルムをコーティングすることで、メサラジンを標的部位である大腸に送達し、大腸全域へ持続的に放出することを可能にした放出制御製剤です。簡易懸濁すると、その特性が失われてしまいます。電子添文抜粋
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.2 乳鉢による粉砕は行わないこと。
14.3 薬剤投与時の注意
本剤は放出制御製剤であることより、かまずに服用すること。2026年2月改訂
-
リアルダ錠の貯法が冷所保存になっている理由は?
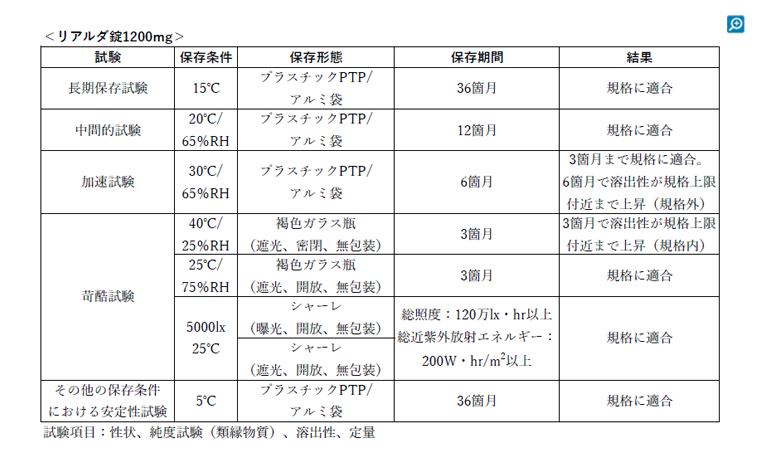
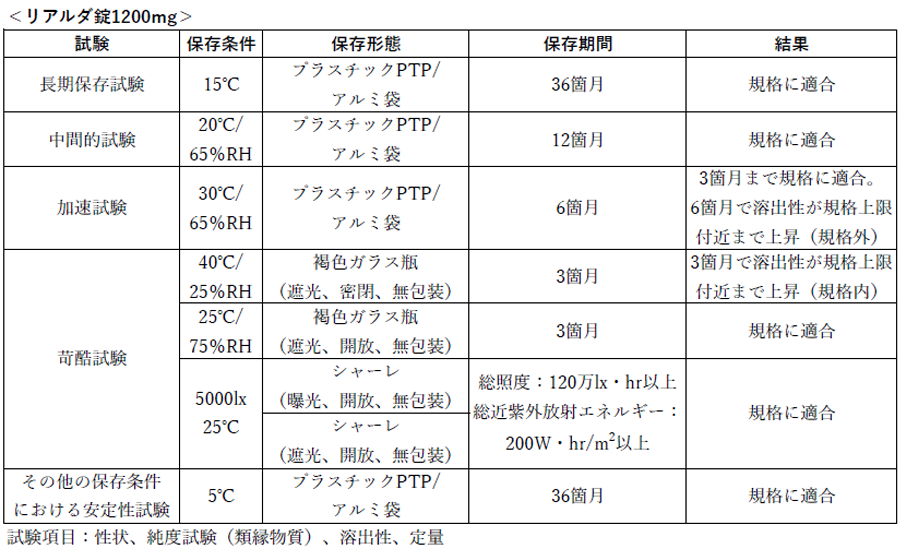
リアルダ錠1200mgについて、室温保存の規定(1~30℃)の上限である30℃(65%RH)で6ヵ月の加速試験を実施したところ、3ヵ月まで規格に適合しましたが、6ヵ月で溶出性が規格上限付近まで上昇し規格外となったためです1)。
高温多湿の日本における取り扱いやロット間のばらつきを考慮し、冷所保存(1~15℃)に設定しています。電子添文抜粋
貯法:冷所保存
【参考資料】
1) インタビューフォーム Ⅳ. 製剤に関する項目 6. 製剤の各種条件下における安定性2026年2月改訂
-
リアルダ錠の家庭での保管方法は?
リアルダ錠の貯法は、冷所保存(1~15℃)ですので、家庭では冷蔵庫に保管してください1)、2)。
電子添文抜粋
貯法:冷所保存
【参考資料】
1) 患者指導箋:リアルダ錠を服用されている方へ(製作物コード:14438)
2) 患者冊子:リアルダ錠を服用されている方へ(製作物コード:14335)2026年2月改訂
-
リアルダ錠の貯法は冷所保存ですが、薬局から持ち帰る際、保冷は必要ですか?
薬局から持ち帰る程度の短い時間であれば、保冷せずそのまま持ち帰って構いません。帰宅後すぐに冷蔵庫に保管するようにしてください1)、2)。
電子添文抜粋
貯法:冷所保存
【参考資料】
1) 患者指導箋:リアルダ錠を服用されている方へ(製作物コード:14438)
2) 患者冊子:リアルダ錠を服用されている方へ(製作物コード:14335)2026年2月作成
-
リアルダ錠の貯法は冷所保存ですが、旅行などで持ち歩く際の温度管理はどのようにすればよいですか?
常温であれば1週間程度そのまま持ち歩くことができます1)、2)。
夏場など高温になる場合は、保冷剤などを使用してのご移動をご検討ください。
旅行先で冷蔵庫に保管できる場合は、なるべく冷蔵庫に保管してください。冷蔵庫に保管したまま持ち帰るのを忘れないようご注意ください。電子添文抜粋
貯法:冷所保存
【参考資料】
1) 患者指導箋:リアルダ錠を服用されている方へ(製作物コード:14438)
2) 患者冊子:リアルダ錠を服用されている方へ(製作物コード:14335)2026年2月作成
-
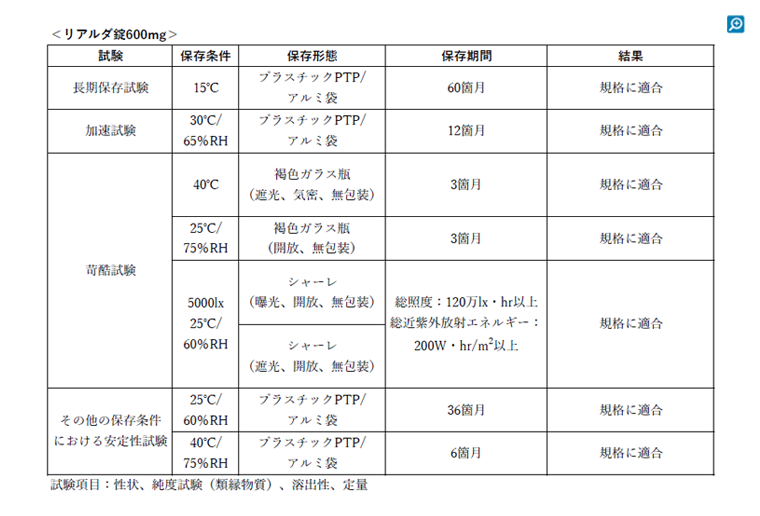
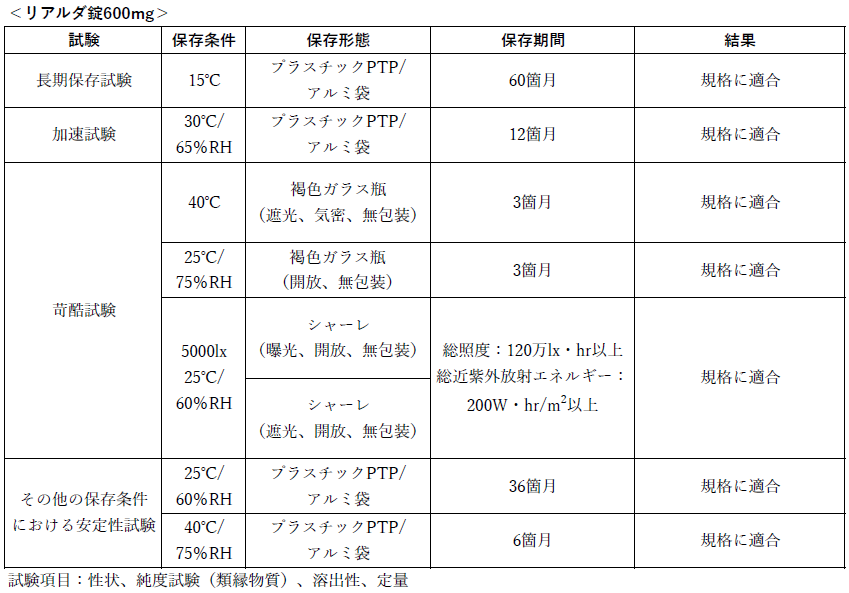
リアルダ錠の各種条件下における安定性は?