- 医療関係者向けホーム
- 循環器領域
- ユリス®錠
- Clinical Study:後期第Ⅱ相試験(用量反応検証試験) 安全性
 Clinical Study後期第Ⅱ相試験(用量反応検証試験)
Clinical Study後期第Ⅱ相試験(用量反応検証試験)
安全性
痛風関節炎を除く副作用発現状況(SP解析対象)注)
痛風関節炎を除く副作用(臨床検査値異常を含む)は、プラセボ群で6/39例(15.4%)、ドチヌラド0.5mg群で5/40例(12.5%)、1mg群で6/42例(14.3%)、2mg群で6/39例(15.4%)、4mg群で4/40例(10.0%)に認められた。2例以上に発現した副作用は、プラセボ群で尿中β2ミクログロブリン増加が2/39例(5.1%)、ドチヌラド1mg群でβ-NアセチルDグルコサミニダーゼ増加が3/42例(7.1%)、2mg群で尿中β2ミクログロブリン増加、β-NアセチルDグルコサミニダーゼ増加、白血球数増加がそれぞれ2/39例(5.1%)、4mg群で尿中β2ミクログロブリン増加、β-NアセチルDグルコサミニダーゼ増加、α1ミクログロブリン増加がそれぞれ2/40例(5.0%)に認められた。ドチヌラド0.5mg群でみられた副作用は、四肢不快感、γ-グルタミルトランスフェラーゼ増加等でいずれも1/40例(2.5%)に認められた。本試験において、死亡例を含む重篤な副作用は認められなかった。また本試験において投与中止に至った痛風関節炎を除く副作用は、プラセボ群で尿中β2ミクログロブリン増加が1例に認められた。
- SP解析対象:治験薬を1回以上投与され、投与後に安全性の評価が可能な情報が得られている症例
痛風関節炎(SP解析対象)注)
痛風関節炎の副作用は、ドチヌラド0.5mg群で1/40例(2.5%)、1mg群で2/42例(4.8%)、2mg群で3/39例(7.7%)及び4mg群で3/40例(7.5%)に認められた。プラセボ群では痛風関節炎の副作用は認められなかった。本試験において投与中止に至った痛風関節炎の副作用は、1mg群で1例に認められた。
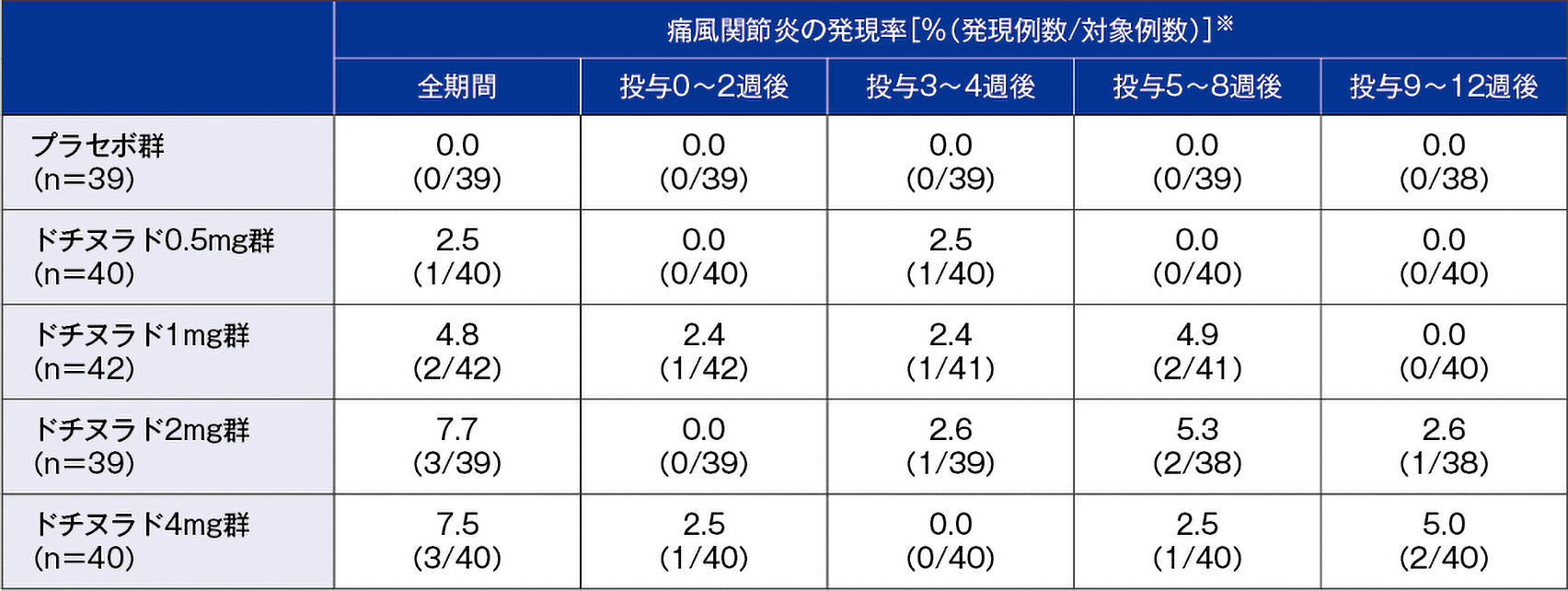
投与群ごとの痛風関節炎の時期別発現率は下表のとおりであった。
- ※:各期間で症例の重複あり
- 注)本薬の薬理効果により血清尿酸値の急激な変動に伴い痛風関節炎が誘発される可能性があることから、痛風関節炎に関しては他の有害事象と別集計とした。