- 医療関係者向けホーム
- 循環器領域
- ユリス®錠
- Clinical Study:後期第Ⅱ相試験(用量反応検証試験) 血清尿酸値低下率
 Clinical Study後期第Ⅱ相試験(用量反応検証試験)
Clinical Study後期第Ⅱ相試験(用量反応検証試験)
血清尿酸値低下率
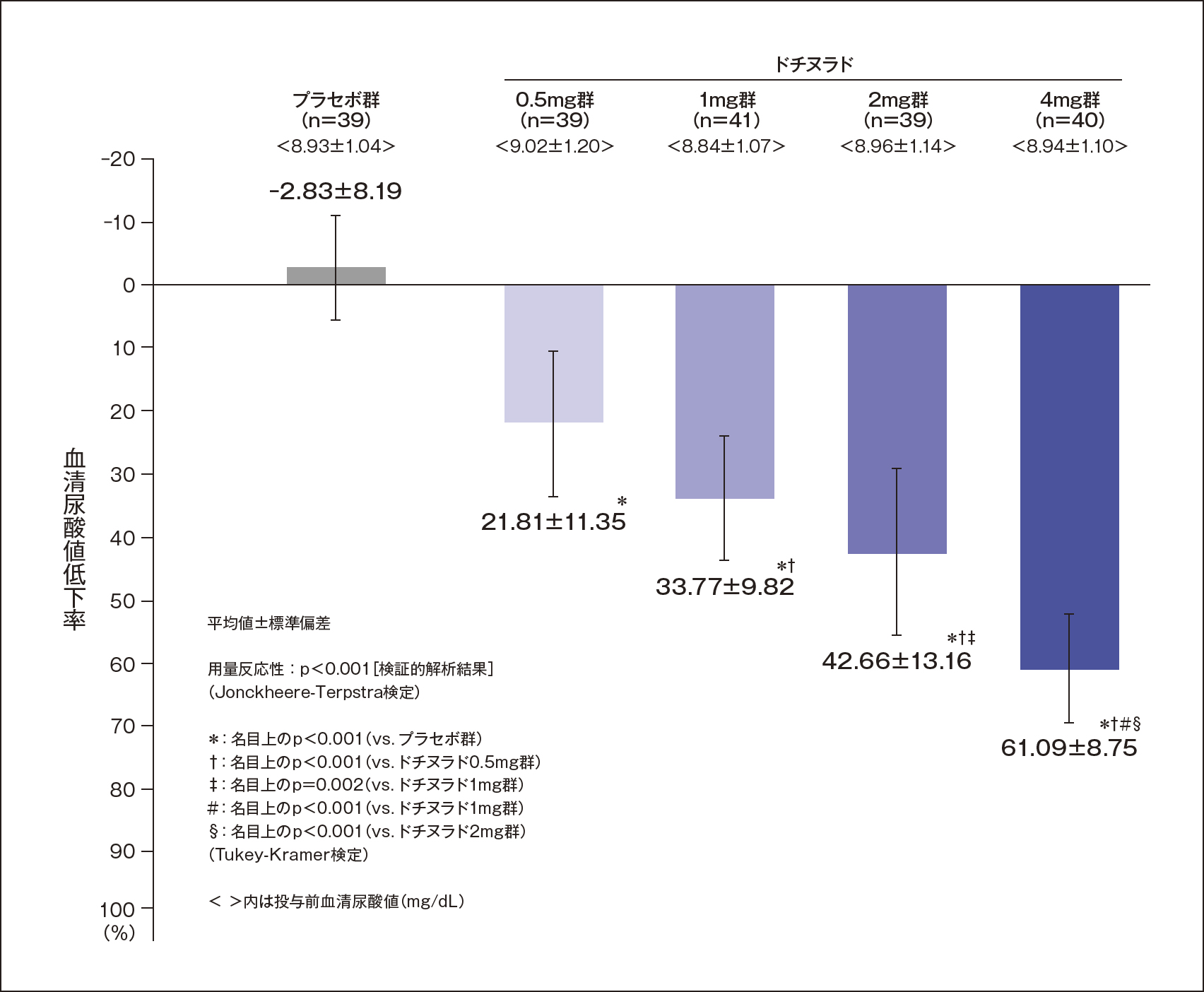
投与終了時の血清尿酸値低下率(主要評価項目;FAS解析対象、LOCF)
投与終了時における投与前値からの血清尿酸値低下率(平均値±標準偏差)は、プラセボ群で-2.83±8.19%、ドチヌラド0.5mg群で21.81±11.35%、1mg群で33.77±9.82%、2mg群で42.66±13.16%、4mg群で61.09±8.75%であり、ドチヌラドの用量反応性が検証された([主解析]p<0.001、Jonckheere-Terpstra検定)。また、群間比較では、いずれの群間においても有意差が認められた(ドチヌラド1mg群 vs. 2mg群:名目上のp=0.002、その他の群間:名目上のp<0.001、Tukey-Kramer検定)。
- LOCF:欠測データを最後に観察した値に置き換えて補完する
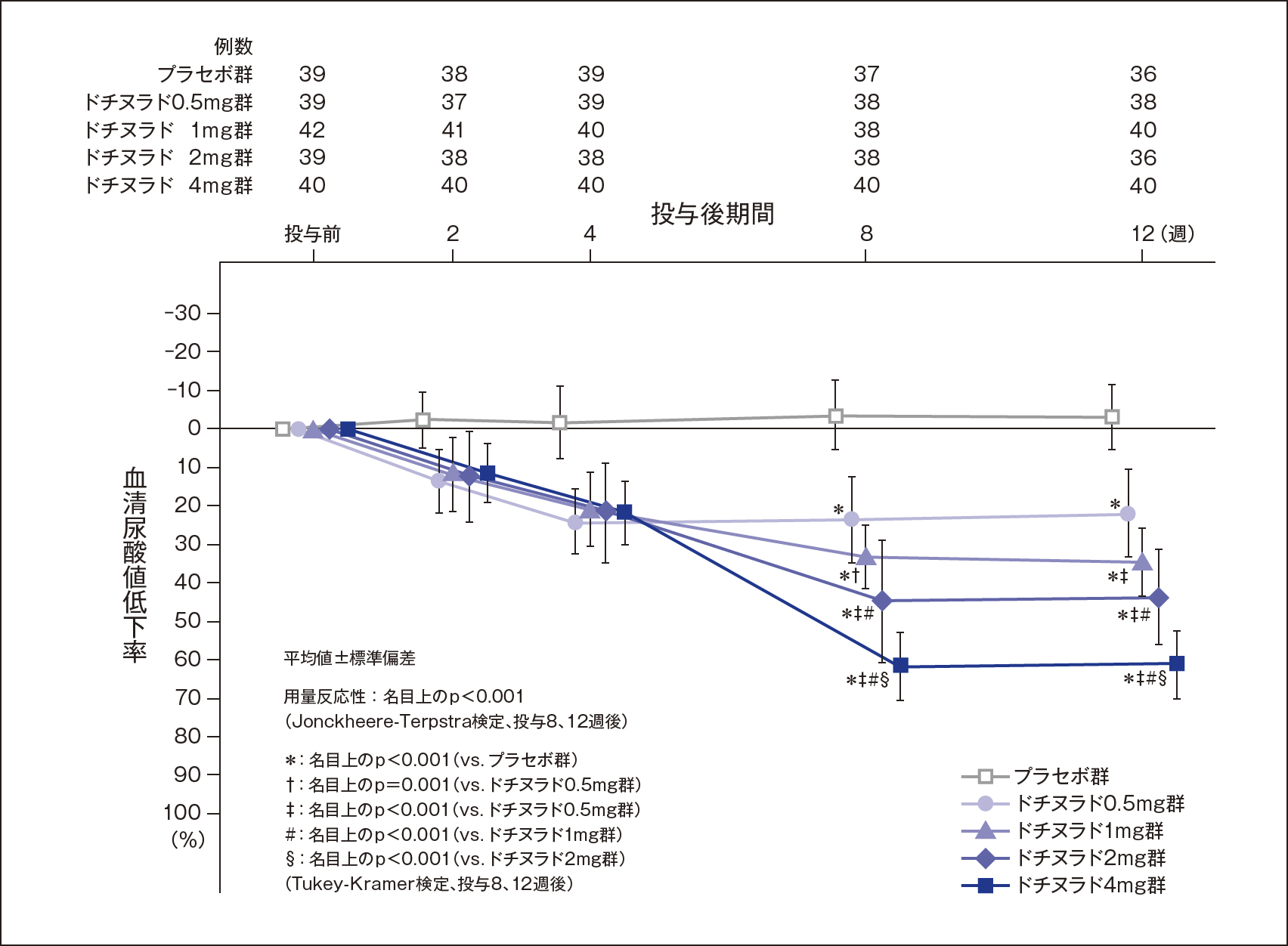
各時点の血清尿酸値低下率(副次評価項目;FAS解析対象)
各時点(投与2、4、8、12週後)における投与前値からの血清尿酸値低下率(平均値±標準偏差)は、下図のとおりに推移し、投与12週後では、プラセボ群で-3.01±8.36%、ドチヌラド0.5mg群で21.92±11.48%、1mg群で34.52±8.71%、2mg群で43.86±12.34%、4mg群で61.09±8.75%であった。
投与8、12週後では、ドチヌラドの用量反応性が認められた(名目上のp<0.001、Jonckheere-Terpstra検定)。また、投与8週後及び12週後の群間比較では、いずれの群間においても有意差が認められた(投与8週後のドチヌラド0.5mg群 vs. 1mg群:名目上のp=0.001、その他の群間:名目上のp<0.001、Tukey-Kramer検定)。