- 医療関係者向けホーム
- 消化器領域
- アダリムマブBS「MA」
- Information:薬効薬理
 Information
Information
薬効薬理
作用機序
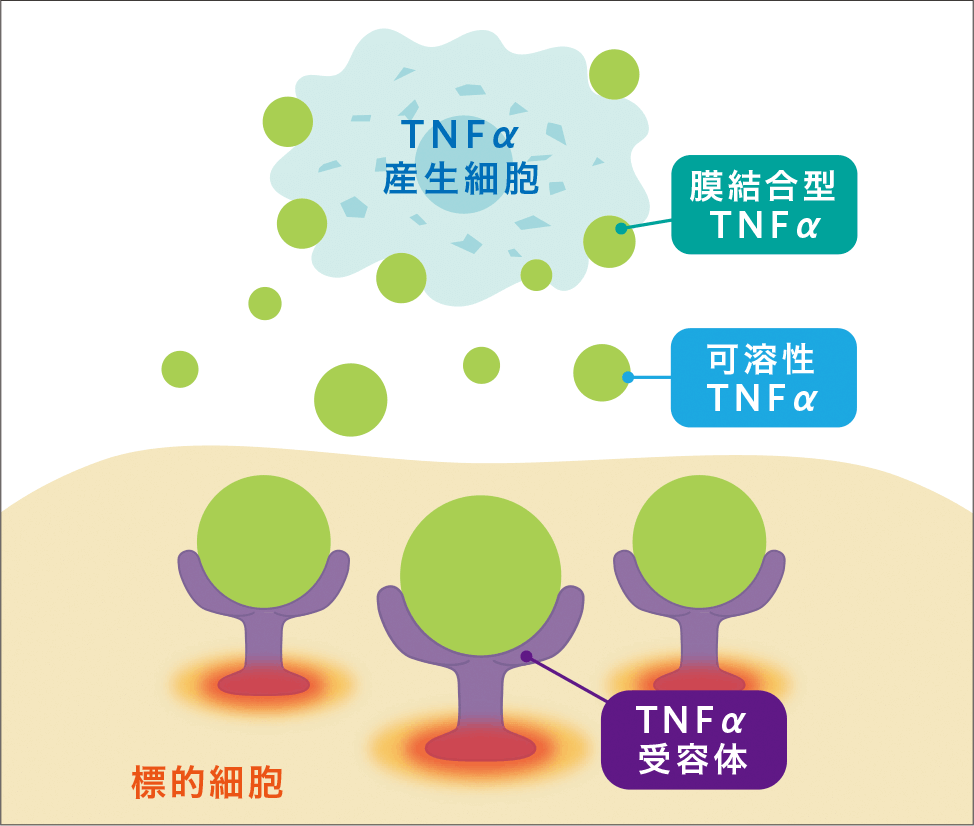
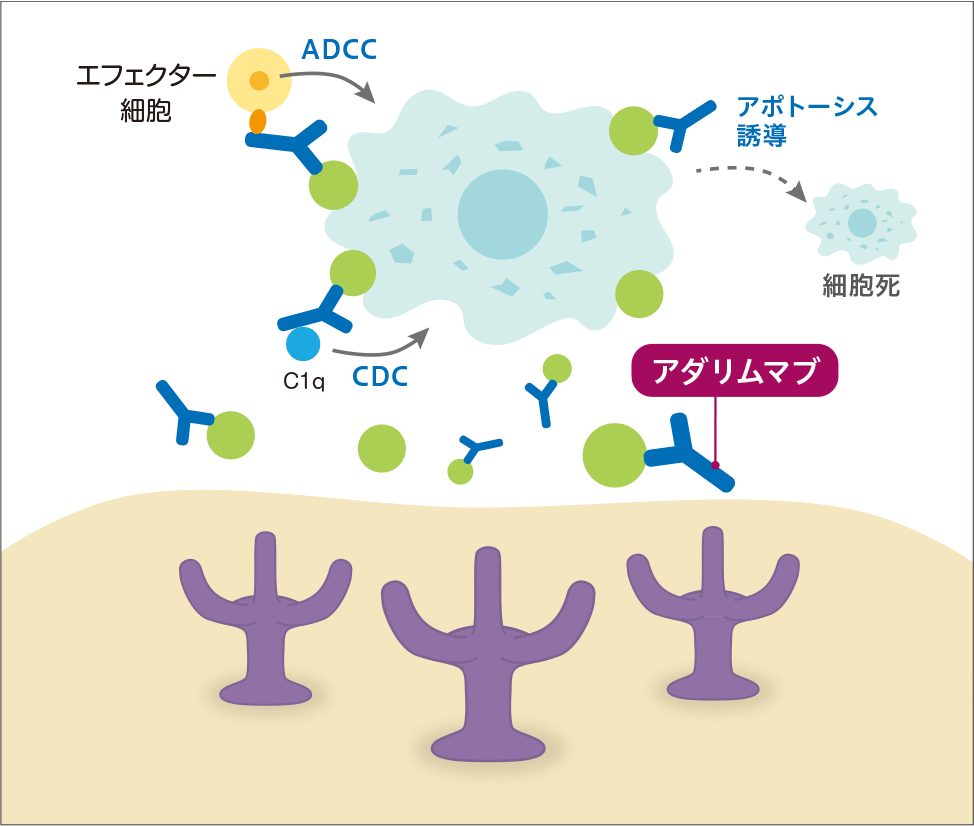
TNFαは炎症反応や免疫反応に関わる重要なサイトカインである。アダリムマブはヒトTNFαに特異的に結合し、細胞表面のp55及びp75TNF受容体とTNFαの相互作用を阻害することでTNFαの生物活性を中和する1)。また、アダリムマブは膜結合型TNFαと結合することで、逆シグナルによるアポトーシスやFc領域を介したADCC活性あるいはCDC活性を誘導し、TNFα産生細胞を破壊することにより炎症反応を抑制すると考えられている2,3,4)。
非臨床試験
以下の非臨床試験では、本剤として40mg/0.8mL製剤及び原薬を使用し、先行バイオ医薬品は国内流通品と同一の品質特性を有する韓国及び欧州流通品を使用した。本剤の40mg/0.8mL製剤と40mg/0.4mL製剤のTNFファミリーに対する結合親和性、Fc受容体及びC1qに対する結合親和性、TNFα誘導性細胞傷害に対する阻害活性、ADCC活性及びCDC活性、アポトーシス誘導活性は同等であることが確認されている。
1. TNFファミリーに対する結合親和性(in vitro)5)
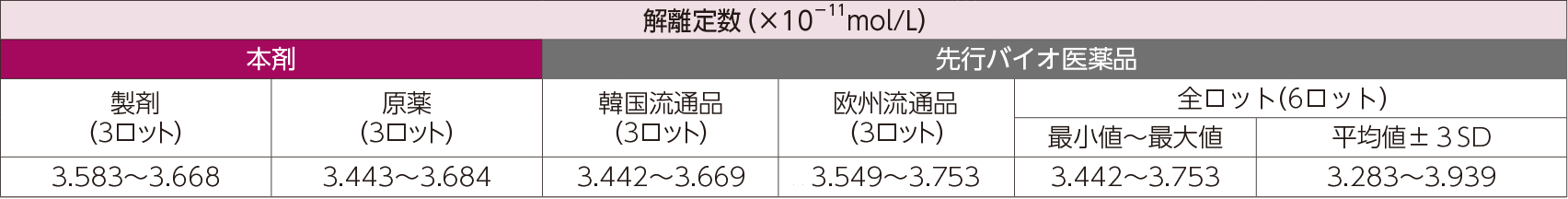
(1)可溶性TNFαに対する結合親和性(in vitro)
本剤又は先行バイオ医薬品の可溶性TNFαに対する結合親和性を、表面プラズモン共鳴(SPR)法により算出した解離定数を指標として検討した。その結果、本剤の解離定数は先行バイオ医薬品と類似していた。
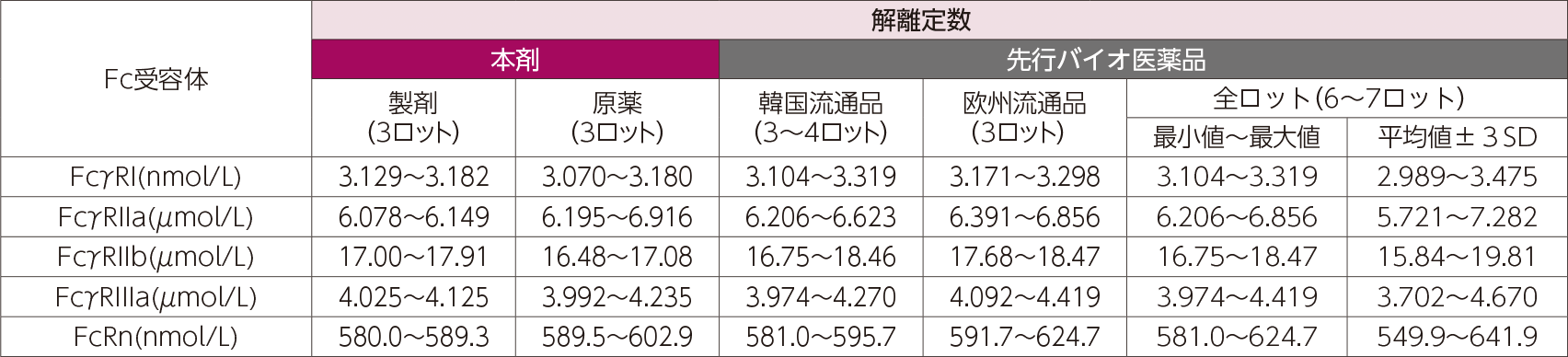
2. 各種Fc受容体に対する結合親和性(in vitro)5)
本剤又は先行バイオ医薬品のFcγRI、FcγRIIa、FcγRIIb、FcγRIIIa及びFcRnに対する結合親和性を、SPR法により算出した解離定数を指標として検討した。その結果、本剤の各種Fc受容体に対する解離定数はいずれも先行バイオ医薬品と類似していた。
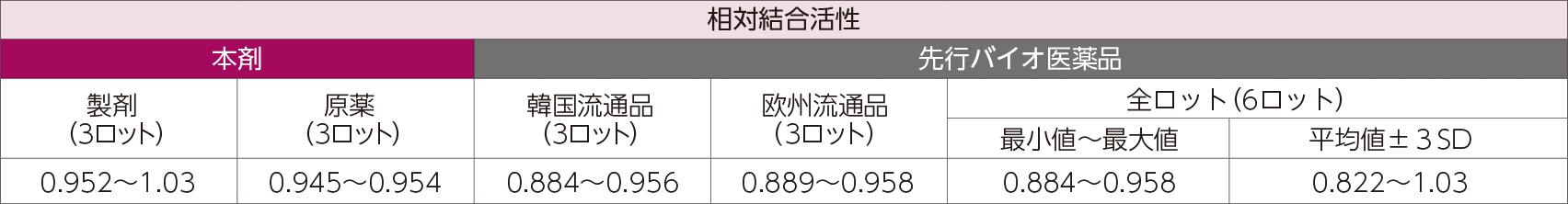
3. C1qに対する結合活性(in vitro)5)
本剤又は先行バイオ医薬品のC1qに対する結合活性を、ELISA法により算出した相対結合活性を指標として検討した。その結果、本剤の相対結合活性は先行バイオ医薬品と類似していた。
- 相対結合活性 = 標準物質のEC50値 / 各被験物質のEC50値
4. TNFα誘導性細胞傷害に対する阻害活性(in vitro)5)
本剤又は先行バイオ医薬品のTNFα誘導性細胞傷害に対する阻害活性を、マウス線維芽細胞株(L929細胞)を用いた細胞アッセイ法により算出した相対阻害活性を指標として検討した。その結果、本剤の相対阻害活性は先行バイオ医薬品と類似していた。
- 相対阻害活性 = 標準物質の50%阻害濃度(IC50)値 / 各被験物質のIC50値
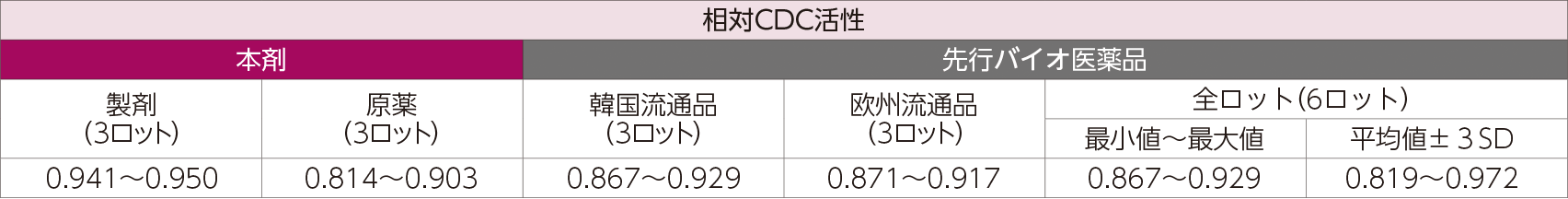
5. ADCC活性及びCDC活性(in vitro)5)
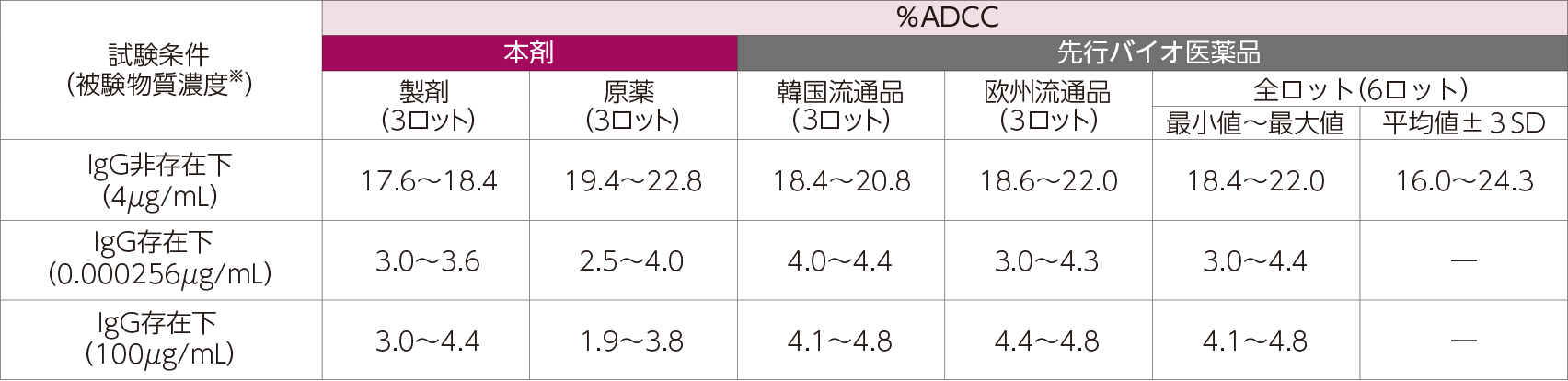
(1)ADCC活性(in vitro)
本剤又は先行バイオ医薬品のADCC活性を、標的細胞としてヒト膜結合型TNFαを強制発現させたCHO-K1細胞、エフェクター細胞として末梢血単核細胞(PBMC)を用いた細胞アッセイ法により算出した化学発光強度比(%ADCC)を指標として検討した。IgG非存在下及びIgG存在下(10mg/mL)の試験条件で検討した結果、IgG非存在下における本剤の%ADCCは先行バイオ医薬品と類似していた。一方、IgG存在下では、いずれの被験物質もIgG非存在下に比べて顕著にADCC活性が低下し、100μg/mLにおいても明らかなADCC活性は認められなかった。
- %ADCC = 各被験物質の化学発光強度 / 細胞を完全に溶解したときの化学発光強度×100
- ※:評価に用いる被験物質濃度は、使用するPBMCと標準物質1ロットの用量反応関係をもとに設定した。
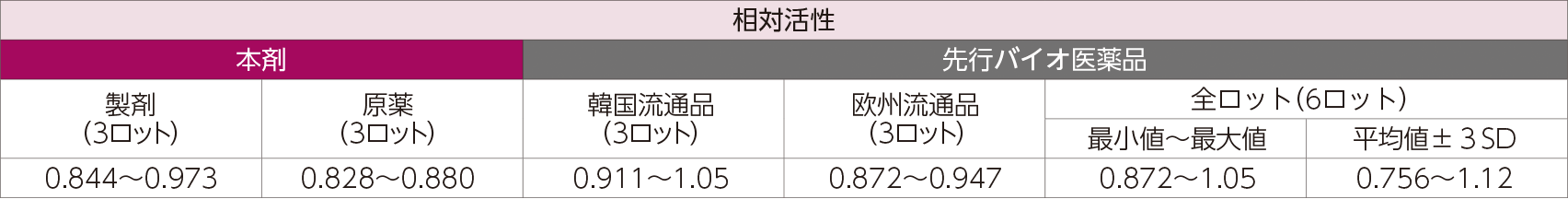
6. アポトーシス誘導活性(in vitro)5)
本剤又は先行バイオ医薬品のアポトーシス誘導活性を、九州大学より供与されたヒト膜結合型TNFα発現Jurkat細胞4,6,7)及びフローサイトメトリーを用いた細胞アッセイ法により算出した相対活性を指標として検討した。その結果、本剤の相対活性は先行バイオ医薬品と類似していた。
- 相対活性 = 標準物質のEC50値 / 各被験物質のEC50値
7. 関節炎抑制作用(マウス)8)
ヒトTNFαを高発現させたトランスジェニックマウス(Tg197マウス)を用いて、本剤(製剤)及び先行バイオ医薬品(韓国及び欧州流通品)の関節炎発症に及ぼす影響を、肉眼的所見による関節炎スコア及び病理組織学的所見による関節炎スコアを用いて評価した。
試験方法)
1群8例(雄4例、雌4例)のTg197マウス(3週齢)に、溶媒、本剤又は先行バイオ医薬品をそれぞれ1、3及び10mg/kg、週2回反復腹腔内投与した(7週間、合計14回)。投与開始から1週間毎に体重測定と関節炎の肉眼的評価(各個体の関節炎の程度を0から3.0点でスコア化)を実施し、3週齢から10週齢までのスコア累積値も算出した。10週齢時点で両側の後肢膝関節を摘出して、病理組織学的評価(各個体の関節炎の程度を0から4点でスコア化)を実施した。
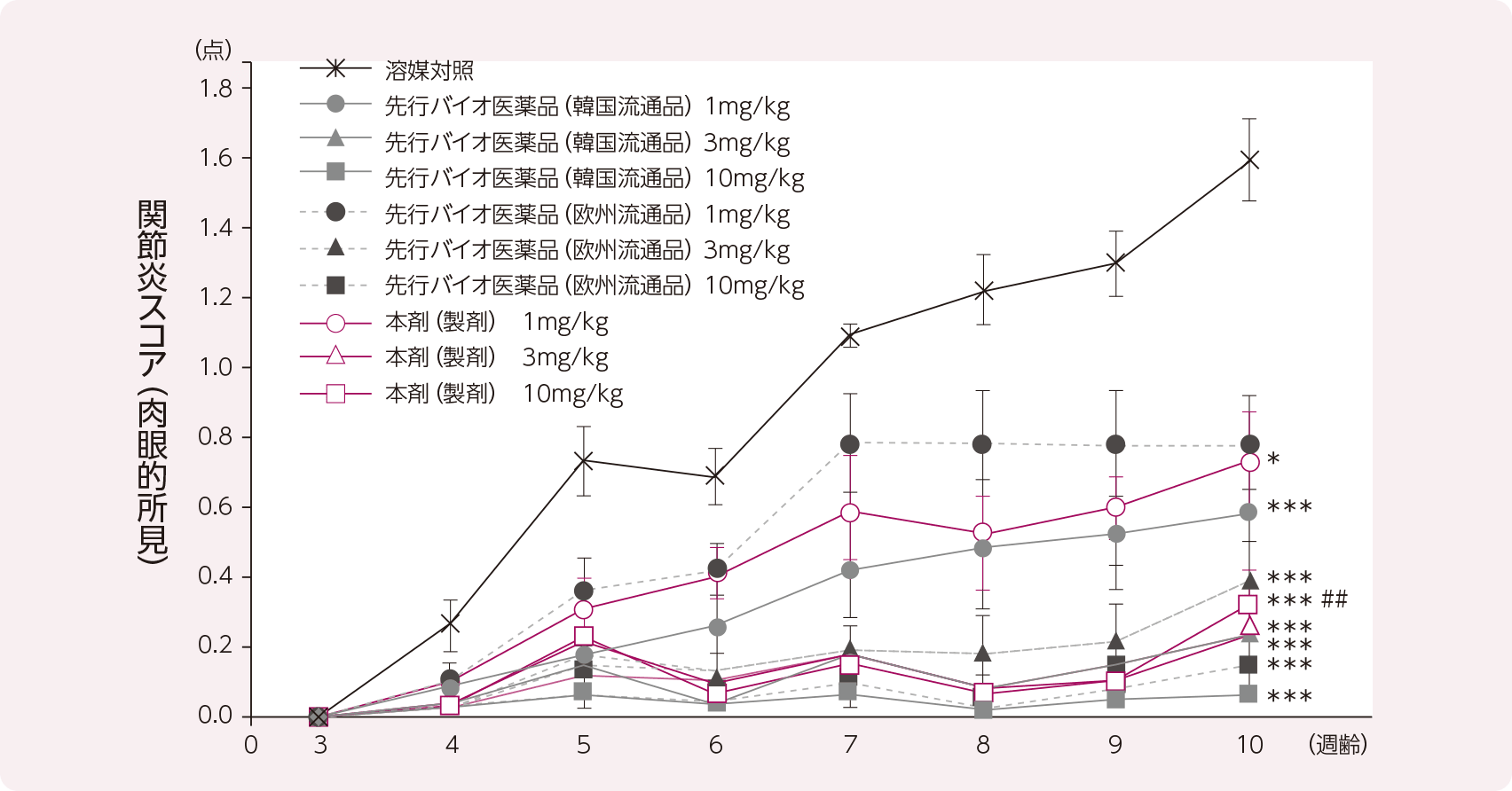
(1)肉眼的所見による関節炎スコアの推移及び累積値
各群における関節炎スコアは下図の通り推移した。本剤群と先行バイオ医薬品群における3及び10mg/kg群の10週齢時の関節炎スコア及び累積値は、溶媒対照群に比し低値であった。10週齢時の関節炎スコアは1及び3mg/kgの投与量において、本剤群と先行バイオ医薬品群との間に有意差は認められなかった。10mg/kg群の10週齢時の関節炎スコアにおいて本剤群と先行バイオ医薬品(韓国流通品)群間に有意差が認められたものの偶発的なものと考えられ、本剤群の肉眼的所見における関節炎スコアは先行バイオ医薬品群と類似していると考えられた。
- 結果は、1群7~8例の平均値及び標準誤差で示す(6週齢以降は本剤3mg/kg群のみ7例)。
- *:p<0.05, ***:p<0.001 vs. 溶媒対照群(10週齢時、Kruskal-Wallis検定及びDunnの多重比較検定)
- ##:p<0.01 vs. 先行バイオ医薬品(韓国流通品)10mg/kg群(10週齢時、Kruskal-Wallis検定及びDunnの多重比較検定)
- 10週齢の関節炎スコアは、1及び3mg/kgの投与量において被験物質間に統計学的有意差は認められなかった(p>0.05、Kruskal-Wallis検定)。
- 結果は、1群7~8例の平均値及び標準誤差で示す(本剤3mg/kg群のみ7例)。
- **:p<0.01, ***:p<0.001 vs. 溶媒対照群(Kruskal-Wallis検定及びDunnの多重比較検定)
- 1, 3及び10mg/kgの投与量において、被験物質間に統計学的有意差は認められなかった(p>0.05、Kruskal-Wallis検定)。
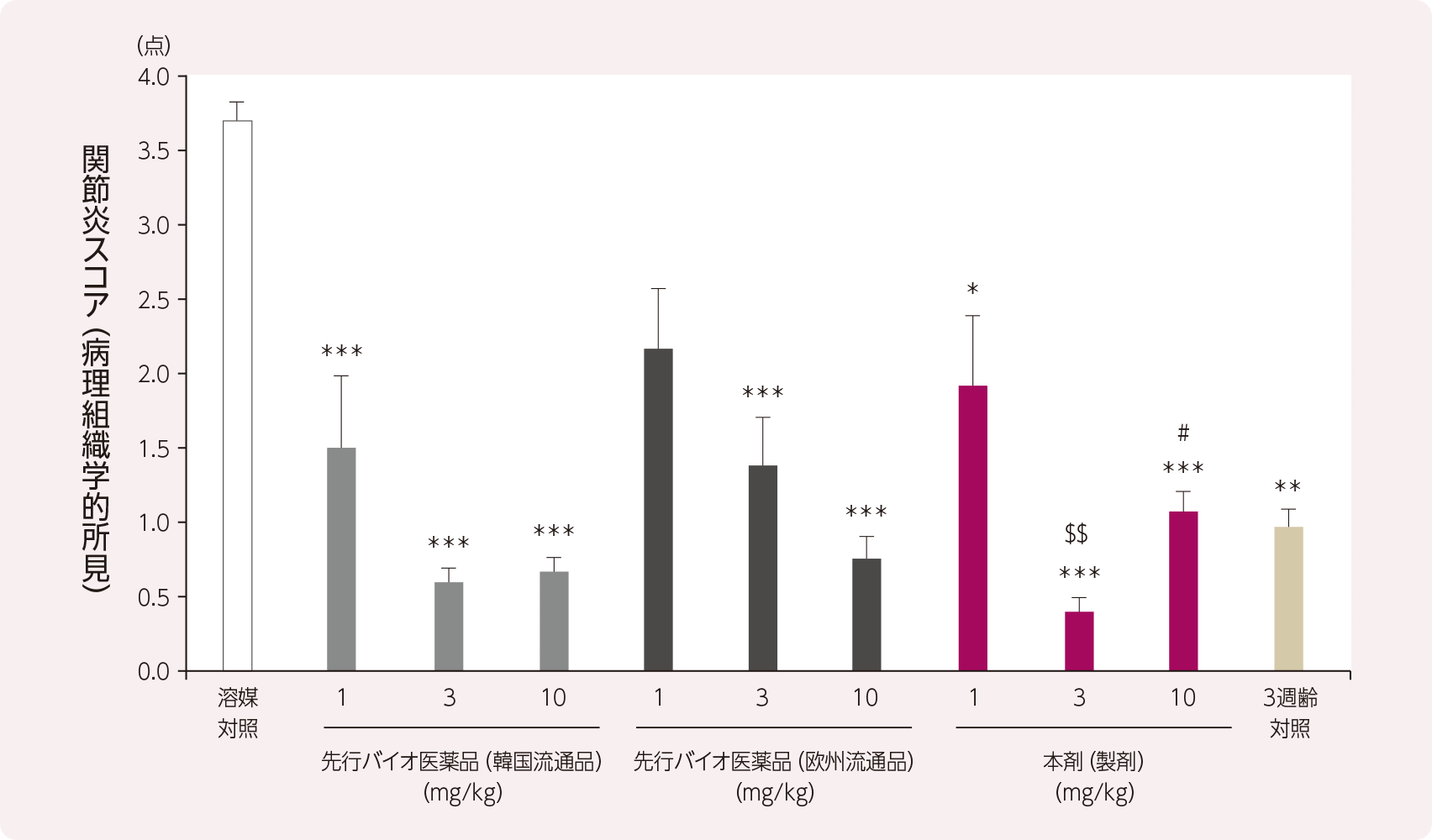
(2)病理組織学的所見による関節炎スコア
溶媒対照群の関節炎スコアは関節炎発症前の3週齢対照群と比較して有意に高値であった。本剤群及び先行バイオ医薬品群の関節炎スコアは、溶媒対照群と比較して、先行バイオ医薬品(欧州流通品)1mg/kg群を除き、有意差が認められた。同用量で比較すると、1mg/kg群の関節炎スコアは、本剤群と先行バイオ医薬品群の間に有意差は認められなかった。本剤3及び10mg/kg群の関節炎スコアでは、一方の先行バイオ医薬品群と有意差が認められたものの、もう一方の先行バイオ医薬品群とは有意差がなかったことから、先行バイオ医薬品との間での一貫した差異ではなく、実験内のばらつきによるものと考えられた。したがって、本剤群の病理組織学的所見における関節炎スコアは先行バイオ医薬品群と類似していると考えられた。
- 溶媒対照群及び被験物質群の結果は1群7~8例の平均値及び標準誤差で示す(本剤3mg/kg群及び先行バイオ医薬品(欧州流通品)10mg/kg群のみ7例)。
- 3週齢対照群の結果は4例の平均値及び標準誤差で示す。
- *:p<0.05, **:p<0.01, ***:p<0.001 vs. 溶媒対照群(Kruskal-Wallis検定及びDunnの多重比較検定)
- $$:p<0.01 vs. 先行バイオ医薬品(欧州流通品)3mg/kg群(Kruskal-Wallis検定及びDunnの多重比較検定)
- #:p<0.05 vs. 先行バイオ医薬品(韓国流通品)10mg/kg群(Kruskal-Wallis検定及びDunnの多重比較検定)
- 1mg/kgの各被験物質間に統計学的有意差は認められなかった(p>0.05、Kruskal-Wallis検定)。
略語
- TNF:Tumor Necrosis Factor
- ADCC:Antibody-Dependent Cellular Cytotoxicity
- CDC:Complement-Dependent Cytotoxicity
- 1)Zhao S, et al. Curr Rheumatol Rep. 2018;20:57(p.1-10).
- 2)天野宏一. 日本内科学会雑誌. 2011;100:2966
- 3)Tracey D, et al. Pharmacol Ther. 2008;117:244
- 4)Horiuchi T, et al. Rheumatology. 2010;49:1215
- 5)持田製薬社内資料(薬理試験-in vitro 薬理試験- )
- 6)Ueda N, et al. Inflamm Bowel Dis. 2013;19:1224
- 7)Mitoma H, et al. Arthritis Rheum. 2008;58:1248
- 8)持田製薬社内資料(薬理試験-ヒトTNFαトランスジェニックマウスモデルにおける有効性の検討-)