- 医療関係者向けホーム
- 消化器領域
- アダリムマブBS「MA」
- Information:薬物動態
 Information
Information
薬物動態
本剤の薬物動態は、健康成人男性を対象とした海外第Ⅰ相試験、健康成人男性を対象とした国内生物学的同等性試験(BE試験)及びMTX治療で効果不十分なRA患者を対象とした国際共同第Ⅲ相試験の成績に基づき評価した。
血中濃度
1. 単回投与試験
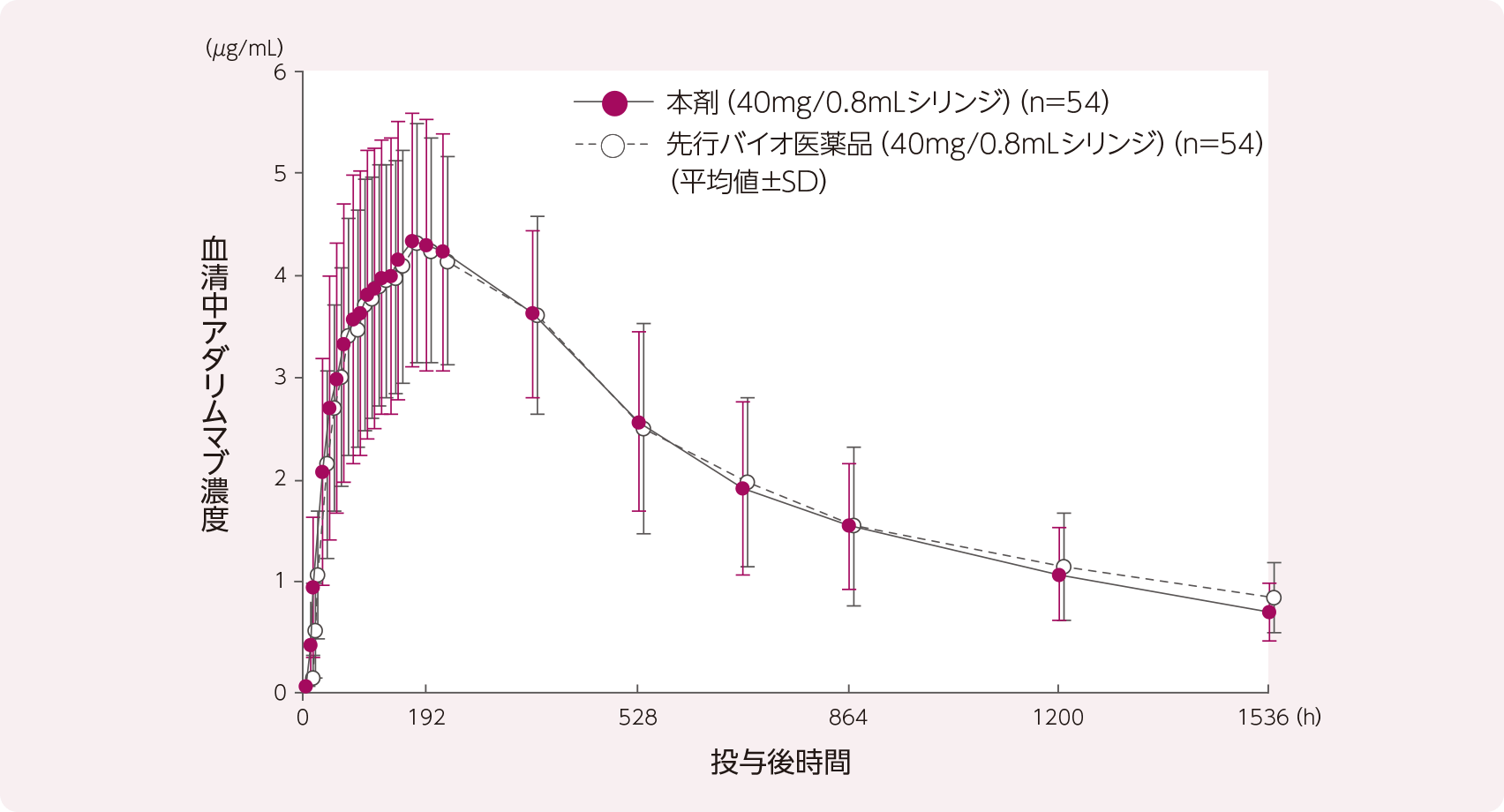
(1)海外第Ⅰ相試験(健康成人)(外国人データ)1)
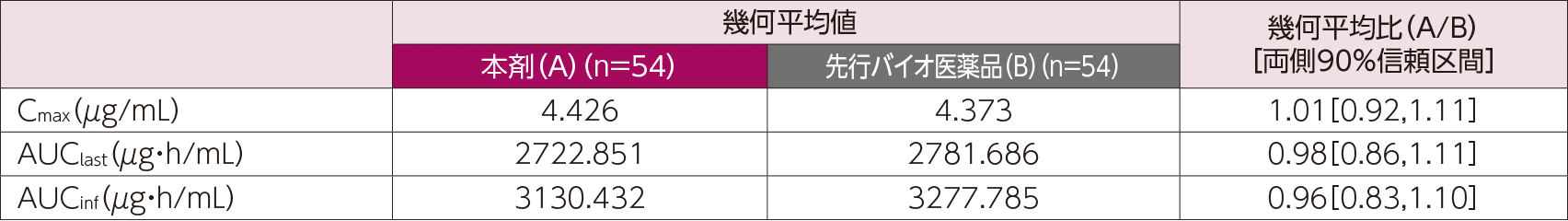
健康成人男性に本剤(40mg/0.8mLシリンジ)又は先行バイオ医薬品(40mg/0.8mLシリンジ、欧州流通品)を1回40mgを単回皮下投与し、投与65日目までの薬物動態を評価した。両群のCmax及びAUCinfの幾何平均比の両側90%信頼区間は、いずれも治験実施計画書で定めた薬物動態の同等性判定基準(0.80~1.25)の範囲内であり、両剤の薬物動態の同等性が検証された。また、AUClastについても0.80~1.25の範囲内であった。
- 平均値±SD
- *1:中央値[最小値,最大値]
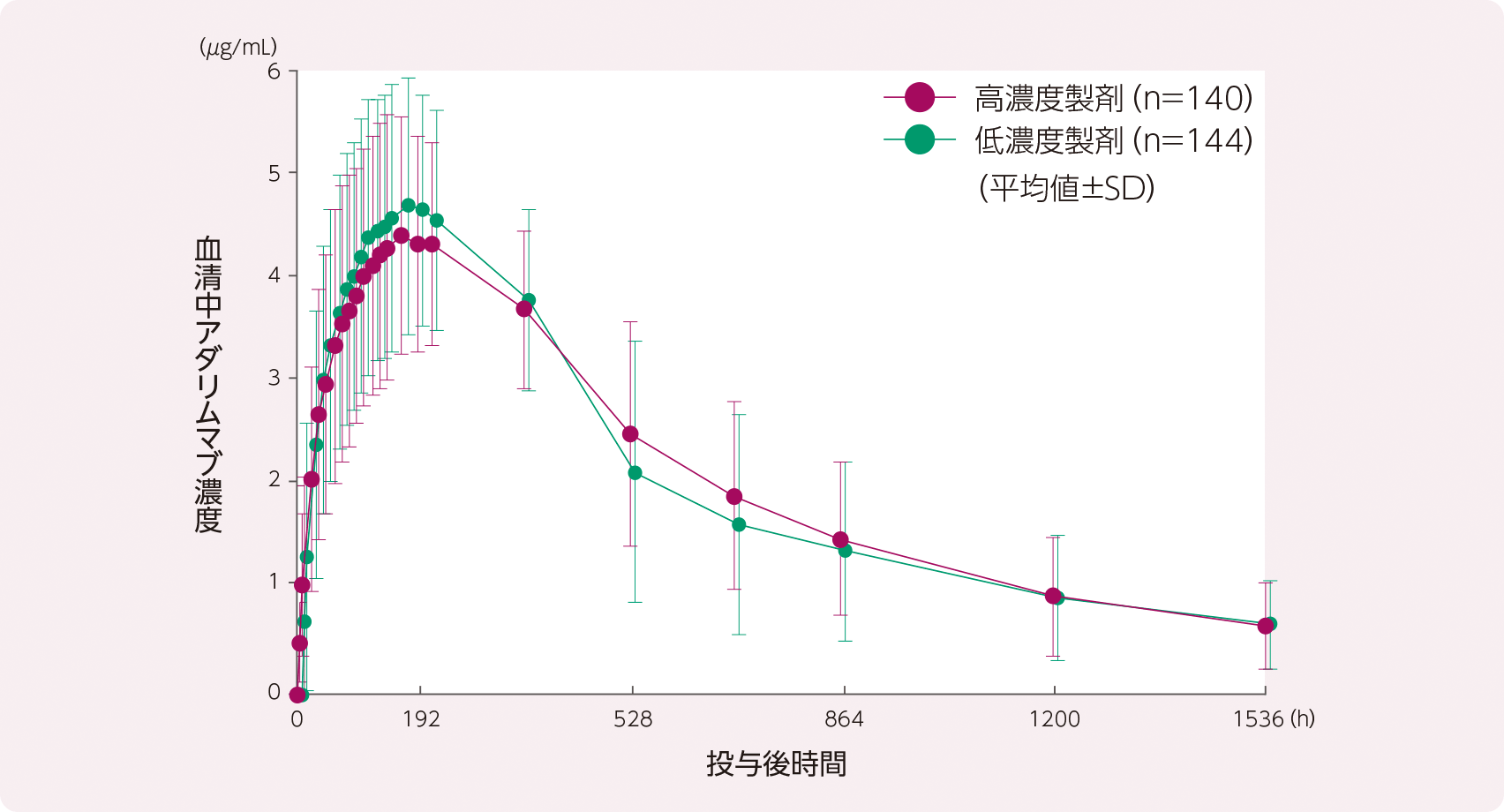
2. 国内生物学的同等性(BE)試験(健康成人)2)
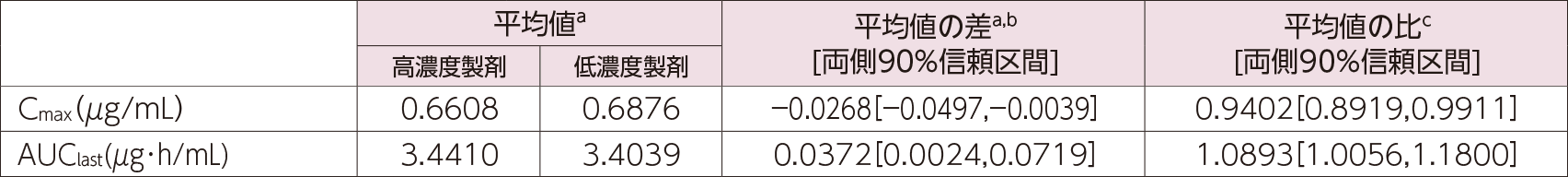
本剤の高濃度製剤(40mg/0.4mLシリンジ、発売製品の濃度)と低濃度製剤(40mg/0.8mLシリンジ)の生物学的同等性を検証することを目的として実施した。健康成人男性に高濃度製剤又は低濃度製剤1回40mgを単回皮下投与し、投与65日目までの薬物動態を評価した。Cmax及びAUClastの対数変換値の平均値の差(高濃度製剤群−低濃度製剤群)の両側90%信頼区間は、いずれも治験実施計画書で定めた同等性判定基準[log(0.80)~log(1.25)]の範囲に含まれ、両製剤の生物学的同等性が検証された。
- 平均値±SD
- 解析対象:生物学的同等性解析対象集団
- a:常用対数変換
- b:平均値の差=(高濃度製剤群の平均値)−(低濃度製剤群の平均値)
- c:平均値の比=10平均値の差
3. 関節リウマチ(RA)患者における薬物動態(2週に1回反復投与時)(外国人データ含む)
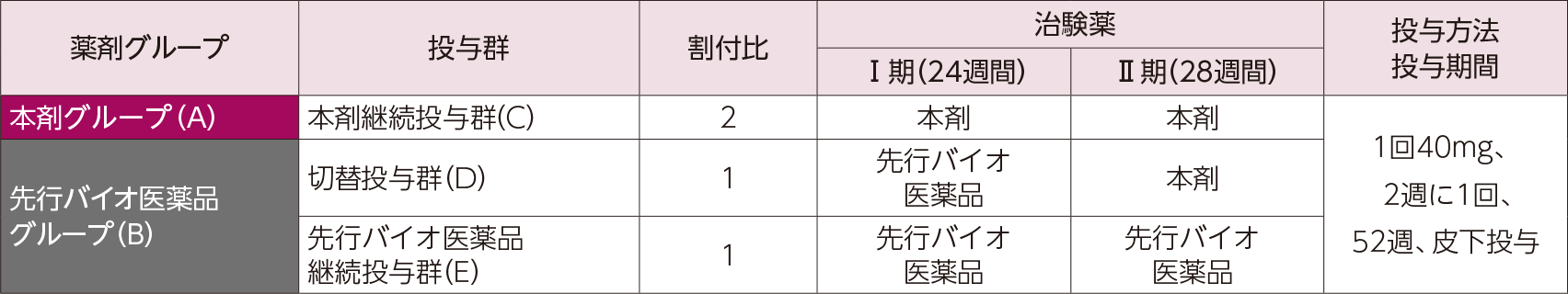
(1)国際共同第Ⅲ相試験3)
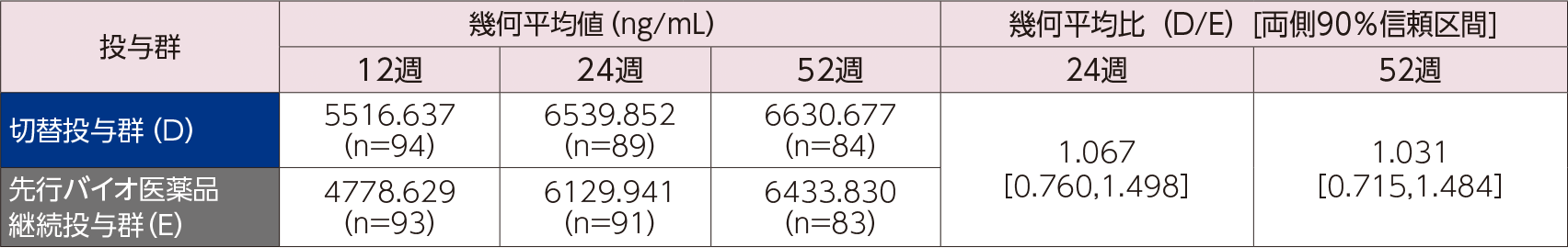
〈本剤グループと先行バイオ医薬品グループの比較〉
本剤グループと先行バイオ医薬品グループの投与開始24週時点における血清中トラフ濃度の幾何平均値、幾何平均比[両側90%信頼区間]は下表の通りで、血清中トラフ濃度は、両グループ間で大きく異ならないと考えられた。
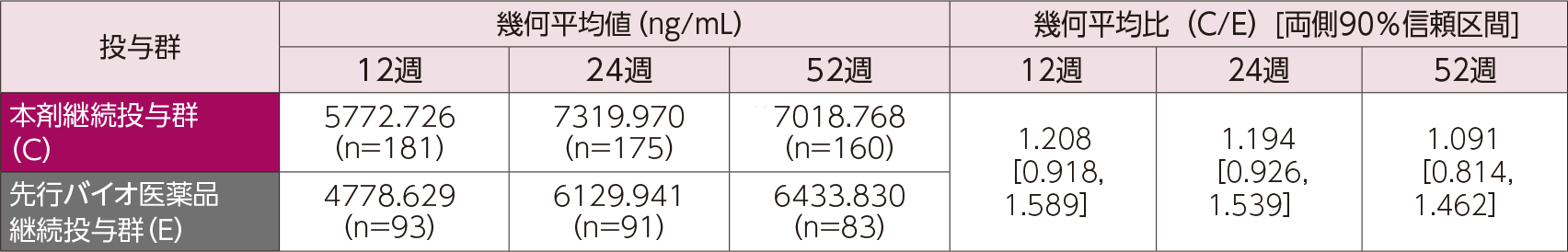
〈本剤継続投与群と先行バイオ医薬品継続投与群の比較〉
本剤継続投与群と先行バイオ医薬品継続投与群の血清中トラフ濃度の幾何平均値、投与開始12、24、52週時点における幾何平均比[両側90%信頼区間]は下表の通りで、血清中トラフ濃度は、両群間で大きく異ならないと考えられた。
- 1)持田製薬社内資料(海外第Ⅰ相試験)
- 2)持田製薬社内資料(生物学的同等性試験)
- 3)持田製薬社内資料(国際共同第Ⅲ相試験)(承認時評価資料)