- 医療関係者向けホーム
- 消化器領域
- リアルダ®錠
- Clinical Study:成人(各臨床試験での定義:16歳以上)の潰瘍性大腸炎患者に対する臨床成績:活動期 安全性
 Clinical Study
Clinical Study
成人(各臨床試験での定義:16歳以上)の潰瘍性大腸炎患者に対する臨床成績:活動期
安全性
投与期の有害事象の発現率は、リアルダ4800mg/日(1日1回)群では50.0%(70/140例)、pH依存型メサラジン放出調節製剤3600mg/日(1日3回)群では55.7%(78/140例)であった。
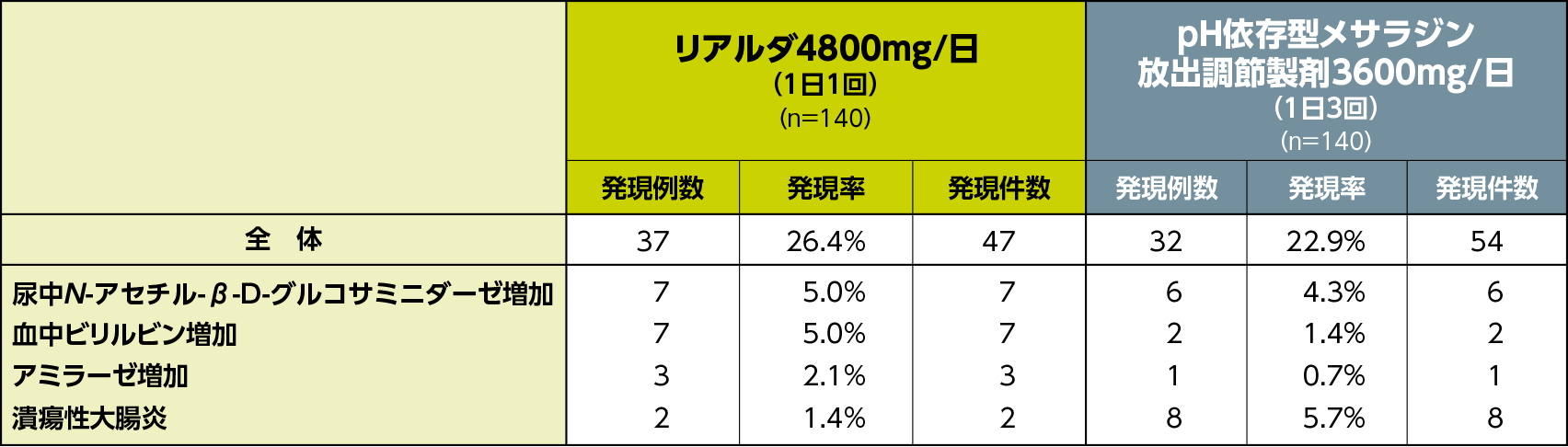
投与期の副作用の発現率は、リアルダ4800mg/日(1日1回)群では26.4%(37/140例)、pH依存型メサラジン放出調節製剤3600mg/日(1日3回)群では22.9%(32/140例)であり、主なもの(いずれかの群で発現率5%以上)は、尿中N-アセチル-β-D-グルコサミニダーゼ増加〔各群5.0%(7例)、4.3%(6例)〕、血中ビリルビン増加〔各群5.0%(7例)、1.4%(2例)〕、潰瘍性大腸炎〔各群1.4%(2例)、5.7%(8例)〕であった。
投与期の中止に至った副作用の発現率は、リアルダ4800mg/日(1日1回)群では3.6%(5/140例、5件)であり、潰瘍性大腸炎が2件、間質性肺疾患、器質化肺炎および肝機能異常は1件ずつ、pH依存型メサラジン放出調節製剤3600mg/日(1日3回)群では7.1%(10/140例、12件)であり、潰瘍性大腸炎が7件、突発性難聴、心筋炎、血中カリウム増加、γ-グルタミルトランスフェラーゼ増加および血中アルカリホスファターゼ増加はいずれも1件ずつであった。
投与期の重篤な副作用は、リアルダ4800mg/日(1日1回)群では間質性肺疾患および器質化肺炎が1例1件ずつ、pH依存型メサラジン放出調節製剤3600mg/日(1日3回)群では潰瘍性大腸炎2例2件および心筋炎1例1件であった。
本試験において、死亡例は認められなかった。
2025年12月作成
14407-18/N14 B8 MDC