- 医療関係者向けホーム
- 循環器領域
- エパデールEM
- Clinical Study:国内第Ⅲ相長期投与試験 安全性
 Clinical Study国内第Ⅲ相長期投与試験
Clinical Study国内第Ⅲ相長期投与試験
安全性
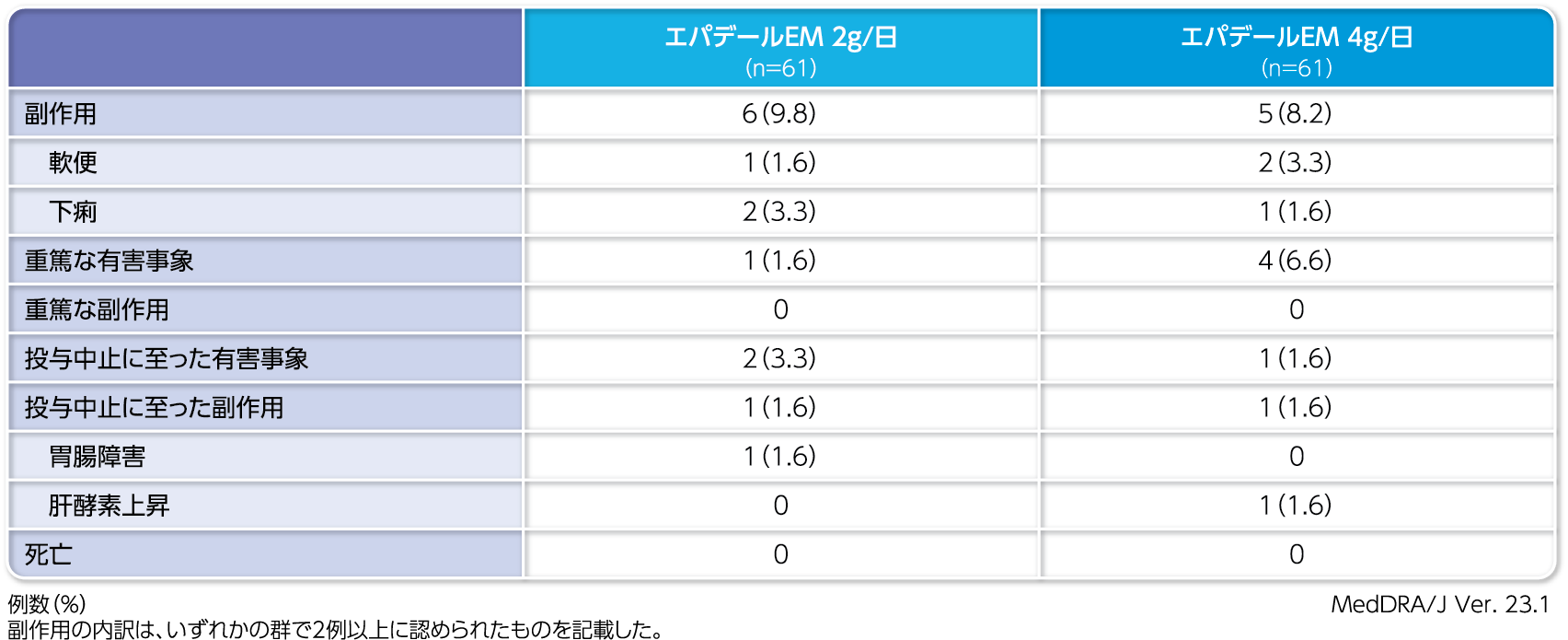
【有害事象:主要評価項目、副作用:副次評価項目】(安全性解析対象集団)
有害事象の発現率は、エパデールEM 2g/日群70.5%(43/61例)、4g/日群62.3%(38/61例)でした。