- 医療関係者向けホーム
- 循環器領域
- ユリス®錠
- Pick Up
- メタボリックシンドローム(MetS)と血清尿酸値の関連(テキスト版)
 Pick Up
Pick Up
2020年08月06日公開(2021年9月30日一部改訂)
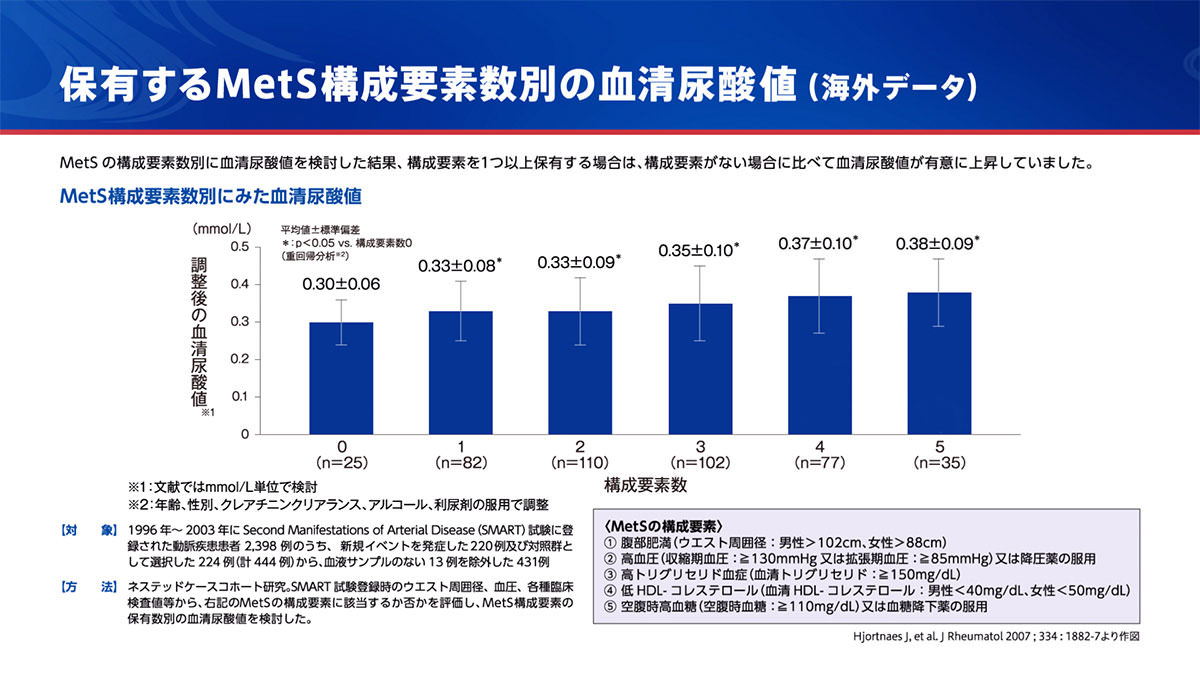
メタボリックシンドローム(MetS)は高尿酸血症と高い頻度で合併することが知られており、その背景の1つとして、インスリン抵抗性の存在が挙げられています。インスリン抵抗性は高インスリン血症を招き、間接的に腎臓の近位尿細管に存在する尿酸トランスポーターであるURAT1による尿酸の再吸収を亢進させることがあると考えられています1)。
2020年5月に発売となったユリス®錠は、URAT1を介した尿酸の再吸収経路を阻害して、血清尿酸値を低下させる、選択的尿酸再吸収阻害薬(SURI)です。
今回は「メタボリックシンドローム(MetS)と血清尿酸値の関連」についてご紹介します。
- 1)Kakutani-Hatayama M, et al. Am J Lifestyle Med 2017;11:321-9
- メタボリック
シンドロームとは - メタボリック
シンドロームと
血清尿酸値の関連 - 高尿酸血症の要因の
1つとしての
インスリン抵抗性 - ユリス®錠のSURI
としての作用機序 - ユリス®錠の
BMI別にみた
血清尿酸値低下作用
メタボリックシンドロームと血清尿酸値の関連-海外の動脈疾患患者対象研究より-
高尿酸血症の要因の1つとしてのインスリン抵抗性
ユリス®錠のSURIとしての作用機序
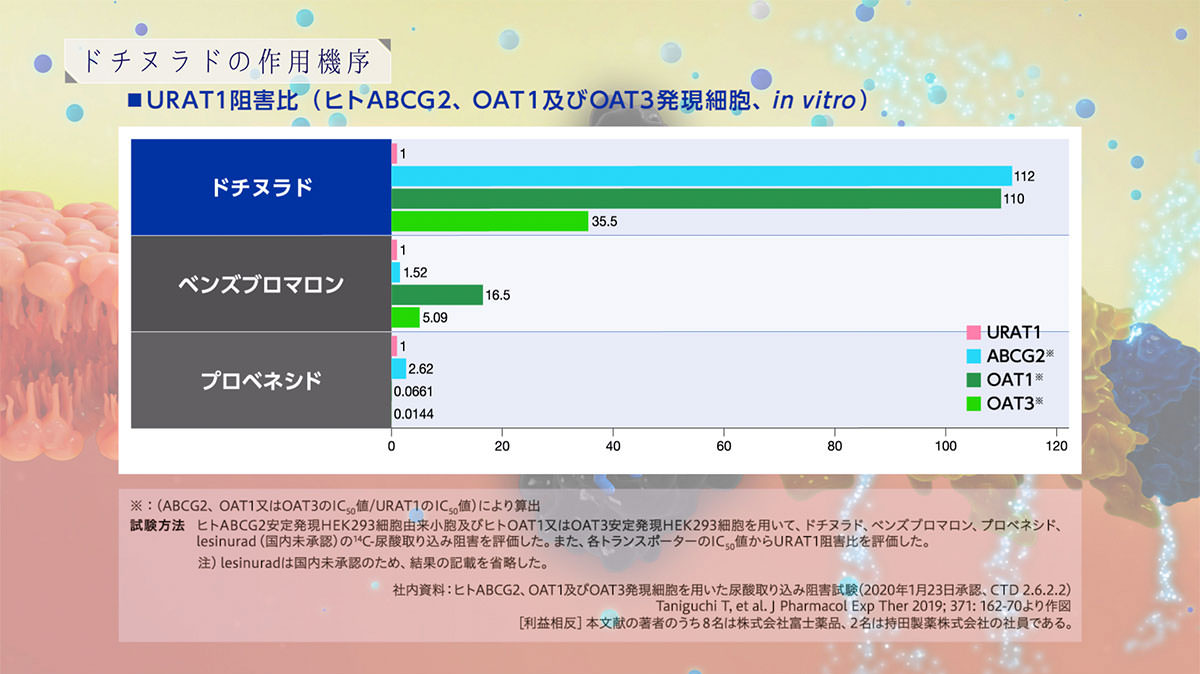
ユリス®錠(ドチヌラド)は、URAT1選択性が高く、ABCG2、OAT1、OAT3を介した尿酸分泌経路は阻害せず、URAT1を介した再吸収経路を阻害する選択的尿酸再吸収阻害薬(SURI)です。
ドチヌラドの作用機序
ドチヌラドは、URAT1選択性が高く、 ABCG2、OAT1、OAT3を介した尿酸の分泌経路には影響を及ぼさず、URAT1を介した尿酸の再吸収経路を抑制し、効率的に血清尿酸値を低下させることが期待されます。
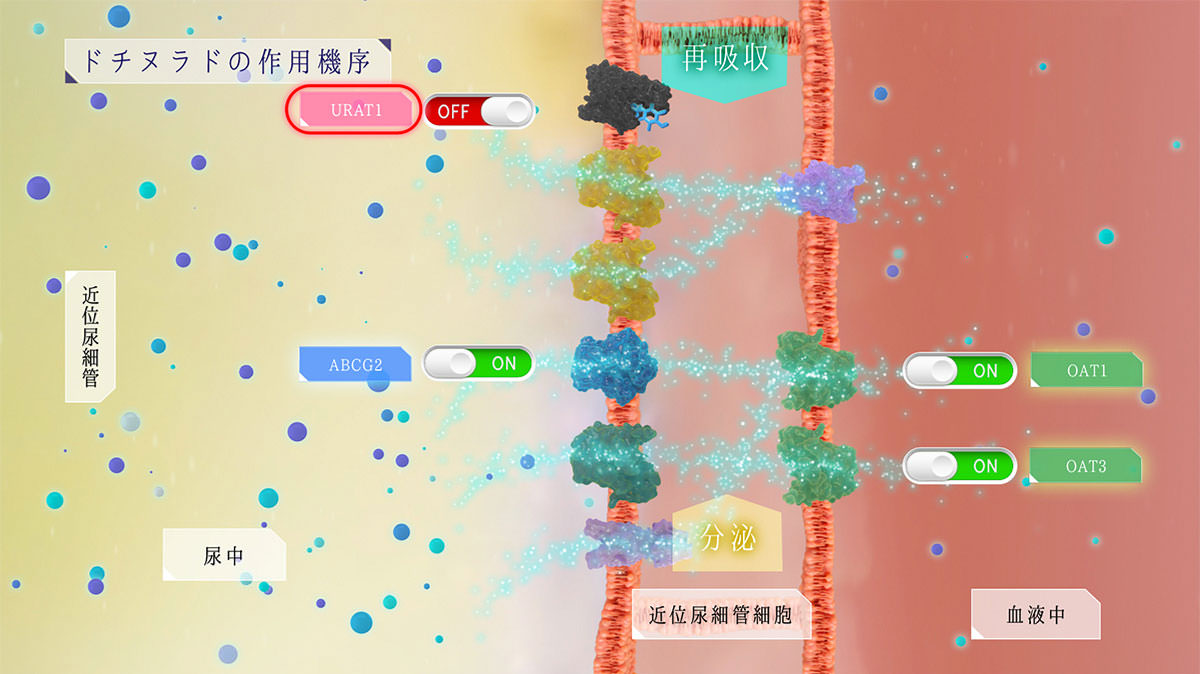
また、腸管においても、 ABCG2を介した尿酸の分泌には影響を及ぼさず、腸管排泄への影響が少ない可能性があります。

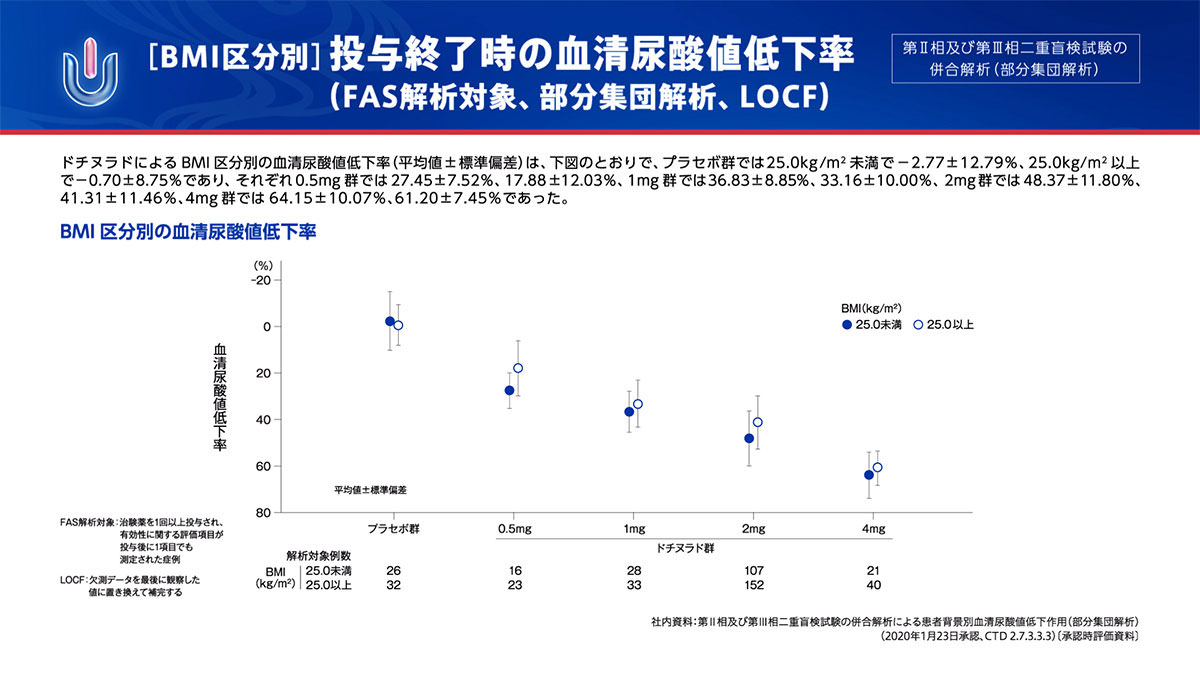
ユリス®錠のBMI別にみた血清尿酸値低下作用
「禁忌を含む使用上の注意」等は添付文書をご参照ください。
第Ⅱ相及び第Ⅲ相二重盲検試験の
併合解析(部分集団解析)
併合解析には一部承認外の成績が含まれますが、
承認時に評価された資料であるため掲載します。
- 社内資料:第Ⅱ相及び第Ⅲ相二重盲検試験の併合解析による患者背景別血清尿酸値低下作用(部分集団解析)(2020年1月23日承認、CTD 2.7.3.3.3)〔承認時評価資料〕
- 社内資料:臨床試験(二重盲検試験の併合)の有害事象の解析(2020年1月23日承認、CTD 2.7.4.2.1)〔承認時評価資料〕
[BMI区分別]投与終了時の血清尿酸値低下率
(FAS解析対象、部分集団解析、LOCF)
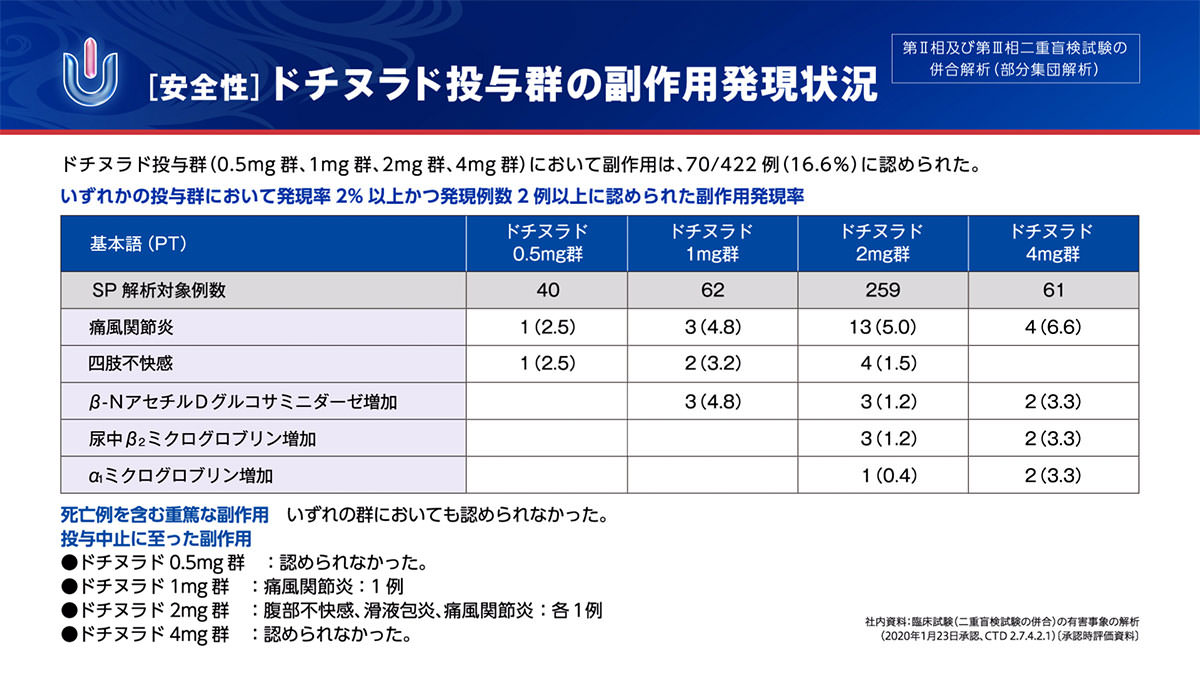
安全性:副作用発現状況
ドチヌラド投与群(0.5mg群、1mg群、2mg群、4mg群)において副作用は、70/422例(16.6%)に認められました。
いずれかの投与群において発現率2%以上かつ発現例数2例以上に認められた副作用は、痛風関節炎[0.5mg群:1/40例(2.5%)、1mg群:3/62例(4.8%)、2mg群:13/259例(5.0%)、4mg群:4/61例(6.6%)]、四肢不快感[0.5mg群:1/40例(2.5%)、1mg群:2/62例(3.2%)、2mg群:4/259例(1.5%)]、β-NアセチルDグルコサミニダーゼ増加[1mg群:3/62例(4.8%)、2mg群:3/259例(1.2%)、4mg群:2/61例(3.3%)]、尿中β2ミクログロブリン増加[2mg群:3/259例(1.2%)、4mg群:2/61例(3.3%)]、α1ミクログロブリン増加[2mg群:1/259例(0.4%)、4mg群:2/61例(3.3%)]でした。
本試験のドチヌラド投与群において死亡例及び重篤な副作用は認められませんでした。また、ドチヌラドを投与中止に至った副作用は、1mg群に痛風関節炎が1例、2mg群に腹部不快感、滑液包炎、痛風関節炎がそれぞれ1例に認められました。
【用法及び用量】
通常、成人にはドチヌラドとして1日0.5mgより開始し、1日1回経口投与する。その後は血中尿酸値を確認しながら必要に応じて徐々に増量する。維持量は通常1日1回2mgで、患者の状態に応じて適宜増減するが、最大投与量は1日1回4mgとする。
コンテンツ評価にご協力をお願いいたします。
このコンテンツは参考になりましたでしょうか?
ご回答ありがとうございます。
マイページ設定により、先生のご興味のある領域/製品の最新情報を
効率的にチェックすることができます!
今後のコンテンツ改善のために、
「参考にならなかった」理由を
教えてください。
(複数回答可)

引き続き、持田製薬 医療関係者向けサイトを
よろしくお願いいたします。