- 医療関係者向けホーム
- 循環器領域
- トラムセット®
- Information:安全性
 Information
Information
安全性
<承認時>
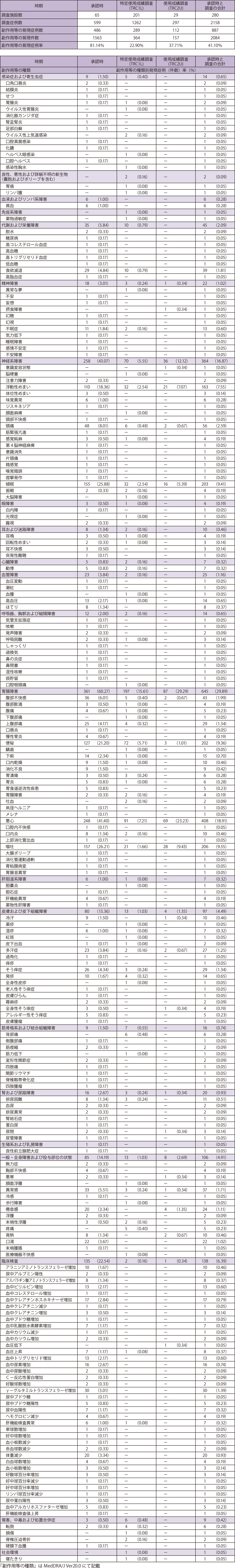
慢性疼痛及び抜歯後疼痛を有する患者を対象に実施した国内臨床試験1)、2)、3)における安全性評価対象症例599例中486例(81.1%)に副作用(臨床検査値異常を含む)が認められた。主なものは、悪心248例(41.4%)、嘔吐157例(26.2%)、傾眠155例(25.9%)、便秘127例(21.2%)、浮動性めまい113例※(18.9%)であった。
- ※副作用一覧の「浮動性めまい」と「体位性めまい」を合計した例数
<再審査終了時>
慢性疼痛を対象とした特定使用成績調査における副作用(臨床検査値異常を含む)は1262例中289例(22.9%)に認められた。主な副作用は、悪心91例(7.2%)、便秘72例(5.7%)、浮動性めまい32例(2.5%)、傾眠32例(2.5%)、嘔吐21例(1.7%)であった。
抜歯後疼痛を対象とした使用成績調査における副作用(臨床検査値異常を含む)は297例中112例(37.7%)に認められた。主な副作用は、悪心69例(23.2%)、嘔吐28例(9.4%)、浮動性めまい21例(7.1%)、傾眠16例(5.4%)、倦怠感4例(1.4%)、便秘3例(1.0%)であった。
- 1)トラムセット®配合錠国内第Ⅲ相臨床試験(JNS013-JPN-04)(社内資料:承認時評価資料)
- 2)トラムセット®配合錠国内第Ⅲ相臨床試験(JNS013-JPN-05)(社内資料:承認時評価資料)
- 3)トラムセット®配合錠国内第Ⅱ/Ⅲ相臨床試験(JNS013-JPN-03)(社内資料:承認時評価資料)