- 医療関係者向けホーム
- 循環器領域
- ユリス®錠
- Clinical Study:第Ⅲ相試験(フェブキソスタット対照非劣性試験) 血清尿酸値低下率
 Clinical Study第Ⅲ相試験(フェブキソスタット対照非劣性試験)
Clinical Study第Ⅲ相試験(フェブキソスタット対照非劣性試験)
血清尿酸値低下率
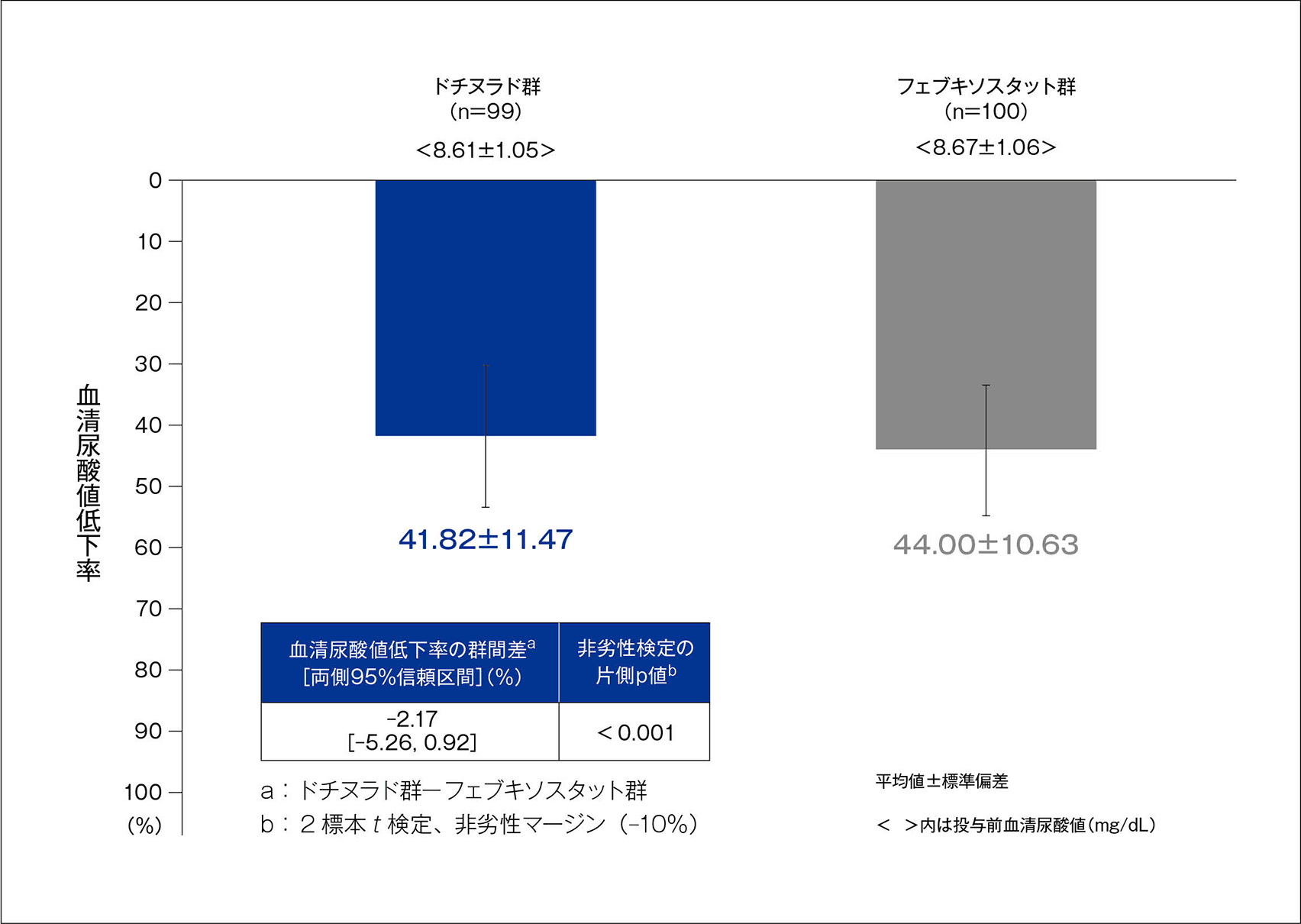
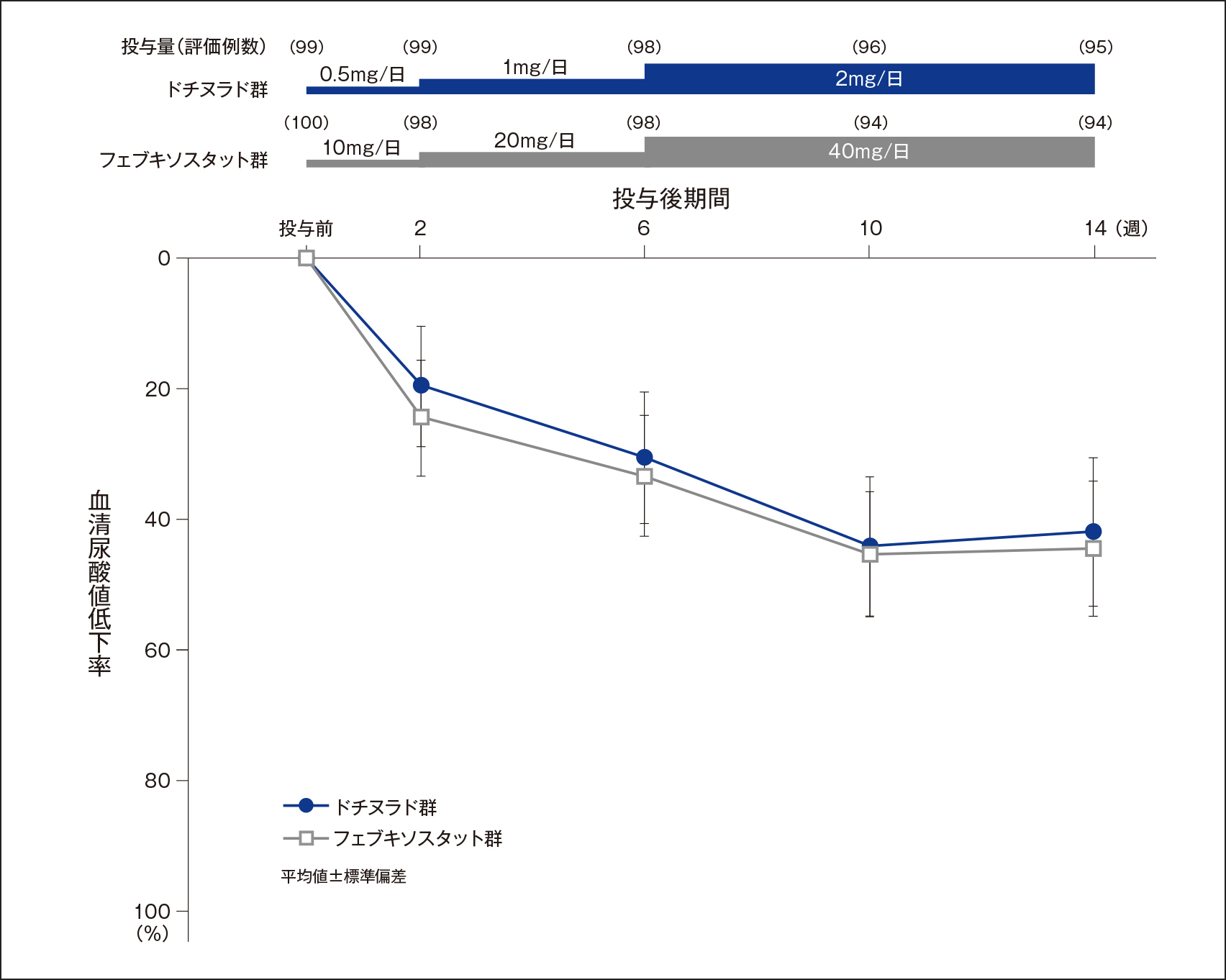
投与終了時の血清尿酸値低下率(主要評価項目;FAS解析対象、LOCF)検証的解析結果
投与終了時における投与前値からの血清尿酸値低下率(平均値±標準偏差)は、ドチヌラド群で41.82±11.47%、フェブキソスタット群で44.00±10.63%であった。
血清尿酸値低下率の投与群間の平均値の差は-2.17%[両側95%信頼区間:-5.26%,0.92%]であり、両側95%信頼区間の下限値が非劣性マージン(-10%)を上回ったため、フェブキソスタット群に対するドチヌラド群の非劣性が検証された。