- 医療関係者向けホーム
- 循環器領域
- トレプロスト®注射液
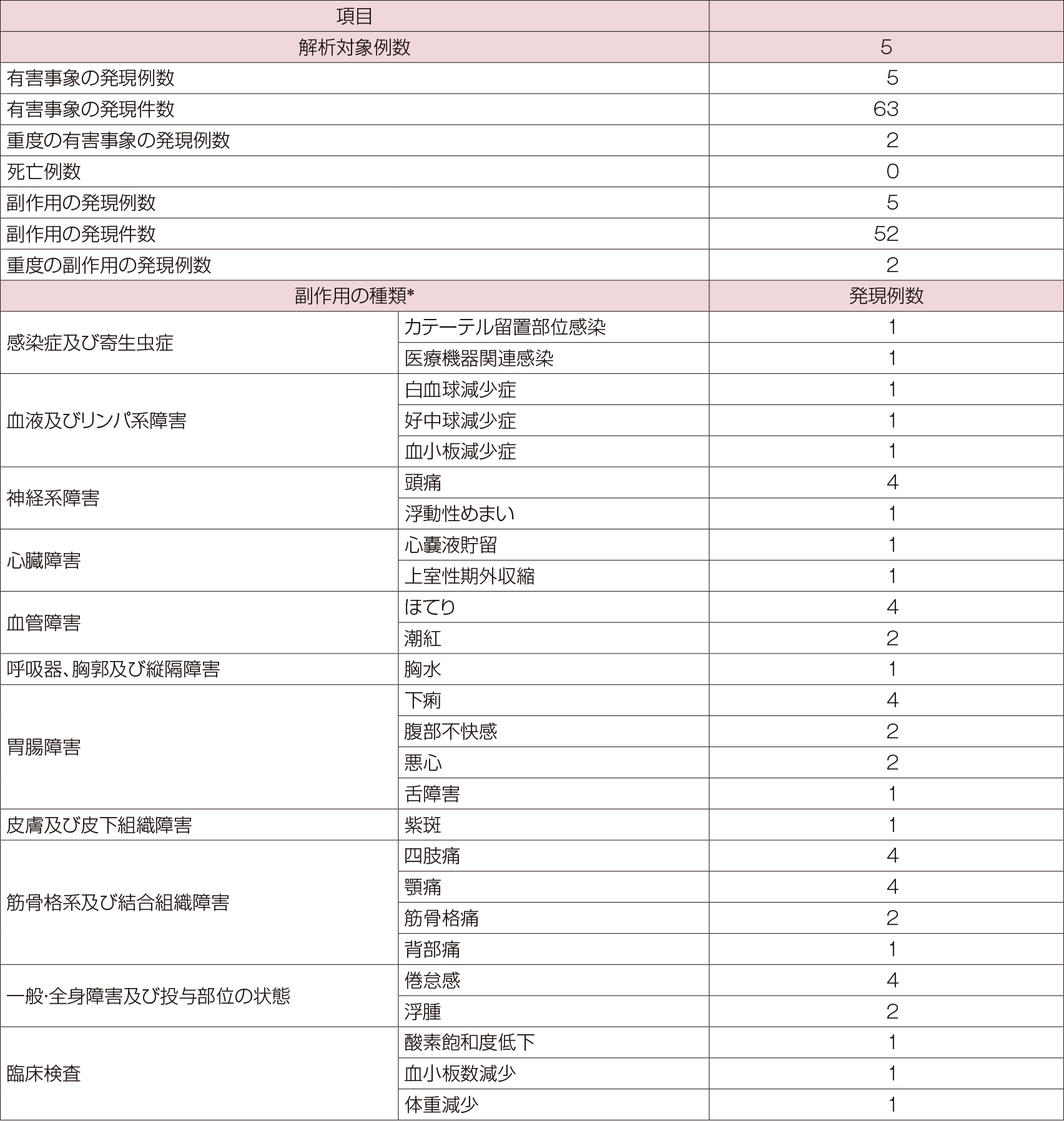
- Clinical Study:国内第Ⅱ/Ⅲ相追加試験(静脈内投与試験) 安全性
医療関係者向けサイト
ご利用の注意
・このサイトに掲載している情報は、弊社医療用医薬品を適正にご使用いただくためのものであり、広告を目的とするものではありません。
・日本国内の医療関係者(医師、薬剤師等)を対象としております。
国外の医療関係者、一般の方に対する情報提供を目的としたものではありませんので、ご了承ください。
・このサイトで提供している以外の弊社医療用医薬品の情報をお求めの方は、弊社MR、またはくすり相談窓口までお問い合わせください。
会員限定コンテンツのご利用について
会員の方
会員限定コンテンツのご利用には
medパスIDが必要となります。
-
でログイン
※外部サイトへ移動します
-
新規会員登録はこちら
※外部サイトへ移動します
medパスのご紹介はこちら
医療関係者ではない方(コーポレートサイトへ)
医療関係者向けサイト
ご利用の注意
・このサイトに掲載している情報は、弊社医療用医薬品を適正にご使用いただくためのものであり、広告を目的とするものではありません。
・日本国内の医療関係者(医師、薬剤師等)を対象としております。
国外の医療関係者、一般の方に対する情報提供を目的としたものではありませんので、ご了承ください。
・このサイトで提供している以外の弊社医療用医薬品の情報をお求めの方は、弊社MR、またはくすり相談窓口までお問い合わせください。
医療関係者ではない方(コーポレートサイトへ)
このコンテンツは役に立ちましたでしょうか?
ご回答いただき
ありがとうございます
引き続き、持田製薬医療関係者向け
サイトをご利用ください
ログアウトします。
よろしいですか?
先生
新規会員登録ありがとうございます。
「持田製薬株式会社 医療関係者向けサイト」は日本国内の医療関係者(医師、薬剤師、看護師等)を対象に製品情報、お役立ち情報等をお届けします。
メールアドレス
希望する領域または製品にチェックをいれてください。