- 医療関係者向けホーム
- 循環器領域
- ユリス®錠
- Clinical Study:第Ⅲ相試験(長期投与試験) ドチヌラド2mgから4mgへ増量後の成績
 Clinical Study第Ⅲ相試験(長期投与試験)
Clinical Study第Ⅲ相試験(長期投与試験)
ドチヌラド2mgから4mgへ増量後の成績
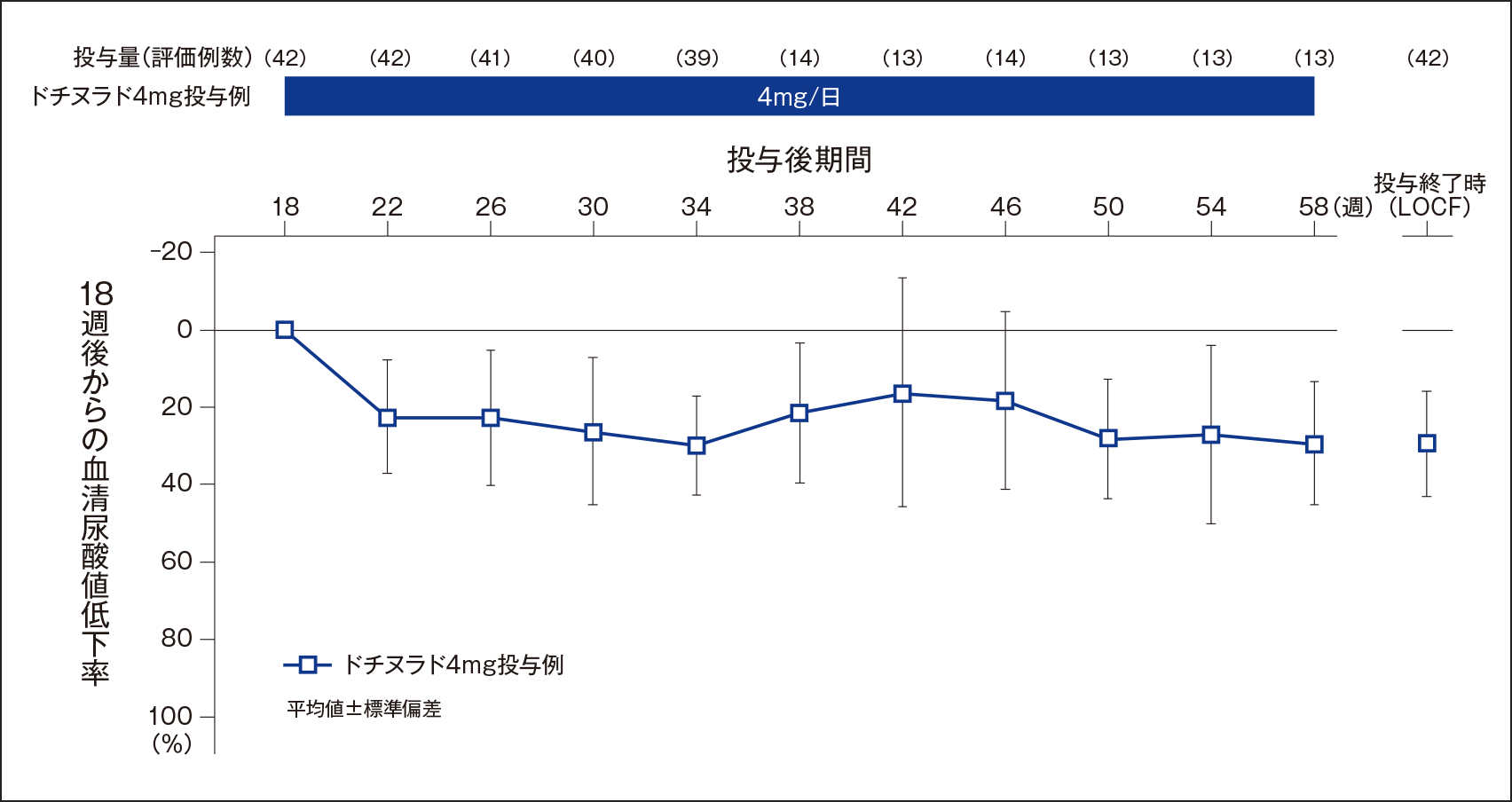
ドチヌラド4mg投与例における、投与18週後から各時点及び投与終了時の血清尿酸値低下率
(副次評価項目;FAS解析対象)
ドチヌラド4mg投与例では、各時点(投与22週後以降、58週後まで4週ごと)及び投与終了時における投与18週後からの血清尿酸値低下率(平均値±標準偏差)は、下図のとおりに推移し、投与58週後では29.02±15.96%であった。
投与18週後との比較において、投与42週後では有意差が認められなかったが(名目上のp=0.075、1標本t検定)、その他の時点では有意差が認められた[名目上のp=0.011(投与46週後)、名目上のp=0.001(投与54週後)、名目上のp<0.001(それ以外の時点及び投与終了時)、1標本t検定]。
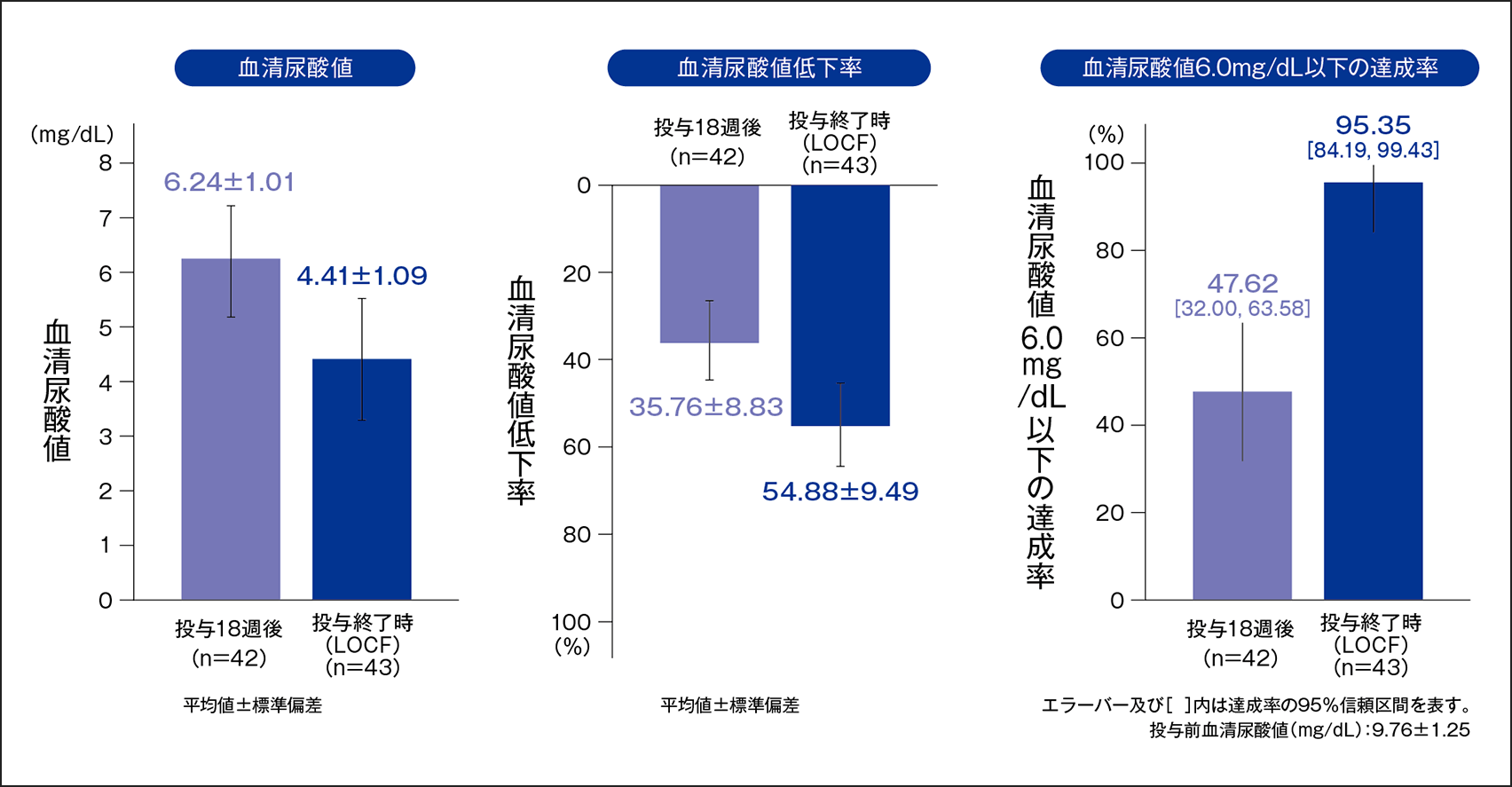
ドチヌラド4mg投与例における、投与18週後と投与終了時における血清尿酸値、血清尿酸値低下率、血清尿酸値6.0mg/dL以下の達成率(副次評価項目;FAS解析対象)
ドチヌラド4mg投与例において、血清尿酸値(平均値±標準偏差)は投与18週後6.24±1.01mg/dLに対して投与終了時4.41±1.09mg/dL、血清尿酸値低下率(平均値±標準偏差)は投与18週後35.76±8.83%に対して投与終了時54.88±9.49%、血清尿酸値6.0mg/dL以下の達成率[95%信頼区間]は投与18週後47.62%[32.00%,63.58%]に対して投与終了時95.35%[84.19%,99.43%]であった。