- 医療関係者向けホーム
- 消化器領域
- グーフィス®錠5mg
- Clinical Study:国内第Ⅲ相試験 完全自発排便回数
 Clinical Study国内第Ⅲ相試験
Clinical Study国内第Ⅲ相試験
完全自発排便回数
副次評価項目
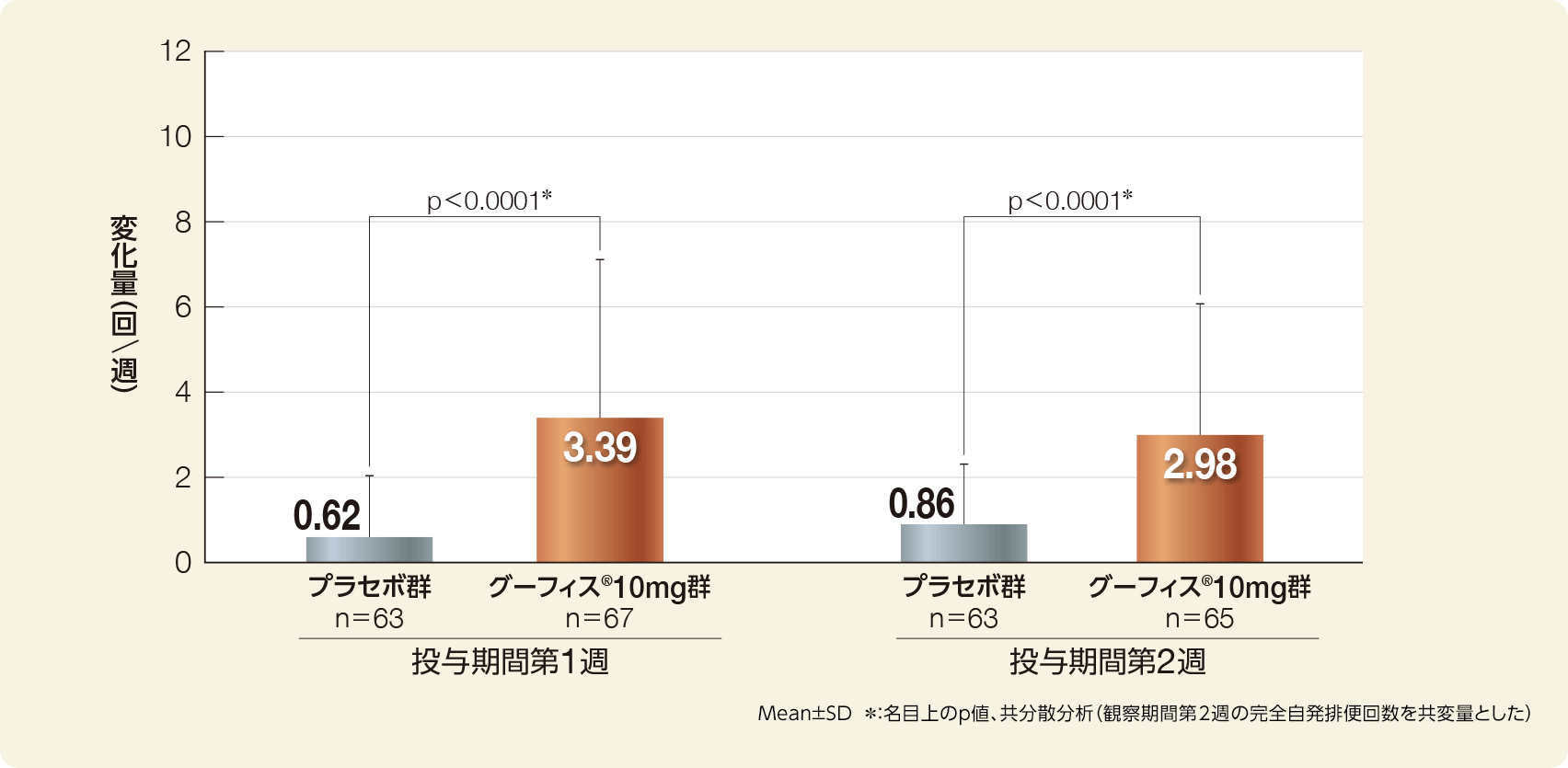
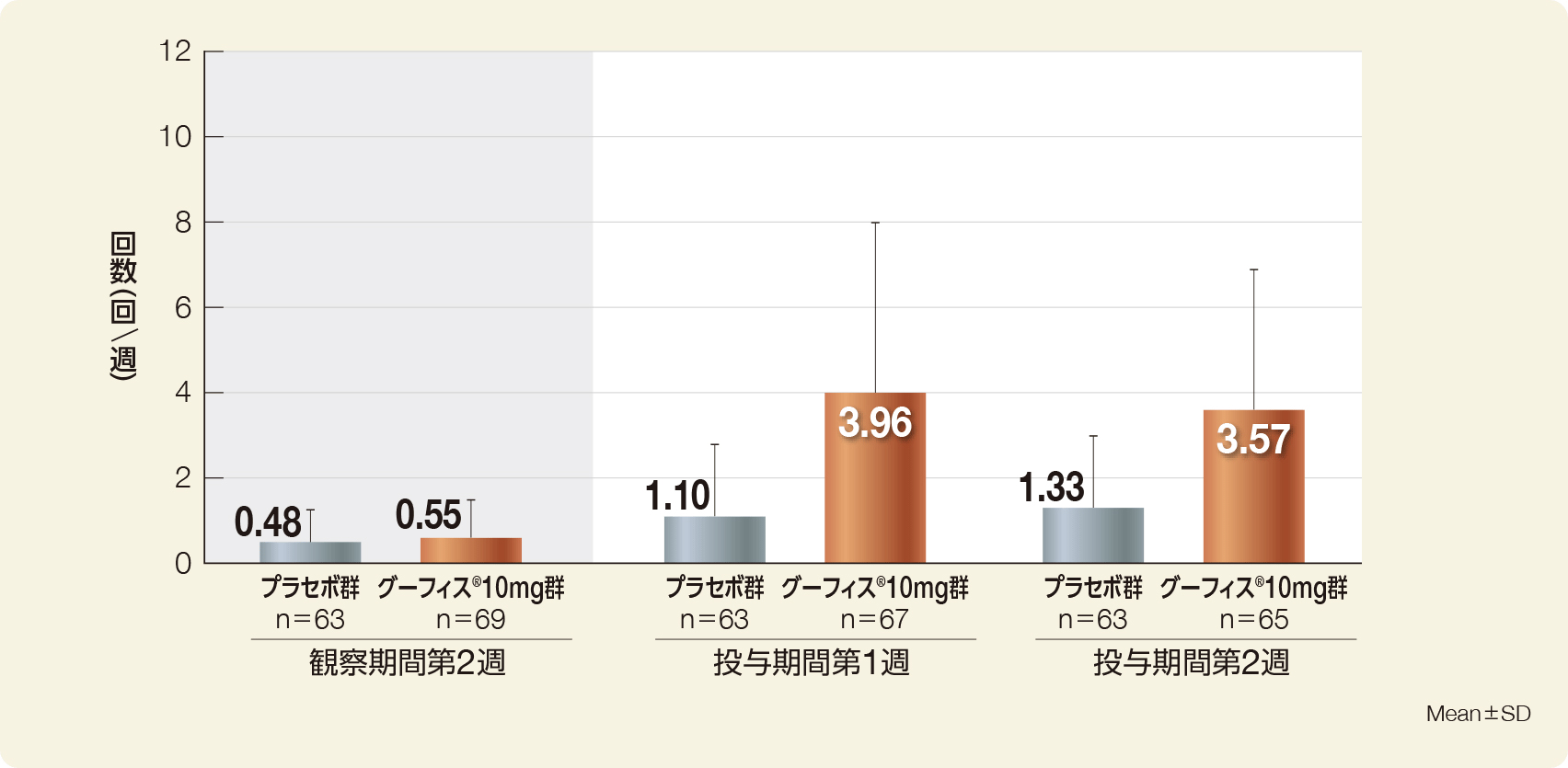
完全自発排便回数の変化量(観察期間第2週 vs. 投与期間第1週・第2週)(FAS)
投与期間第1週の完全自発排便回数の観察期間第2週からの変化量(Mean±SD)は、プラセボ群0.62±1.44回、グーフィス®群3.39±3.86回、投与期間第2週の完全自発排便回数の観察期間第2週からの変化量は、プラセボ群0.86±1.45回、グーフィス®群2.98±3.10回で、グーフィス®群は投与期間第1週及び第2週いずれにおいても、プラセボ群に対して完全自発排便回数の変化量の有意な増加が認められた(投与期間第1週、第2週ともにp<0.0001、名目上のp値、共分散分析)。