- 医療関係者向けホーム
- 消化器領域
- グーフィス®錠5mg
- Clinical Study:国内第Ⅲ相試験 便硬度・重症度
 Clinical Study国内第Ⅲ相試験
Clinical Study国内第Ⅲ相試験
便硬度・重症度
副次評価項目
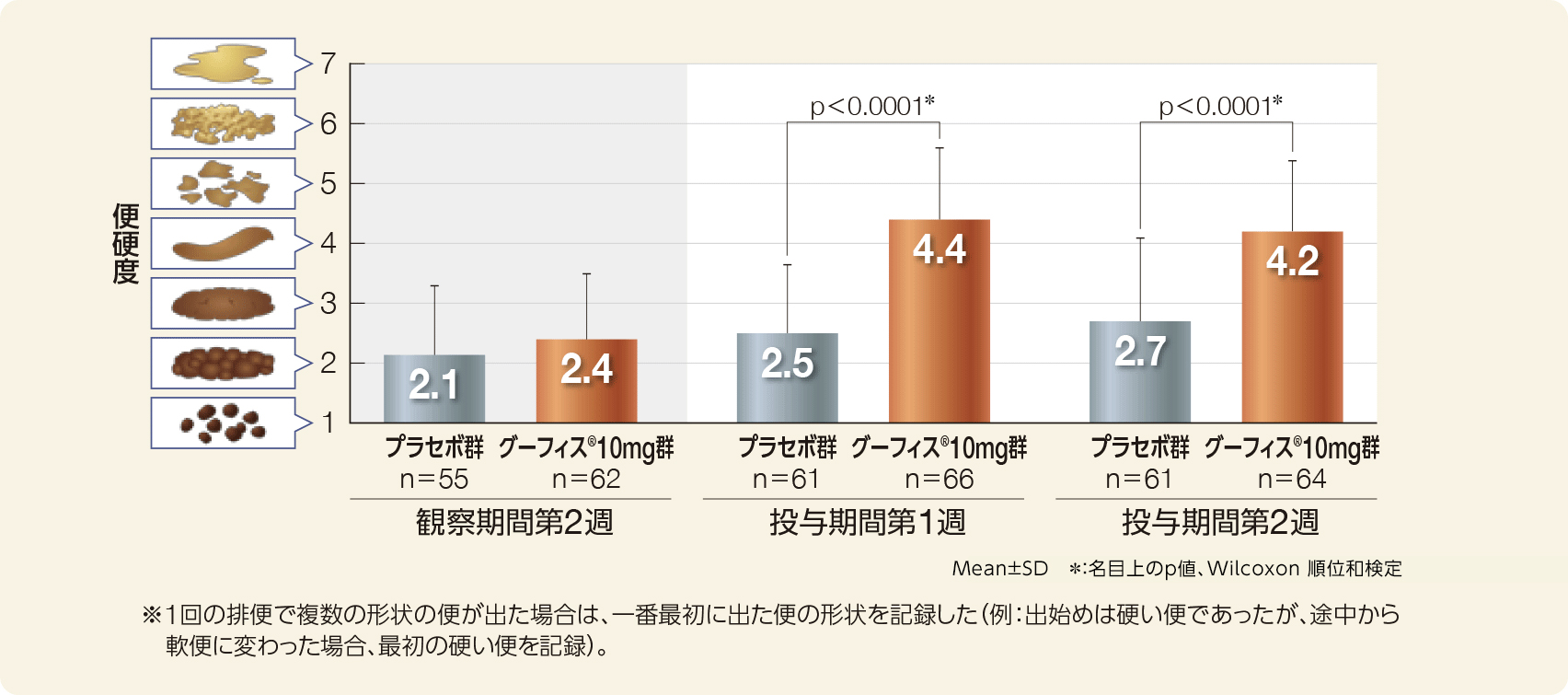
Bristol便形状スケールに基づいた便硬度(FAS)
Bristol便形状スケールの1週間あたりの中央値(Mean±SD)は、観察期間第2週においてプラセボ群2.1±1.2、グーフィス®群2.4±1.1、投与期間第1週においてプラセボ群2.5±1.2、グーフィス®群4.4±1.3、投与期間第2週においてプラセボ群2.7±1.4、グーフィス®群4.2±1.2であり、投与期間第1週、第2週ともグーフィス®群のBristol便形状スケールに基づいた便硬度の中央値はプラセボ群に対して有意に大きかった(投与期間第1週、第2週ともにp<0.0001、名目上のp値、Wilcoxon 順位和検定)。
「Bristol 便形状スケール」についてはこちらをご参照ください。
副次評価項目
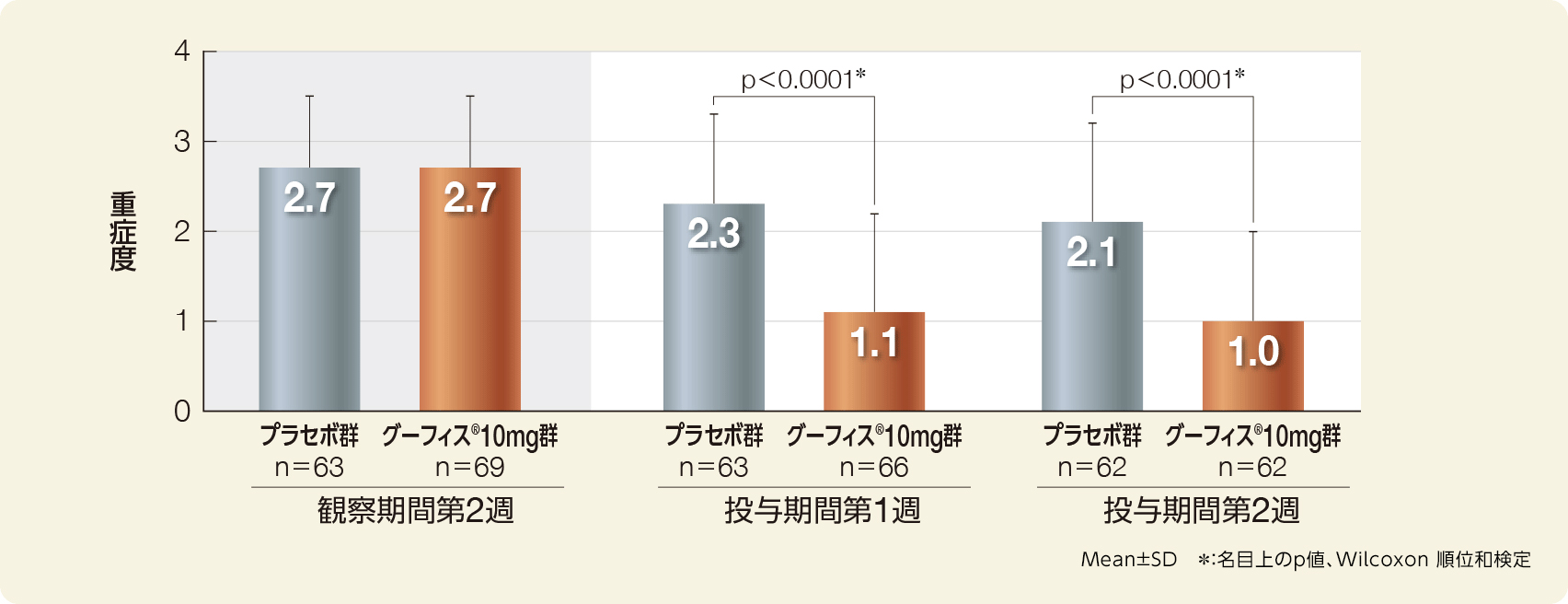
便秘の重症度評価(FAS)
便秘の重症度(Mean±SD)は、観察期間第2週においてプラセボ群2.7±0.8、グーフィス®群2.7±0.8、投与期間第1週においてプラセボ群2.3±1.0、グーフィス®群1.1±1.1、投与期間第2週においてプラセボ群2.1±1.1、グーフィス®群1.0±1.0であり、投与期間第1週、第2週ともにグーフィス®群の便秘の重症度評価はプラセボ群に対して有意に低かった(投与期間第1週、第2週ともにp<0.0001、名目上のp値、Wilcoxon 順位和検定)。
「便秘の重症度」についてはこちらをご参照ください。