- 医療関係者向けホーム
- 循環器領域
- エパデールS/カプセル
- Clinical Study:高脂血症に対する効果(冠動脈疾患を有する脂質異常症患者) 試験の概要
 Clinical Study高脂血症に対する効果(冠動脈疾患を有する脂質異常症患者)
Clinical Study高脂血症に対する効果(冠動脈疾患を有する脂質異常症患者)
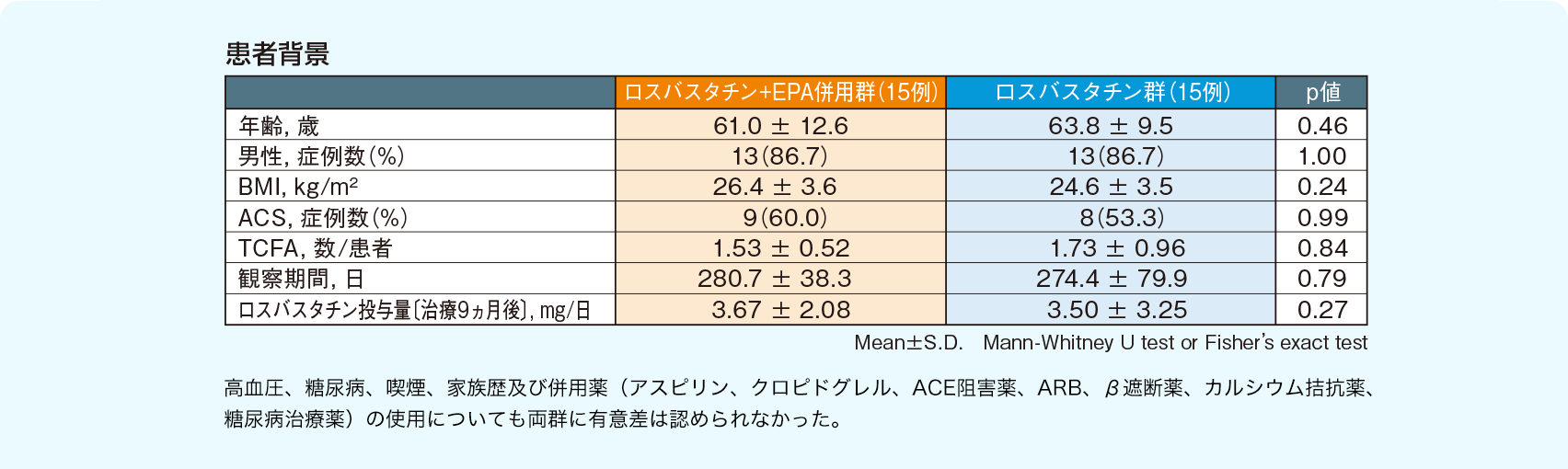
試験の概要「高脂血症に対する効果(冠動脈疾患を有する脂質異常症患者)」
- Nishio R. et al. Atherosclerosis 2014 ; 234 : 114-119
「禁忌を含む注意事項等情報」等は電子添文をご参照ください。
試験デザイン
ランダム化オープンラベル群間比較試験
目的
脂質異常症患者におけるスタチン+EPA併用療法が血清脂質、EPA/AA比及び不安定プラークに及ぼす影響などを検討した。
対象
安定狭心症、あるいは急性冠症候群(ACS)により経皮的冠動脈インターベンション(PCI)を施行した脂質異常症患者のうち、LDL-コレステロール値>100mg/dLで、かつ光干渉断層撮影(OCT)によってTCFA※が認められた30例
投与方法
ロスバスタチン+EPA併用群とロスバスタチン群の2群に分け(各15例)、ロスバスタチン+EPA併用群に高純度EPA製剤1,800mg/日を、また両群にロスバスタチン(LDL-コレステロール値が70mg/dL未満となるよう用量調節)を、それぞれ9ヵ月間投与した。
評価項目
- 有効性評価項目(治療開始時と治療9ヵ月後):血清脂質、OCTによるプラークの線維性被膜厚、脂質領域の円弧角度及び長さなど
- 安全性評価項目:PCI施行後18ヵ月間の死亡、心筋梗塞、ステント内再狭窄及び標的あるいは非標的プラークにおける血行再建術の有無
- その他の評価項目:EPA/AA比
Limitation
連続的な侵襲的画像研究のため患者数が少ない。ロスバスタチンとEPAの組み合わせのみで検討を行い、他のスタチンや脂質低下療法と比較していない。OCT所見を病理組織学的所見により検証していない。OCTカテーテルから照射される赤外線は1~3mmしか血管壁に侵入できず、脂質が豊富なプラークを通過することができないため、不安定プラークの重要な特徴であるポジティブリモデリングの存在を評価することができなかった。