- 医療関係者向けホーム
- 循環器領域
- エパデールS/カプセル
- Pick Up
- CHERRY STUDY
 Pick Up
Pick Up
2019年06月11日公開(2023年8月23日一部改訂)
-
監修:渡邉 哲(山形大学医学部 内科学第一(循環・呼吸・腎臓内科学) 准教授)
「禁忌を含む注意事項等情報」等は電子添文をご参照ください。
試験概要
- 試験デザイン
-
前向き無作為化・非盲検・多施設共同・並行群間比較試験
- 目的
-
冠動脈疾患患者の高コレステロール血症に対し、高用量ピタバスタチン(PTV)に高純度EPA製剤(エパデール)を追加投与することによる脂質パラメータの変化と冠動脈プラークの退縮および安定化に及ぼす影響を評価する。
- 対象
-
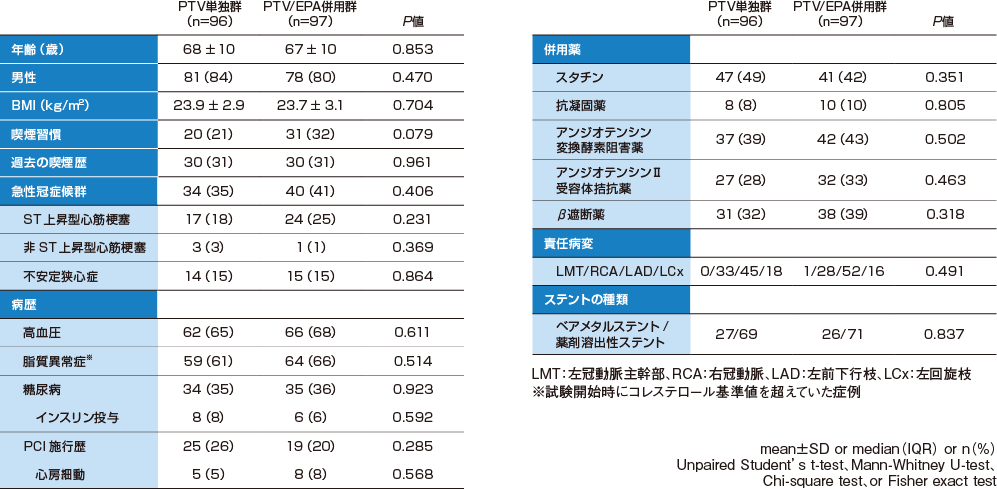
下記の基準を満たした238例を対象とした。
組入れ基準
- ①臨床試験の参加に関する詳細な説明を受け、書面による同意を得た症例
- ②同意時に20歳以上であった症例
- ③高コレステロール血症症例。その定義は(1)総コレステロール(TC)220mg/dL以上、(2)LDL-コレステロール(LDL-C)140mg/dL以上、(3)LDL-C 100mg/dL以上もしくはTC 180mg/dL以上で、コレステロール低下治療が必要と判断された症例
- ④IVUSガイド下に冠動脈インターベンション(PCI)が成功した、安定狭心症もしくは急性冠症候群症例
- ⑤PCIを受けた部位から5mm以上離れた部位にプラーク(厚さ500μm以上またはプラークが占める割合20%以上)が認められる症例
- 投与方法
-
全症例の診断結果および糖尿病の有無を考慮しながら、PTV単独群(ピタバスタチン 4mg/日)とPTV/EPA併用群(ピタバスタチン 4mg/日+エパデール 1,800mg/日)に無作為に割り付けた。
全症例は各自割り付けられた薬剤を、投与期間(PCI 後6~8ヵ月間)の終了、死亡、冠動脈イベントの発生、有害事象の発生、もしくは試験の参加中止となるまで投与した。なお全症例において、PCIから6ヵ月後までアスピリン(100~200mg/日)およびクロピドグレル(75mg/日)を投与した。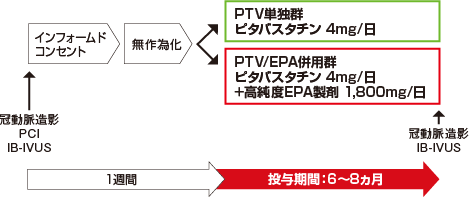
- 評価項目
-
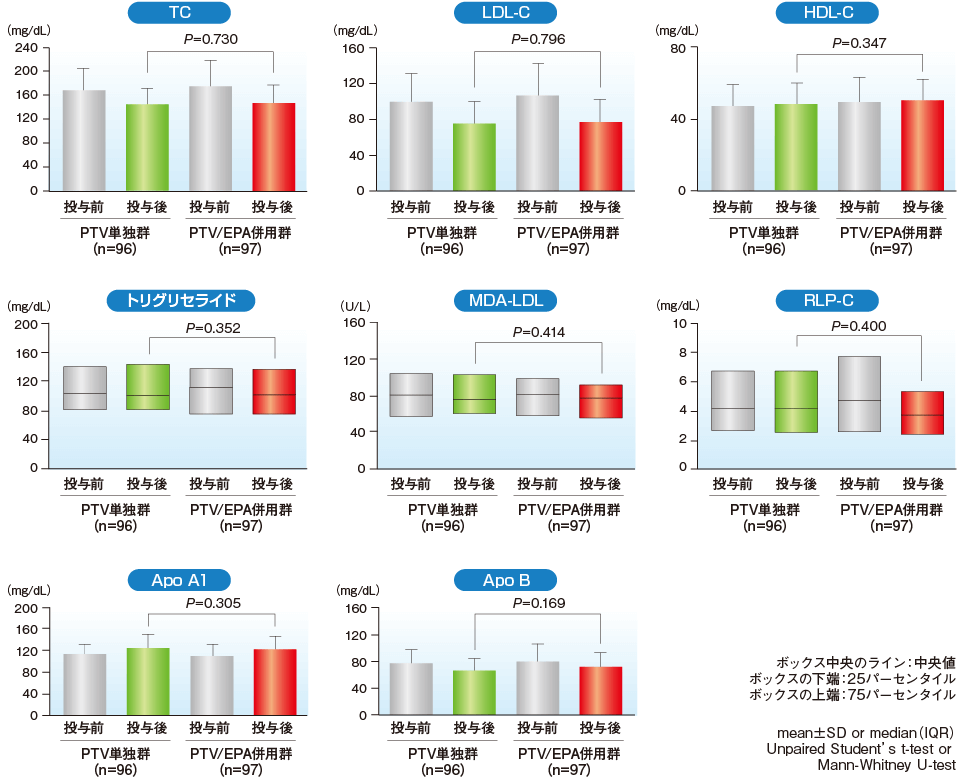
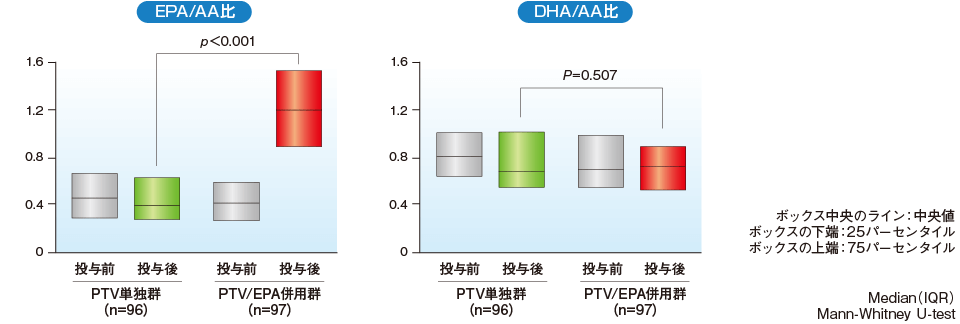
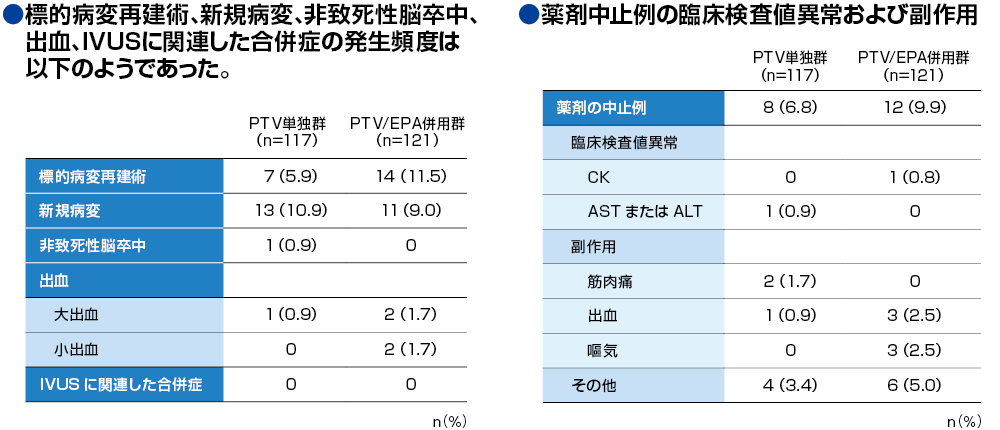
主要評価項目: IB-IVUS※により解析した冠動脈プラークの組織性状別体積変化 副次評価項目: プラーク体積、脂質パラメータの変化[TC、LDL-C、トリグリセライド、HDLコレステロール(HDL-C)、マロンジアルデヒド修飾LDL(MDA-LDL)、レムナント様リポ蛋白コレステロール(RLP-C)、アポリポプロテインA1・B(Apo A1・B)等]、EPA/アラキドン酸(AA)比、高感度CRP、主要冠動脈イベント(死亡、心臓死、非致死性心筋梗塞、不安定狭心症による入院、冠動脈血管再建術)等 安全性評価項目: 標的病変再建術、新規病変、非致死性脳卒中、出血、IVUSに関連した合併症、副作用、臨床検査異常値 ※IB-IVUS:Integrated backscatter intravascular ultrasound
- 解析計画
-
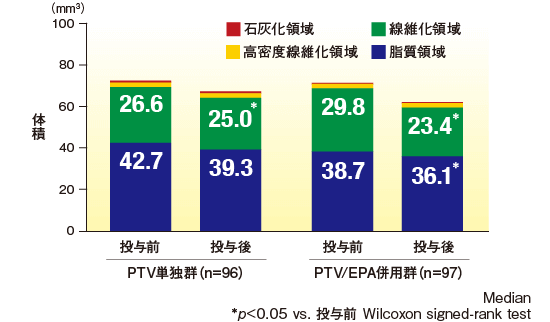
IB-IVUSは投与前および投与期間終了時に行った。ステント留置部位から近位部側もしくは遠位部側に5mm超離れた部位を標的部位とし、1mmごとの画像で解析を行った。各画像から外弾性板の断面積、内腔の断面積、プラークを含む中膜の断面積を計測した。シンプソンの公式により、プラークを含む中膜の断面積の総和を算出し、プラーク体積とした。
また、プラークの組織性状別に4種のカラーで色分けし(赤:石灰化領域、黄:高密度線維化領域、緑:線維化領域、青:脂質領域)、各体積を評価した。
IB-IVUSでの解析から、標準化した総プラーク体積(TAV)および各組織性状の体積変化率を算出した。プラークおよび脂質領域の体積の変化から、プラークの退縮および脂質領域の減少の度合いを評価した。
Unpaired Student’s t-testまたはMann-Whitney U-testを2群間の連続変数の比較に、Wilcoxon signed-rank testを群内比較に、また、Chi-square testまたはFisher’s exact testをカテゴリー変数の比較に用いた。
試験結果
冠動脈疾患患者の高コレステロール血症に対する高純度EPA
製剤エパデールとピタバスタチンの併用意義が示された。2023年8月作成
17357-1 N23/21 B1 GT