- 医療関係者向けホーム
- 産婦人科領域
- ディナゲスト
- ディナゲスト錠1mg
- Clinical Study:国内第Ⅲ相長期投与試験〈52週間投与〉(子宮内膜症) 安全性
 Clinical Study国内第Ⅲ相長期投与試験〈52週間投与〉(子宮内膜症)
Clinical Study国内第Ⅲ相長期投与試験〈52週間投与〉(子宮内膜症)
安全性
主要評価項目
副作用発現率
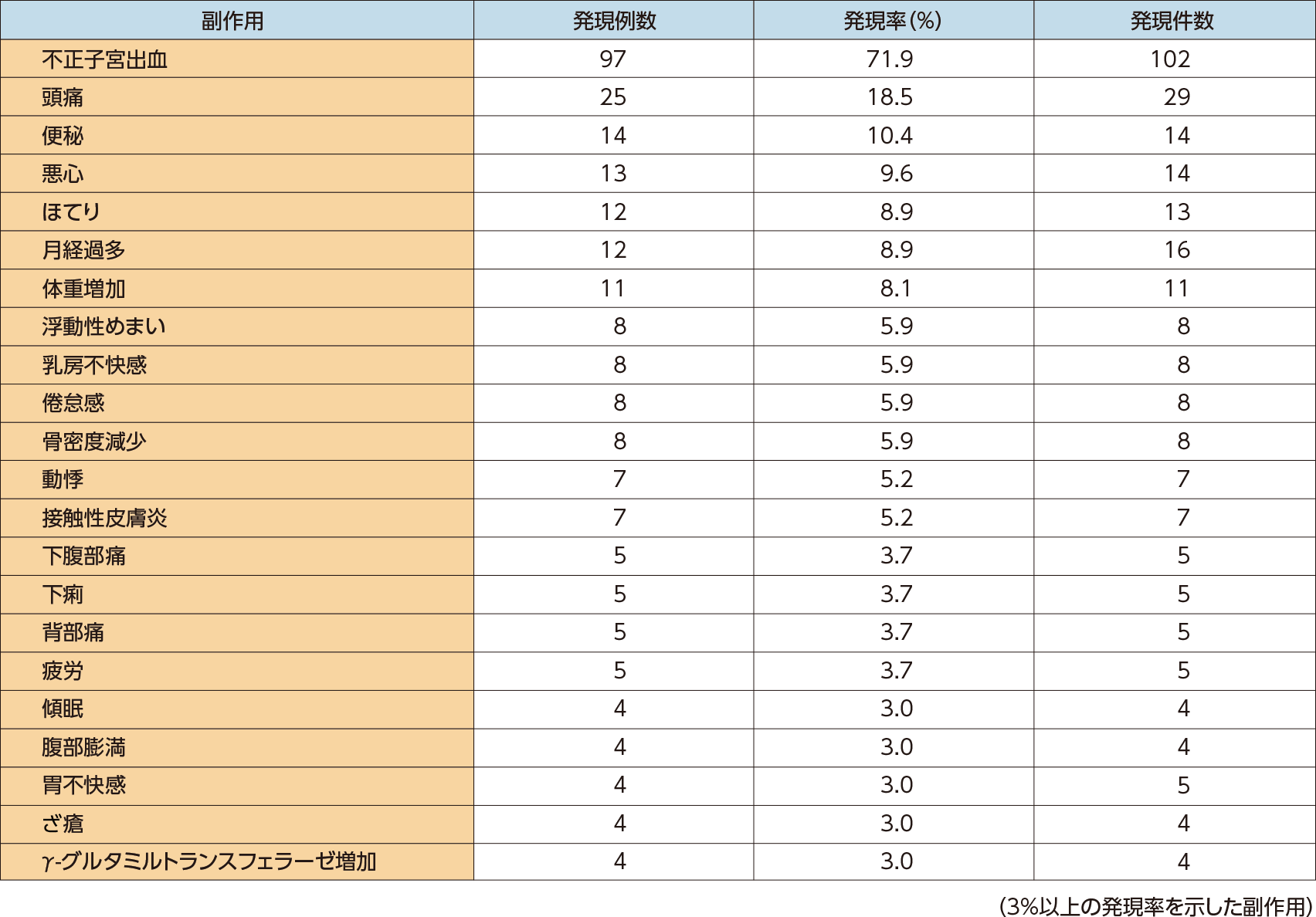
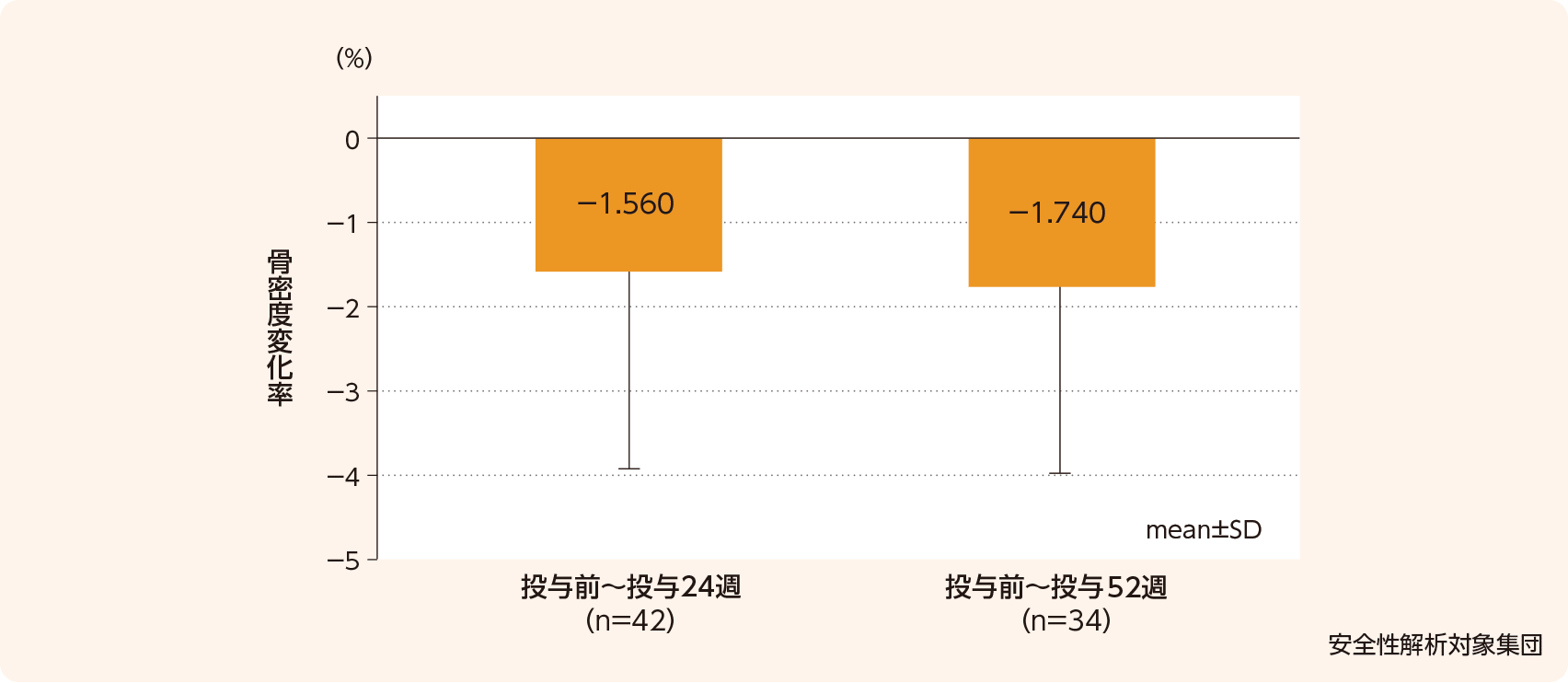
長期投与試験で副作用は135例中120例(88.9%)に認められた。主な副作用は、不正子宮出血(71.9%)、頭痛(18.5%)、便秘(10.4%)、悪心(9.6%)、ほてり、月経過多(各8.9%)、体重増加(8.1%)、浮動性めまい、乳房不快感、倦怠感、骨密度減少(各5.9%)、動悸、接触性皮膚炎(各5.2%)、下腹部痛、下痢、背部痛、疲労(各3.7%)、傾眠、腹部膨満、胃不快感、ざ瘡、γ-グルタミルトランスフェラーゼ増加(各3.0%)であった。
本試験において、死亡例を含む重篤な副作用は認められなかった。投与中止に至った副作用が7例(不正子宮出血2例、背部痛及び四肢痛、骨密度減少、便秘及び乳房不快感、糖鎖抗原125増加及び背部痛、耳鳴が各1例)認められた。