- 医療関係者向けホーム
- ディナゲスト錠0.5mg
- Clinical Study:国内第Ⅲ相長期投与試験(52週間投与) VAS変化量
 Clinical Study国内第Ⅲ相長期投与試験(52週間投与)
Clinical Study国内第Ⅲ相長期投与試験(52週間投与)
VAS変化量
VAS変化量(FAS解析対象、OC)〔副次評価項目、診断分類別及び用量変更の有無別サブグループ解析を含む〕
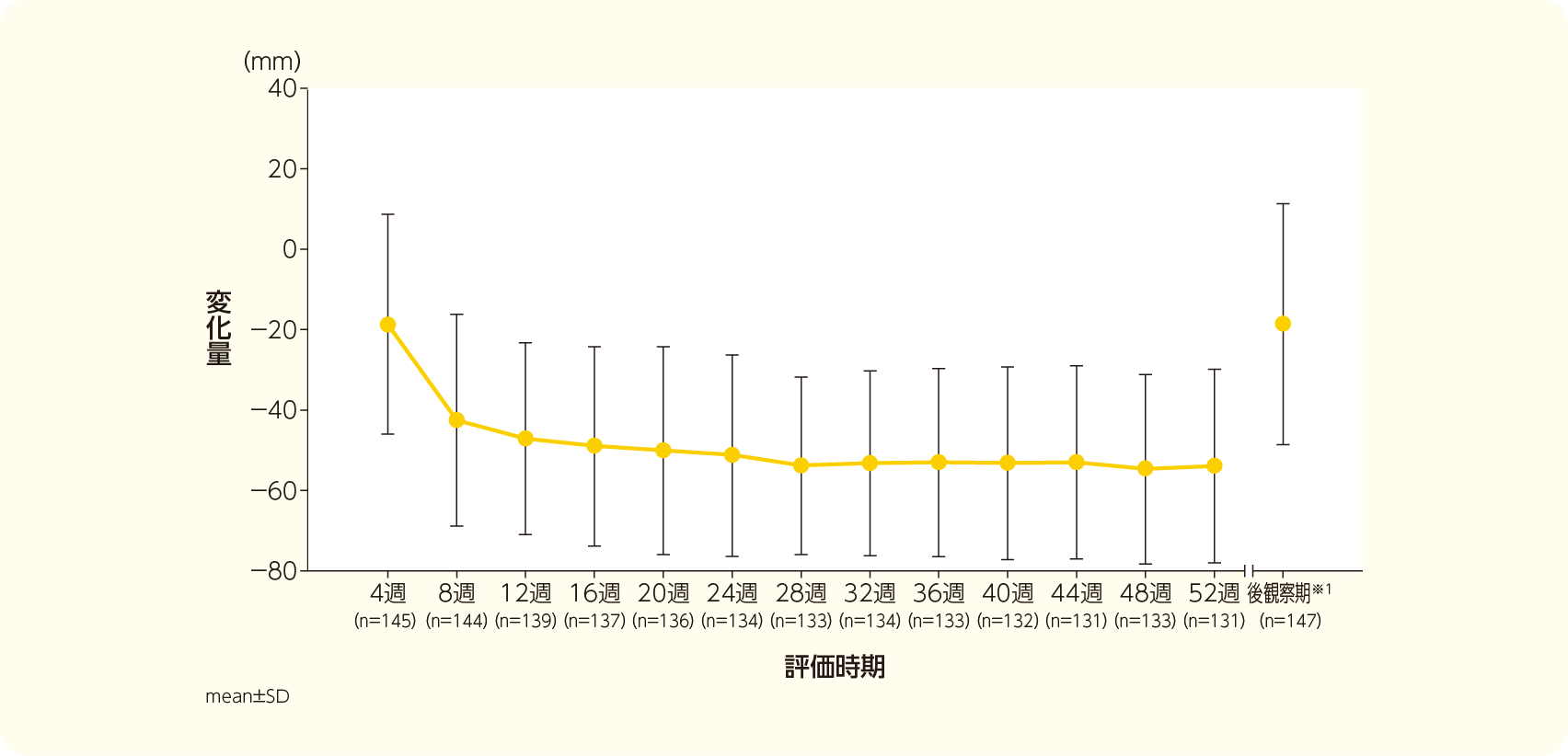
投与4週、8週、12週、16週、20週、24週及び52週時のVAS変化量(mean±SD)は、それぞれ−18.60±27.36mm、−42.60±26.33mm、−47.20±23.88mm、−49.04±24.64mm、−50.15±25.75mm、 −51.33±25.06mm及び−54.01±24.12mmであった。後観察期※1の変化量(mean±SD)は−18.67±29.93mmであった。
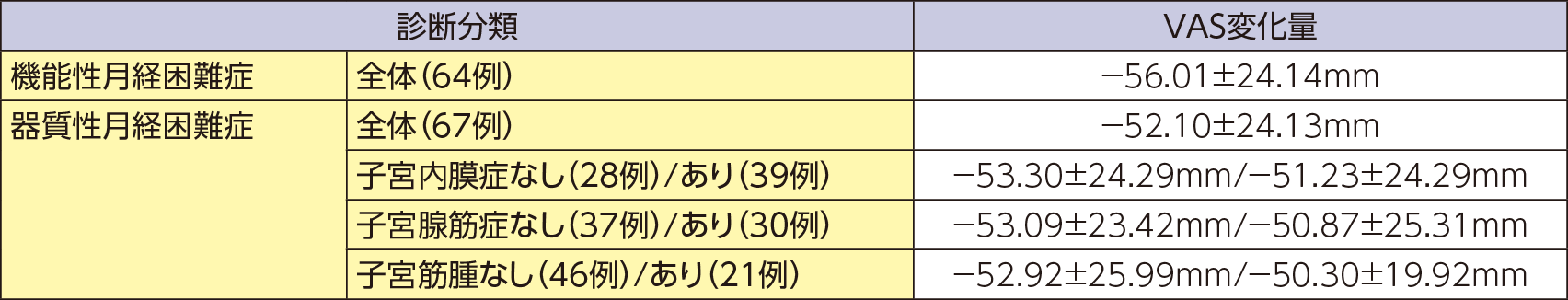
診断分類別では、投与52週時のVAS変化量(mean±SD)は、機能性月経困難症−56.01±24.14mm、器質性月経困難症−52.10±24.13mmであった。器質的疾患の種類別では、子宮内膜症なし−53.30±24.29mm、あり−51.23±24.29mm、子宮腺筋症なし−53.09±23.42mm、あり−50.87±25.31mm、子宮筋腫なし−52.92±25.99mm、あり−50.30±19.92mmであった。
用量変更の有無別では、投与52週時のVAS変化量(mean±SD)は、用量変更なし−54.98±24.20mm、あり−46.52±22.94mmであった※2。
- ※2:投与12週時以降の評価時期に月経困難症スコア変化量に2点以上の改善が認められない場合(疼痛改善効果不十分)、2mg/日に増量することが可能とされており、147例中16例に用量変更があった。