- 医療関係者向けホーム
- 精神科領域
- レクサプロ
- Information:開発の経緯
 Information
Information
開発の経緯
うつ病は、精神症状及び身体症状のため、生活の質(Quality of Life)の低下をきたす疾患です。うつ病患者の多くは気分や意欲の低下と集中困難などにより家事や仕事などの日常生活に支障をきたし、重症例では休職や失職につながり、経済的な困窮に陥ることも問題となっています。これに対して、適切にうつ病治療を行うことにより、治療早期に寛解を得ること、回復までの時間の短縮、再発リスクを抑えることができるとも言われています。
このようなうつ病の治療薬として、海外でSSRIなどの新規抗うつ薬が1980年代から登場し、本邦のうつ病治療においても広く使用されています。その一方で、より高い寛解率の達成、効果発現までの時間の短縮、賦活化症候群や離脱症状の軽減など、抗うつ薬の解決すべき課題も残されています。
こうした状況から、本邦においても新たな抗うつ薬の開発が待ち望まれていました。
レクサプロ錠®10mg(一般的名称:エスシタロプラムシュウ酸塩)は、デンマークのルンドベック社が開発したSSRIです。ルンドベック社はエスシタロプラムの開発に先立ち、ラセミ体であるシタロプラム(国内未承認)を開発し、1989年にデンマークで承認されました。その後シタロプラムの活性本体がS-エナンチオマーであることを見出し、光学分割したS-エナンチオマーがエスシタロプラムです。エスシタロプラムはセロトニントランスポータへの選択性が高く、セロトニン以外の神経伝達系への影響が少ないと考えられます。
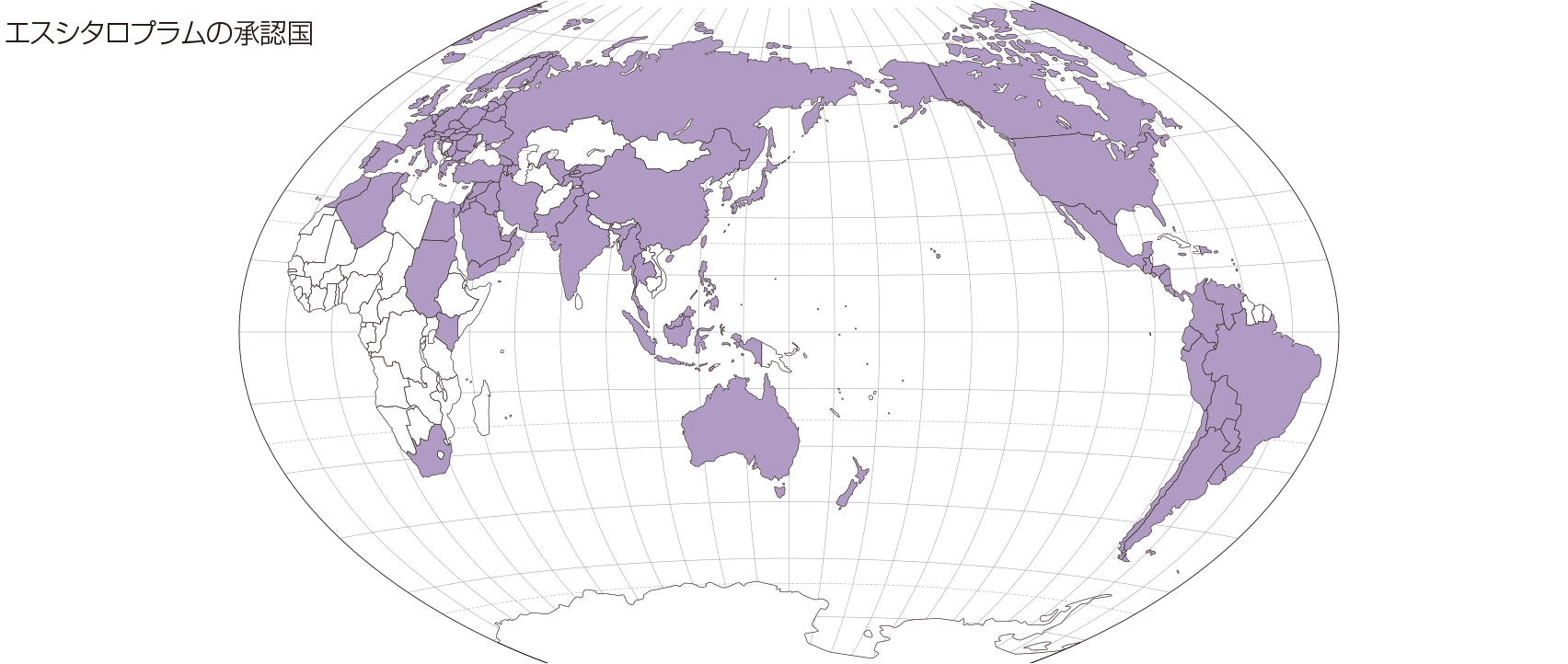
海外では、2001年にスウェーデンで初めて大うつ病性障害及びパニック障害注1)の適応症で承認されました。その後、ヨーロッパ全土で承認され、2017年10月現在、米国、英国、カナダ、オーストラリアなど世界102の国と地域で承認され、2014年12月末までに、全世界で約3億5千万人以上に対して投与されたと推定注2)されます。
持田製薬は、エスシタロプラムがうつ病の薬物治療において新たな選択肢を提供できる臨床的に意義のある薬剤と判断し、2001年より本邦での開発を開始しました。国内の開発治験では、2008年から2010年に実施された第Ⅲ相試験で大うつ病性障害の外来患者を対象に10mgから20mgを1日1回投与した結果、プラセボに対する優越性と既存薬に対する非劣性が検証されました。また、長期投与試験においても安全性と有効性が検討されました。これらの結果より、エスシタロプラムの有効性と安全性が認められ、2011年4月に「うつ病・うつ状態」の効能又は効果で承認されました。
「社会不安障害」の効能又は効果については、2011年より本邦での開発を開始しました。国内で実施した社会不安障害患者を対象とした臨床試験注3)において有効性及び安全性を検討し、効能又は効果の追加申請を行い、2015年11月に承認されました。
レクサプロ錠20mgは、患者への利便性等を考慮して開発企画し、含量が異なる経口固形製剤の生物学的同等性試験ガイドライン(平成24年2月29日 薬食審査発0229第10号)に基づき、溶出試験を実施し、2018年11月に承認取得しました。
- 注1)本邦で承認された効能又は効果は「うつ病・うつ状態」及び「社会不安障害」です。
- 注2)全世界での販売実績をもとに平均投与量10mg、平均投与期間3ヵ月として投与患者数を推定しました。
- 注3)2008年に日本精神神経学会により社交不安障害と表記されることになったため、臨床試験は社交不安障害を対象として実施されましたが、効能又は効果にあわせて、社会不安障害と記載しています。