- 医療関係者向けホーム
- 消化器領域
- モビコール®配合内用剤
- Clinical Study:成人国内第Ⅲ相試験(検証期:プラセボ対照試験) 便硬度
 Clinical Study成人国内第Ⅲ相試験(検証期:プラセボ対照試験)
Clinical Study成人国内第Ⅲ相試験(検証期:プラセボ対照試験)
「モビコール」及びMOVICOLは、Norgineグループの登録商標です。
便硬度
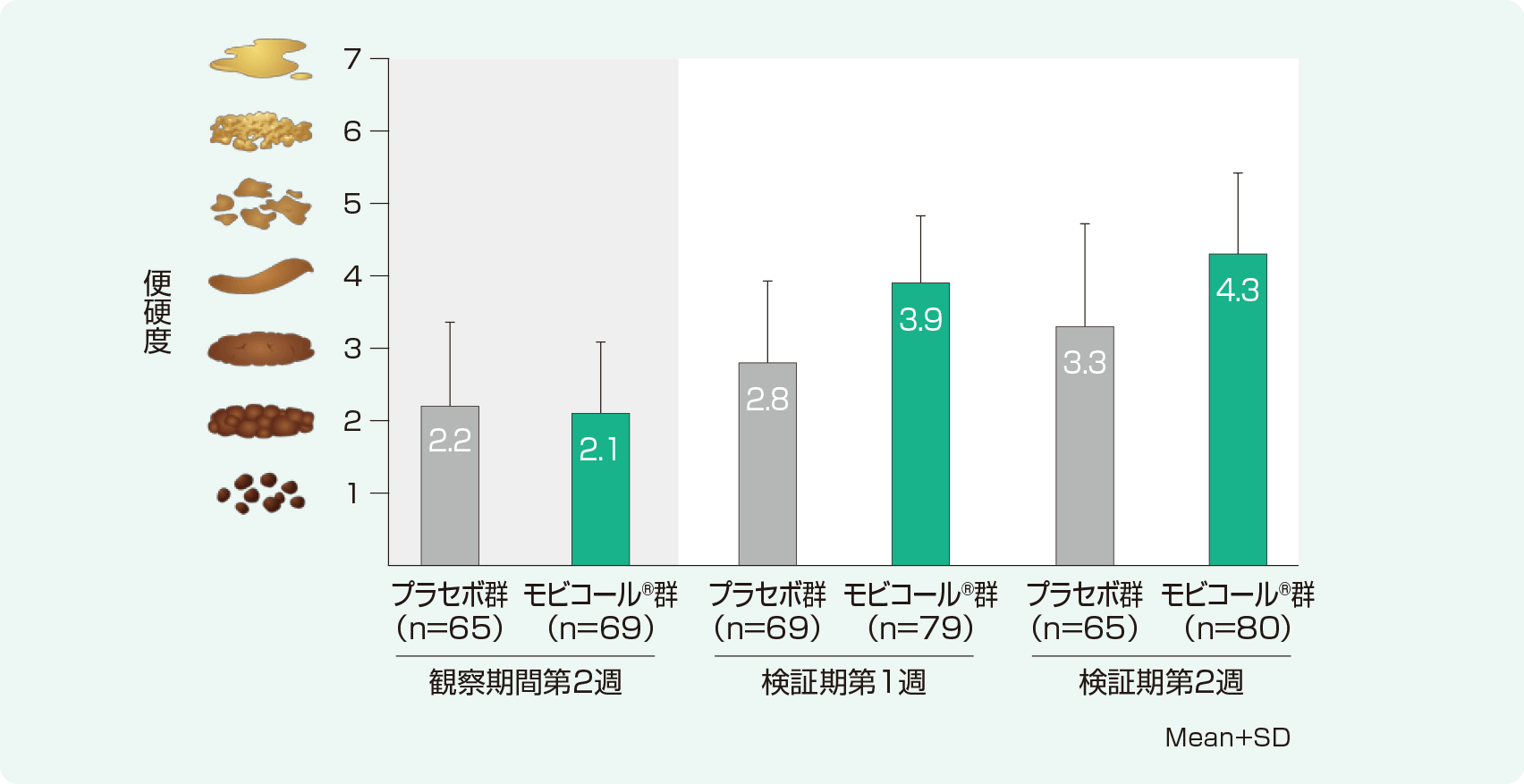
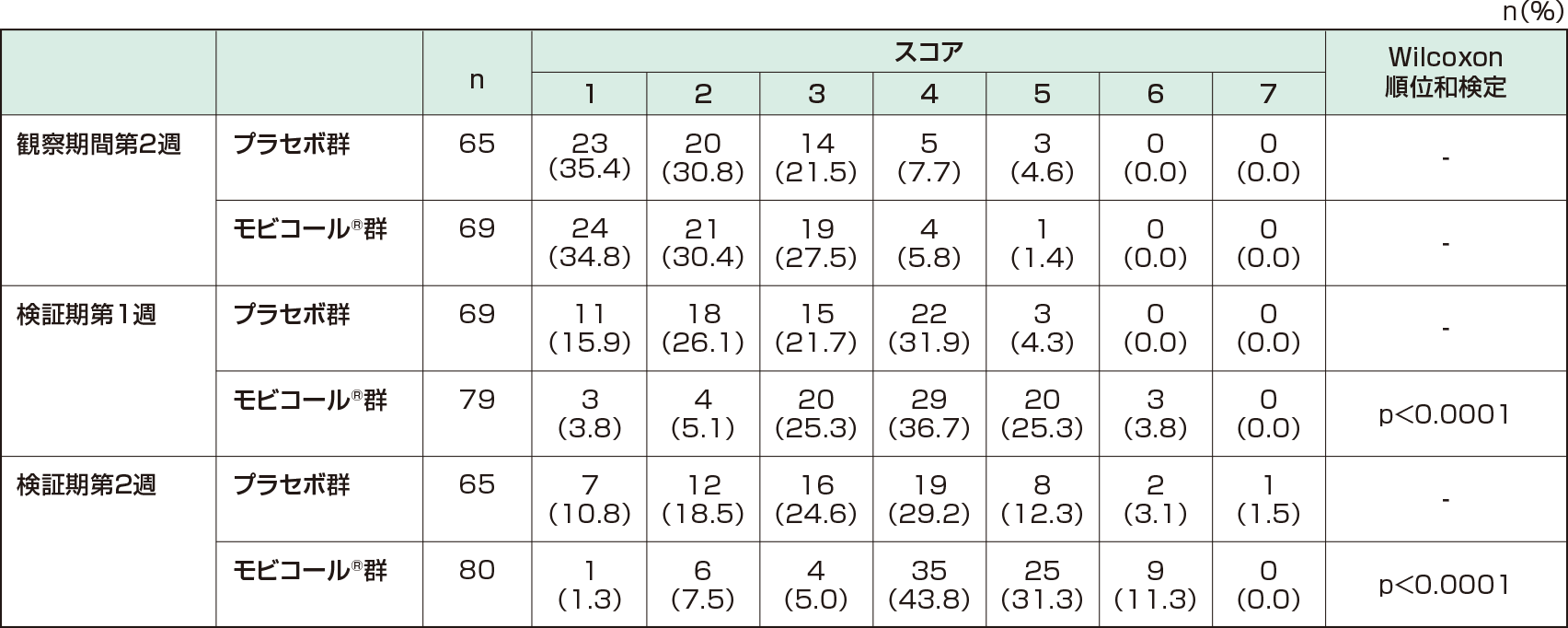
Bristol便形状スケール※に基づいた便硬度<副次評価項目>(FAS)
1週間あたりのBristol便形状スケールに基づいた便硬度の中央値(Mean±SD)は、観察期間第2週においてプラセボ群2.2±1.1、モビコール®群2.1±1.0、検証期第1週においてプラセボ群2.8±1.2、モビコール®群3.9±1.1であった。また、検証期第2週においてプラセボ群3.3±1.4、モビコール®群4.3±1.1であった。
Bristol便形状スケールに基づいた便硬度の中央値のスコア分類別割合は、検証期第1週、第2週ともにプラセボ群とモビコール®群の間に有意に差が認められた(Wilcoxon 順位和検定:検証期第1週、第2週ともにp<0.0001、名目上のp値)。