- 医療関係者向けホーム
- 産婦人科領域
- ディナゲスト
- ディナゲスト錠1mg
- Clinical Study:国内第Ⅲ相長期投与試験〈52週間投与〉(子宮腺筋症) 性器出血
 Clinical Study国内第Ⅲ相長期投与試験〈52週間投与〉(子宮腺筋症)
Clinical Study国内第Ⅲ相長期投与試験〈52週間投与〉(子宮腺筋症)
性器出血
その他の評価項目
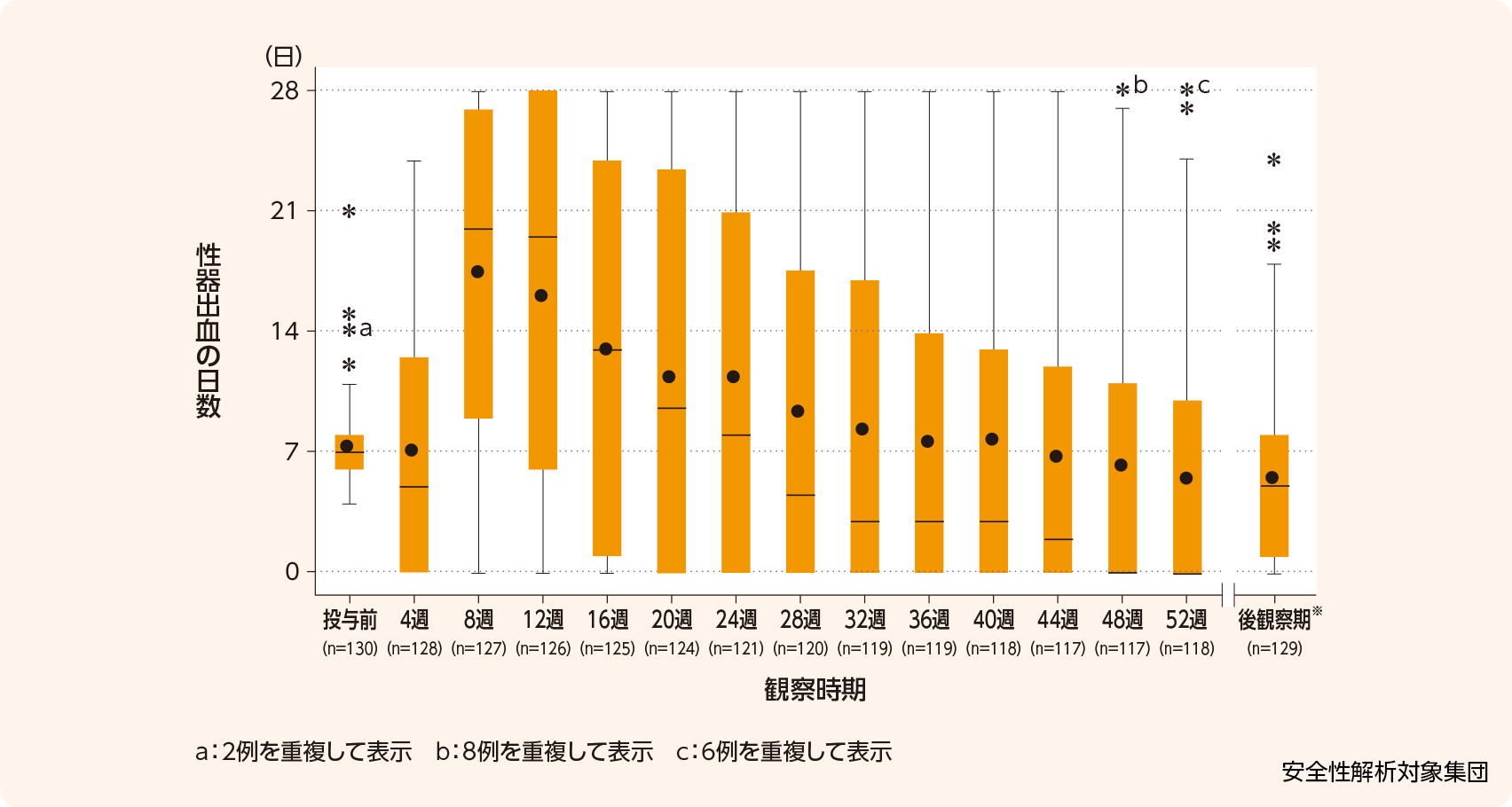
性器出血の発現日数
投与中の性器出血は125/129例に認められ、投与中の性器出血発現日数及び投与日数に占める性器出血の発現日数の割合(mean±SD)は、123.1±86.9日及び36.66±25.31%であった。
各評価時期(28日ごと)の性器出血の発現日数(mean±SD、日)の推移は、投与前、投与4週、8週、12週、16週、20週、24週、52週及び後観察期※でそれぞれ7.3±2.4、7.1±7.2、17.5±10.0、16.1±10.8、13.0±10.8、11.4±10.8、11.3±10.9、5.5±8.5及び5.5±4.8であった。
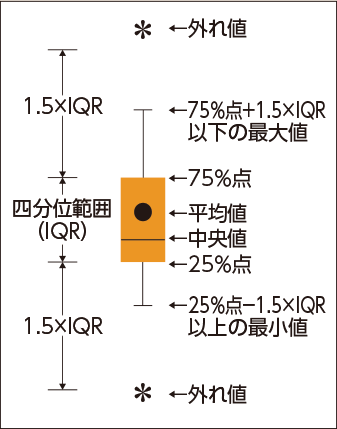
- ボックスプロットの凡例についてはこちらをご参照ください。
- ※後観察期:投与終了後4~8週間(再来月経終了時まで)
8. 重要な基本的注意(一部抜粋)
-
8.4本剤投与後に不正子宮出血があらわれ、重度の貧血に至ることがある。不正子宮出血の程度には個人差があり、投与中に出血が持続する場合や一度に大量の出血が生じる場合もあるので、以下の点に注意すること。[2.4、11.1.1 参照]
- ・患者にはあらかじめ十分に説明し、出血量が多く持続日数が長い場合や一度に大量の不正子宮出血が認められた場合には、医師へ相談するよう指導すること。
- ・貧血のある患者では、必要に応じて本剤投与前に貧血の治療を行うこと。
- ・不正子宮出血が認められた場合には必要に応じて血液検査を実施し、患者の状態を十分に観察すること。異常が認められた場合には鉄剤の投与又は本剤の投与中止、輸血等の適切な処置を行うこと。