- 医療関係者向けホーム
- 産婦人科領域
- ディナゲスト
- ディナゲスト錠・OD錠1mg
- Information:ディナゲスト投与中の不正性器出血について
 Information
Information
ディナゲスト投与中の不正性器出血について
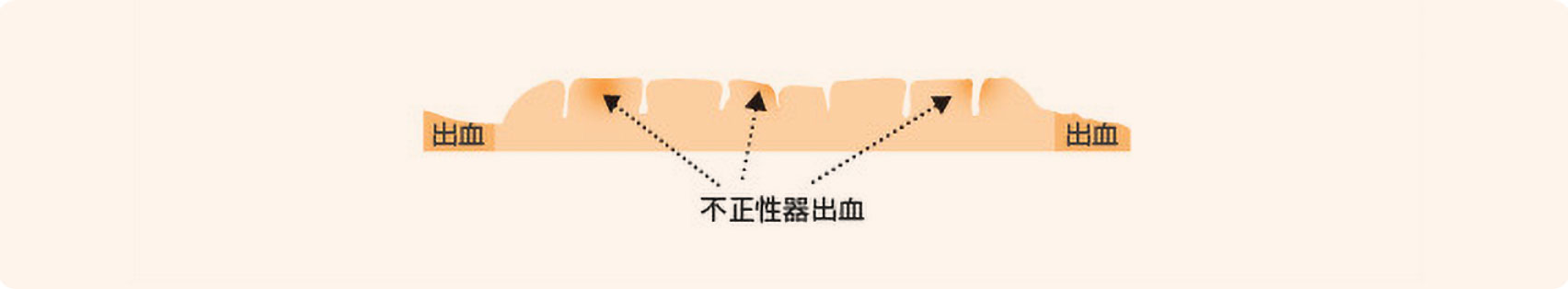
投与中は不正性器出血が起こりやすくなります。
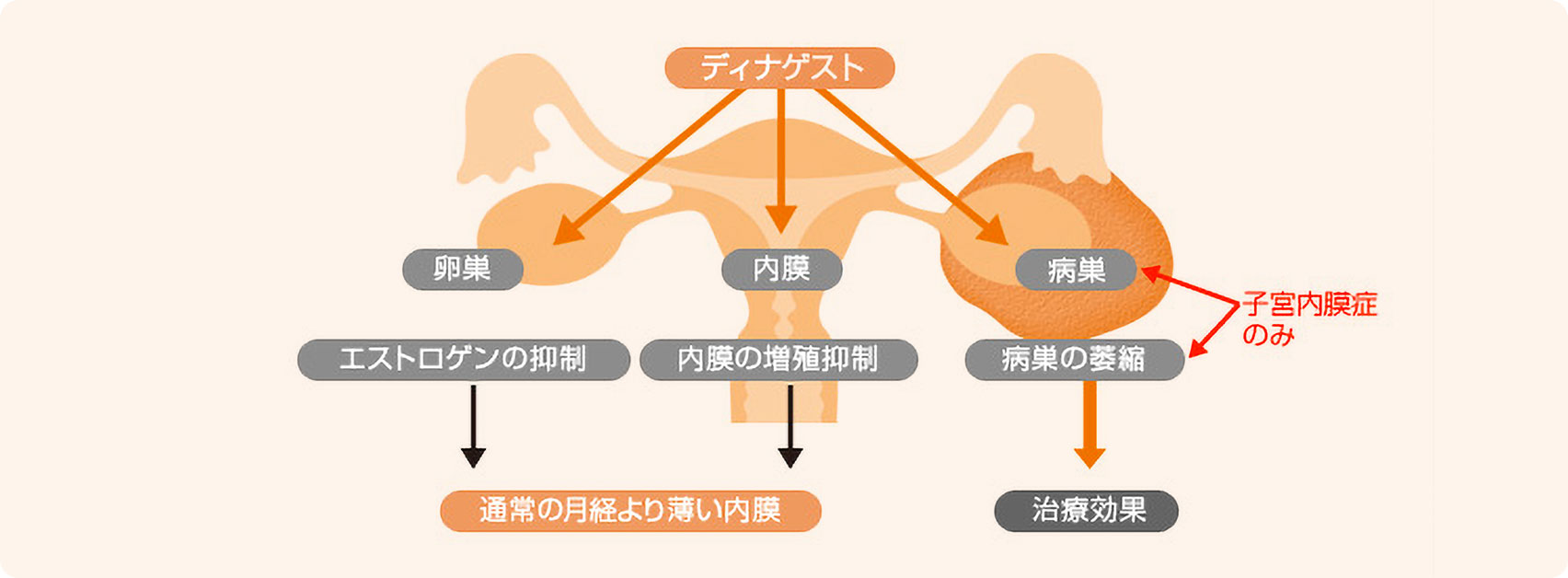
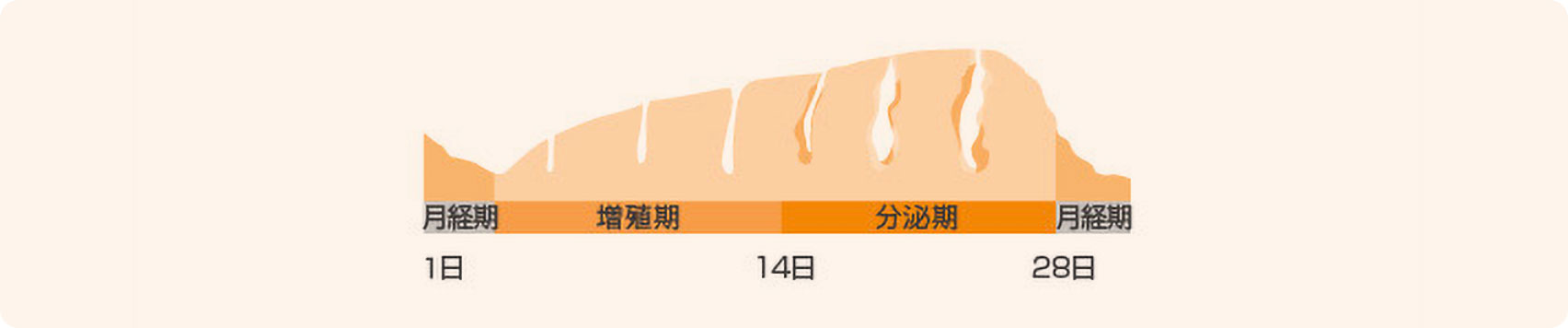
- 1.ディナゲストにはエストロゲンの産生を抑制する作用があるため、投与中は通常の月経(月経のしくみ)より薄い子宮内膜が形成されます。
- 2.また薄い子宮内膜はディナゲストのプロゲステロン作用で、分泌期状態に変化します。
- 3.分泌期状態の薄い子宮内膜は、通常の子宮内膜よりはがれやすいため、ディナゲスト投与中は不正性器出血が起こりやすくなります。
副次評価項目
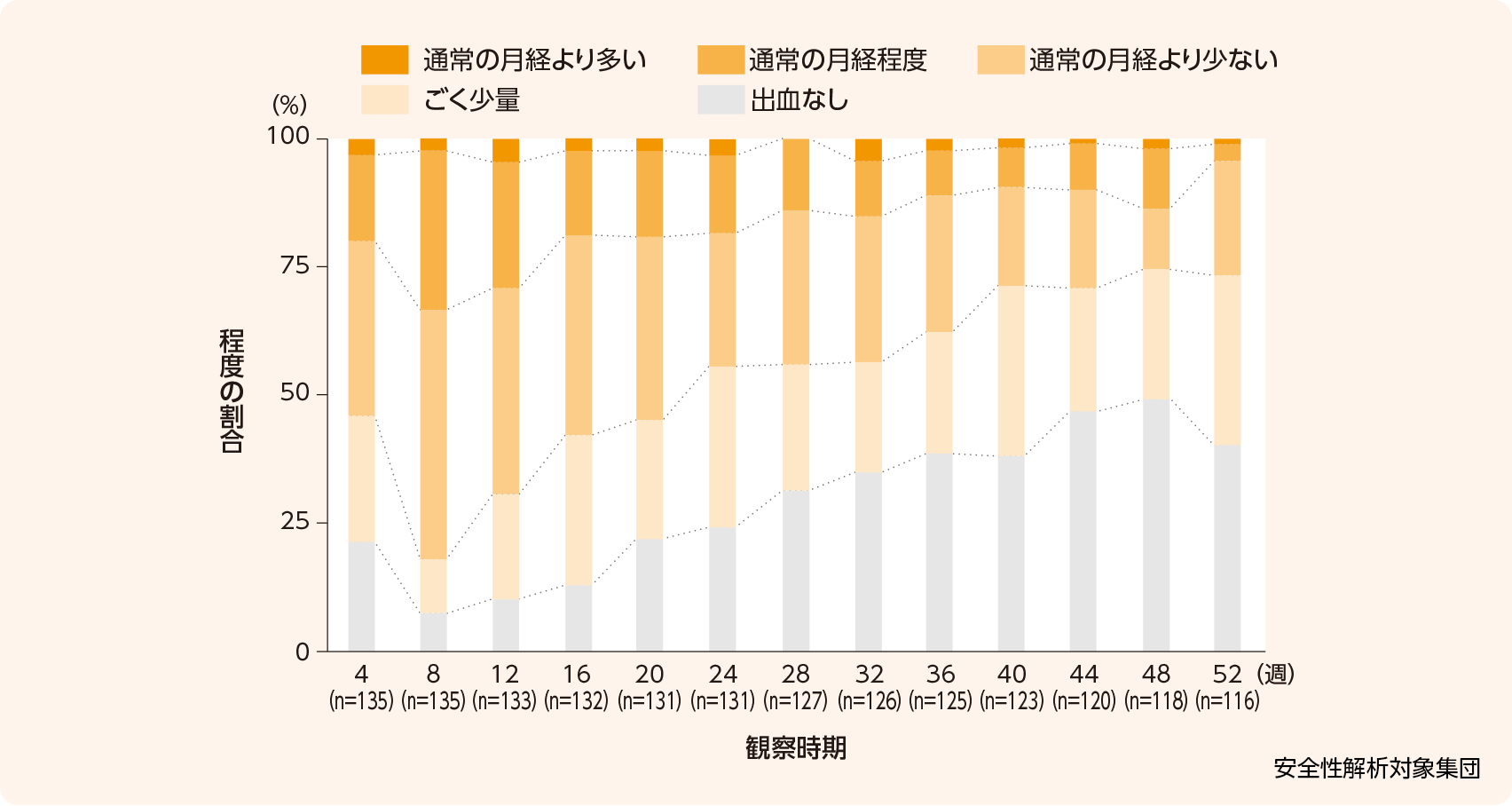
子宮内膜症患者を対象とした国内第Ⅲ相長期投与試験における性器出血1)
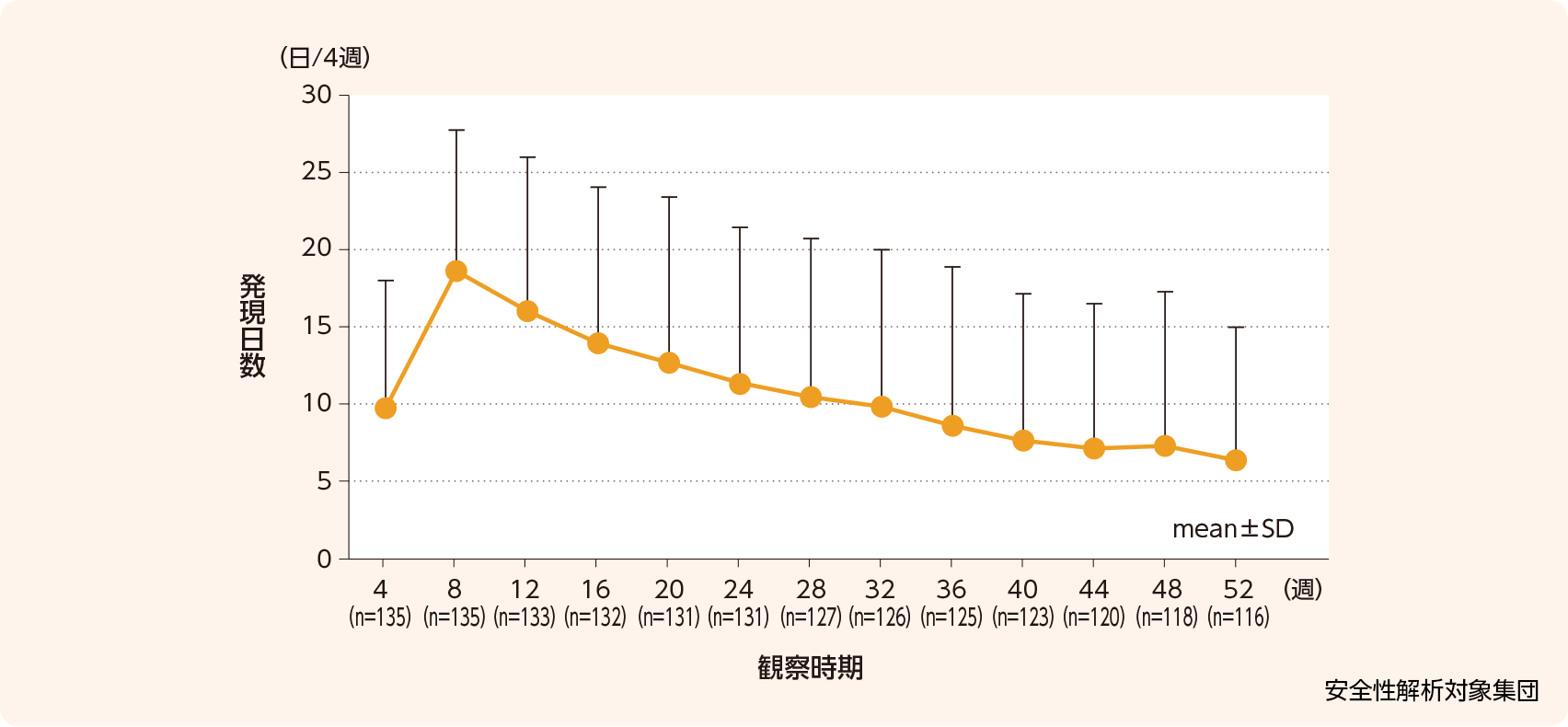
子宮内膜症患者135例に、ジエノゲスト2mg/日を1日2回に分け52週間投与したときの性器出血が認められた症例の割合は、投与8週で92.6%、24週で75.6%、52週で59.5%でした。
また、「通常の月経程度以上」の出血に限った場合には投与8週で33.3%、24週で18.3%、52週で4.3%でした。
性器出血の日数(平均値)は、投与8週で18.7日、24週で11.3日、52週で6.4日でした。
子宮内膜に対する作用(性器出血の発現機序について)2)
子宮内膜症患者に、ジエノゲスト2mg/日を1日2回に分け16週間投与し、性器出血発現時の子宮内膜組織像を検討しました。ジエノゲスト投与期間中の性器出血発現時に、上皮は無機能像あるいは萎縮像を示し、間質には脱落膜反応が認められました。これらの変化(偽脱落膜化)は、ジエノゲストの子宮内膜に対するプロゲステロン作用と考えられました。ジエノゲストにより形成された、偽脱落膜に起因する破綻出血が性器出血の主な原因と推定され、他のプロゲスチンによる性器出血と同じ機序と考えられました。
8. 重要な基本的注意(一部抜粋)
-
8.4本剤投与後に不正出血があらわれ、重度の貧血に至ることがある。出血の程度には個人差があり、投与中に出血が持続する場合や一度に大量の出血が生じる場合もあるので、以下の点に注意すること。[2.4、11.1.1 参照]
- ・患者にはあらかじめ十分に説明し、出血量が多く持続日数が長い場合や一度に大量の出血が認められた場合には、医師へ相談するよう指導すること。
- ・貧血のある患者では、必要に応じて本剤投与前に貧血の治療を行うこと。
- ・不正出血が認められた場合には必要に応じて血液検査を実施し、患者の状態を十分に観察すること。異常が認められた場合には鉄剤の投与又は本剤の投与中止、輸血等の適切な処置を行うこと。
- ・子宮内膜症患者を対象とした国内臨床試験において、子宮腺筋症又は子宮筋腫を合併する患者での貧血の発現率は、合併しない患者と比較して高い傾向が認められている。
その他の評価項目
子宮腺筋症患者を対象とした国内第Ⅲ相長期投与試験における性器出血3、4)
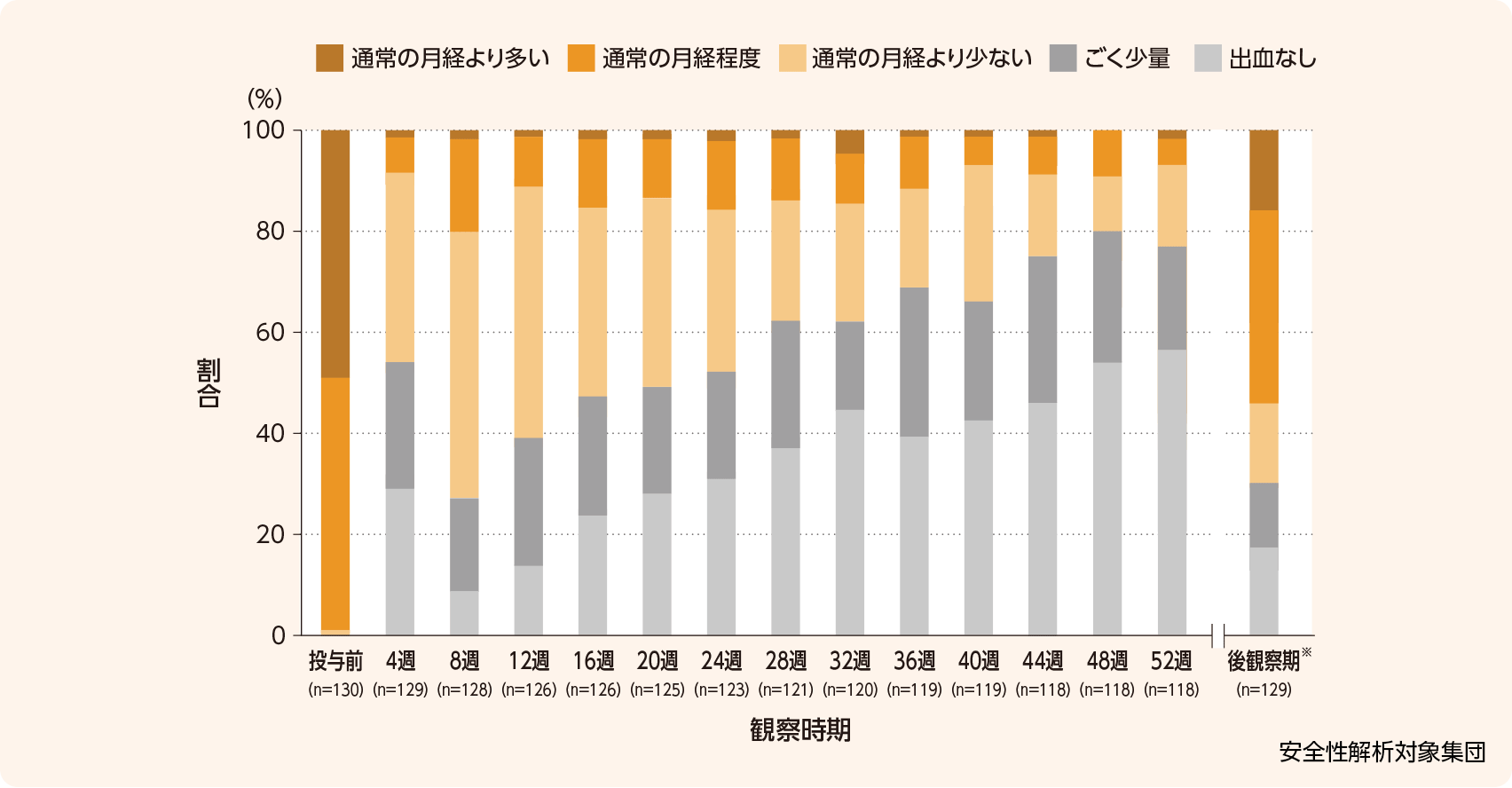
1)性器出血
①性器出血の発現日数
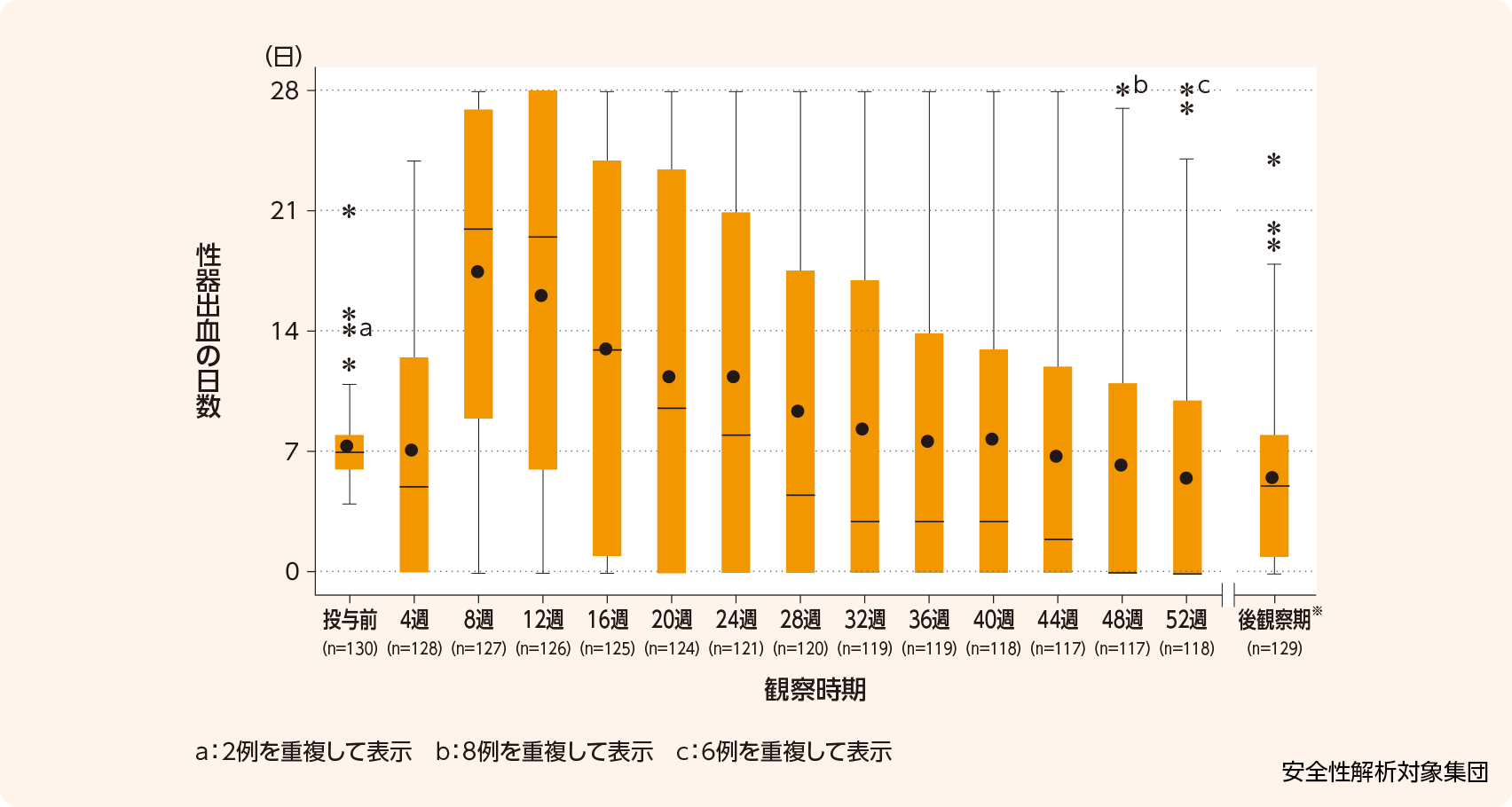
投与中の性器出血は125/129例に認められ、投与中の性器出血発現日数及び投与日数に占める性器出血の発現日数の割合(mean±SD)は、123.1±86.9日及び36.66±25.31%でした。
各評価時期(28日ごと)の性器出血の日数(mean±SD、日)の推移は、投与前、投与4週、8週、12週、16週、20週、24週、52週及び後観察期※でそれぞれ7.3±2.4、7.1±7.2、17.5±10.0、16.1±10.8、13.0±10.8、11.4±10.8、11.3±10.9、5.5±8.5及び5.5±4.8でした。
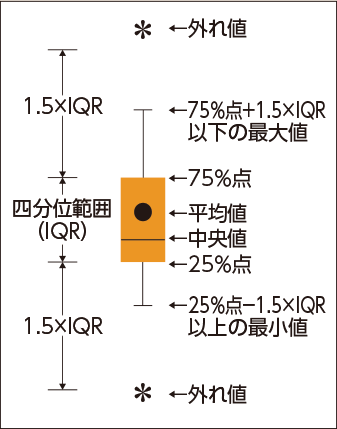
- ボックスプロットの凡例についてはこちらをご参照ください。
- ※後観察期:投与終了後4~8週間(再来月経終了時まで)
8. 重要な基本的注意(一部抜粋)
-
8.4本剤投与後に不正出血があらわれ、重度の貧血に至ることがある。出血の程度には個人差があり、投与中に出血が持続する場合や一度に大量の出血が生じる場合もあるので、以下の点に注意すること。[2.4、11.1.1 参照]
- ・患者にはあらかじめ十分に説明し、出血量が多く持続日数が長い場合や一度に大量の出血が認められた場合には、医師へ相談するよう指導すること。
- ・貧血のある患者では、必要に応じて本剤投与前に貧血の治療を行うこと。
- ・不正出血が認められた場合には必要に応じて血液検査を実施し、患者の状態を十分に観察すること。異常が認められた場合には鉄剤の投与又は本剤の投与中止、輸血等の適切な処置を行うこと。
- 1)持田製薬社内資料 : 長期投与試験-子宮内膜症患者における長期 投与の有効性および安全性の検討-(2007年10月19日承認、 CTD 2.7.6.8)〔承認時評価資料〕
- 2)Irahara, M. et al.: Reprod. Med. Biol. 2007;6(4): 223-228
[利益相反]本研究は持田製薬株式会社の支援により行われた。 - 3)持田製薬社内資料 : 子宮腺筋症患者を対象とした長期投与試験 (2016年12月2日承認、CTD 5.3.5.2.2) 〔承認時評価資料〕
- 4)Osuga, Y. et al.: J. Obstet. Gynaecol. Res. 2017;43(9) : 1441-1448
[利益相反]本研究は持田製薬株式会社の支援により行われた。著者のうち2名は持田製薬株式会社の社員である。