- 医療関係者向けホーム
- 消化器領域
- オンボー®
- Clinical Study(潰瘍性大腸炎)「維持期」に対する効果 臨床的寛解
 Clinical Study(潰瘍性大腸炎)「維持期」に対する効果
Clinical Study(潰瘍性大腸炎)「維持期」に対する効果
臨床的寛解
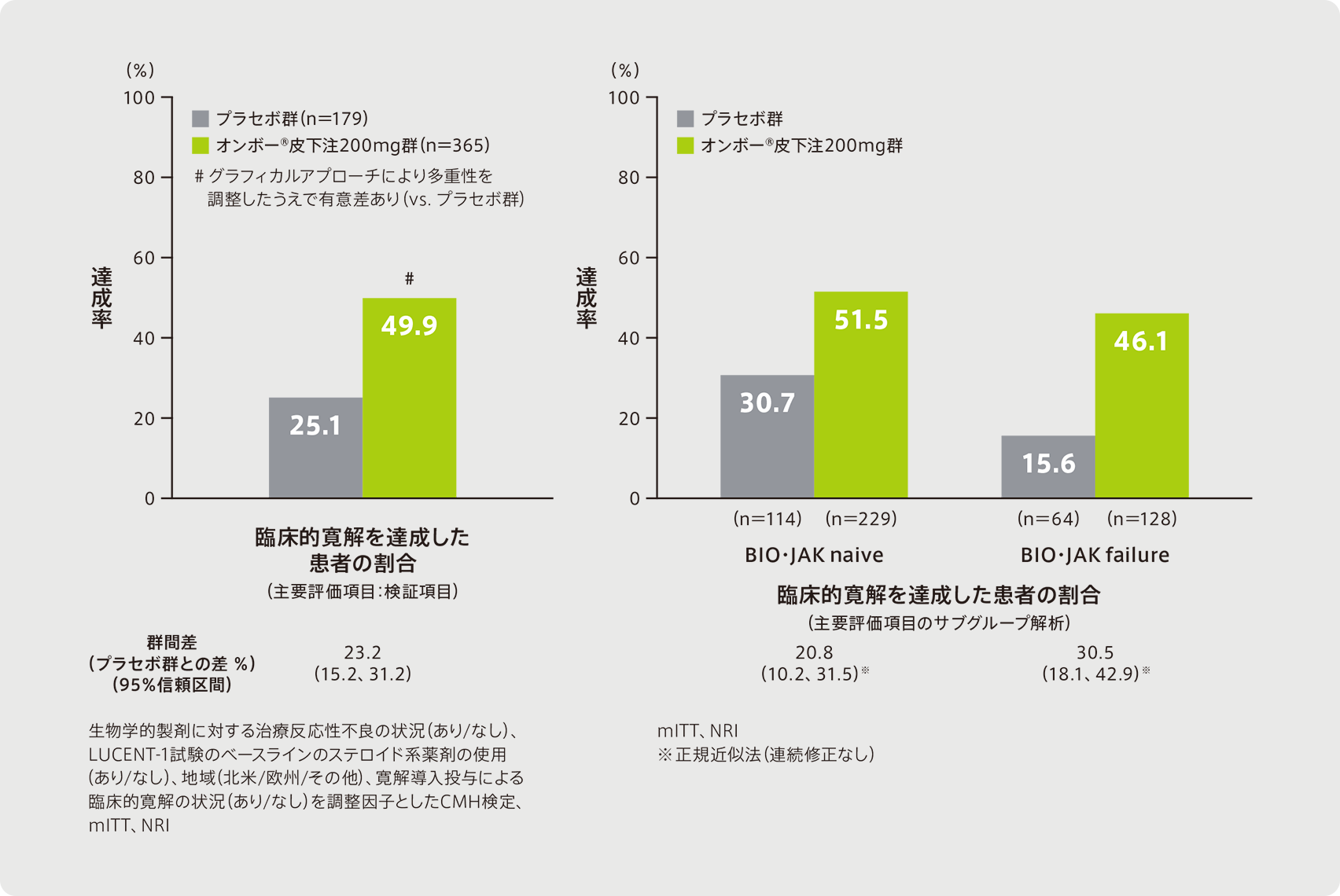
●40週時点で臨床的寛解を達成した患者の割合注)
〔主要評価項目(検証的解析結果)〕(主要評価項目のサブグループ解析)
- 注)LUCENT-1試験でオンボー®の寛解導入投与を受けて臨床的改善を達成した患者を対象に評価した
主要評価項目である40週時点で臨床的寛解を達成した患者の割合は、オンボー®皮下注200mg群では49.9%(182/365例)であり、プラセボ群の25.1%(45/179例)と比較して統計学的有意に高いことが示され、優越性が検証された(p<0.001、CMH検定、多重性調整を実施)。
サブグループ解析であるBIO・JAK naiveにおける40週時点で臨床的寛解を達成した患者の割合は、オンボー®皮下注200mg群51.5%(118/229例)、プラセボ群30.7%(35/114例)、BIO・JAK failureにおける40週時点で臨床的寛解を達成した患者の割合は、オンボー®皮下注200mg群46.1%(59/128例)、プラセボ群15.6%(10/64例)であった。
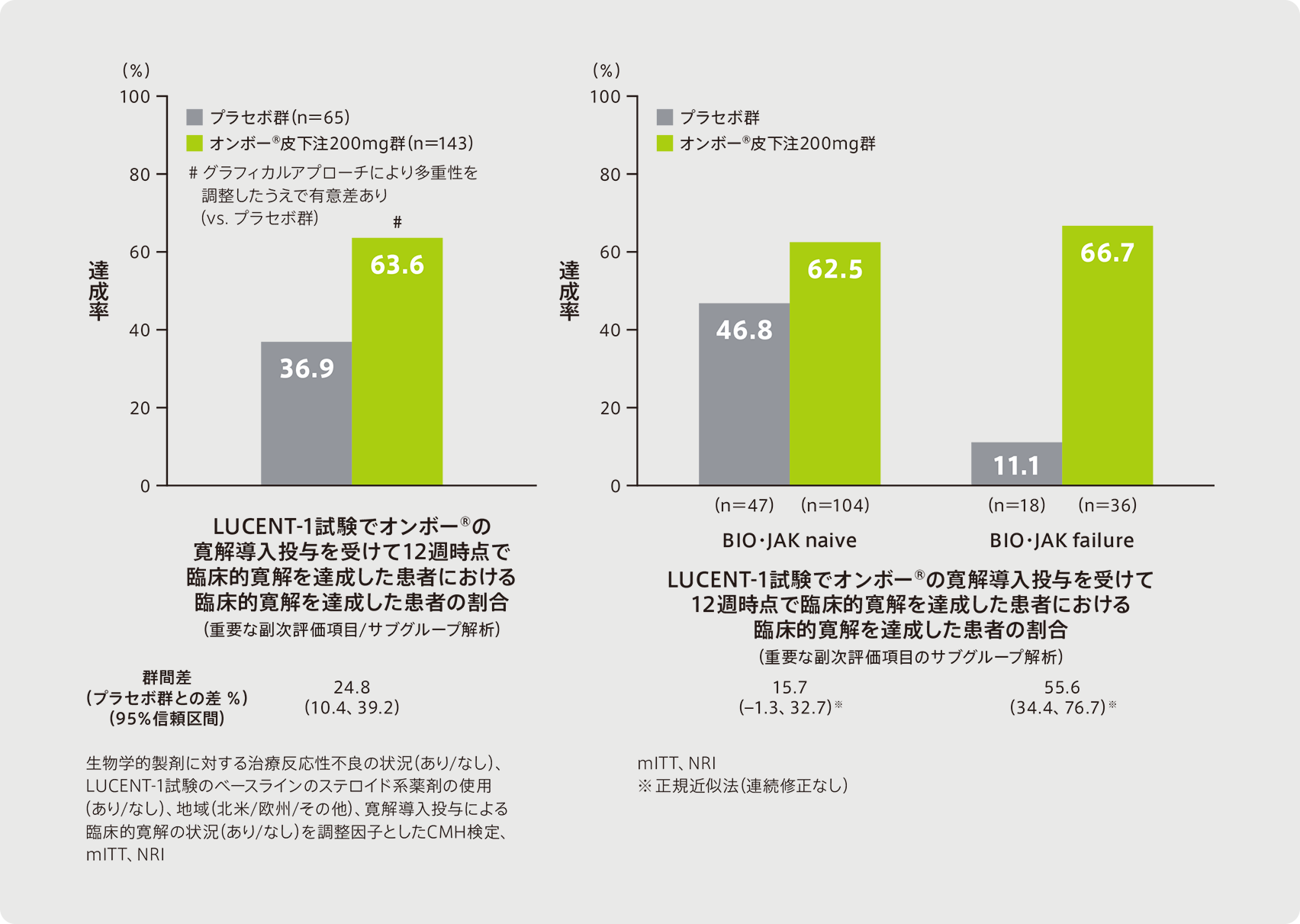
●LUCENT-1試験でオンボー®の寛解導入投与を受けて12週時点で臨床的寛解を達成した患者における40週時点で臨床的寛解を達成した患者の割合
(重要な副次評価項目/サブグループ解析)
(重要な副次評価項目のサブグループ解析)
重要な副次評価項目であるLUCENT-1試験でオンボー®の寛解導入投与を受けて12週時点で臨床的寛解を達成した患者における40週時点で臨床的寛解を達成した患者の割合は、オンボー®皮下注200mg群では63.6%(91/143例)であり、プラセボ群の36.9%(24/65例)と比較して統計学的有意に高いことが示された(p<0.001、CMH検定、多重性調整を実施)。
サブグループ解析であるBIO・JAK naive及びBIO・JAK failureにおける結果は以下のとおりであった。